Ενεργά συστατικά: Βιλνταγλιπτίνη
Galvus δισκία 50 mg
Ενδείξεις Γιατί χρησιμοποιείται το Galvus; Σε τι χρησιμεύει;
Η δραστική ουσία του Galvus, η βιλνταγλιπτίνη, ανήκει σε μια ομάδα φαρμάκων που ονομάζονται «από του στόματος αντιδιαβητικά».
Το Galvus χρησιμοποιείται για τη θεραπεία ενηλίκων ασθενών με διαβήτη τύπου 2. Χρησιμοποιείται όταν ο διαβήτης δεν μπορεί να ελεγχθεί μόνο με δίαιτα και άσκηση. Βοηθά στον έλεγχο του επιπέδου σακχάρου στο αίμα. Ο γιατρός σας θα συνταγογραφήσει Galvus μόνο του ή μαζί. Άλλα αντιδιαβητικά φάρμακα λαμβάνετε ήδη, εάν αυτά δεν έχουν αποδειχθεί ότι είναι αρκετά αποτελεσματικά για τον έλεγχο του διαβήτη.
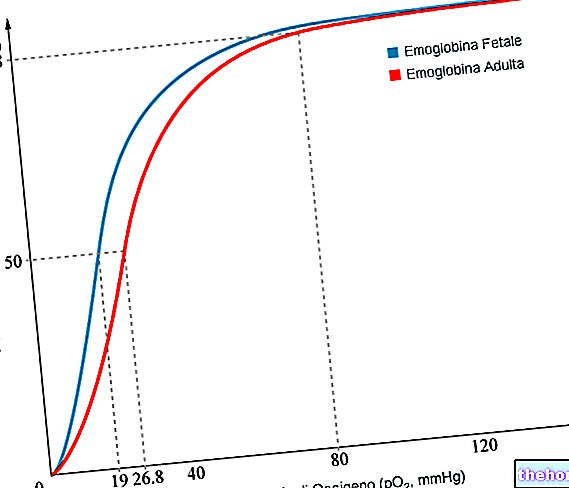
Ο διαβήτης τύπου 2 αναπτύσσεται όταν το σώμα δεν παράγει αρκετή ινσουλίνη ή εάν η ινσουλίνη που παράγει το σώμα δεν λειτουργεί όπως θα έπρεπε. Μπορεί επίσης να αναπτυχθεί όταν το σώμα παράγει υπερβολική γλυκαγόνη.
Η ινσουλίνη είναι μια ουσία που βοηθά στη μείωση των επιπέδων σακχάρου στο αίμα, ειδικά μετά τα γεύματα. Η γλυκαγόνη είναι μια ουσία που ενεργοποιεί την παραγωγή ζάχαρης από το ήπαρ, προκαλώντας αύξηση των επιπέδων σακχάρου στο αίμα. Το πάγκρεας παράγει και τις δύο αυτές ουσίες.
Πώς λειτουργεί ο Galvus
Ο Galvus λειτουργεί προκαλώντας στο πάγκρεας να παράγει περισσότερη ινσουλίνη και λιγότερη γλυκαγόνη. Αυτό βοηθά στον έλεγχο του επιπέδου σακχάρου στο αίμα. Αυτό το φάρμακο έχει αποδειχθεί ότι μειώνει το σάκχαρο στο αίμα. Αυτό μπορεί να βοηθήσει στην πρόληψη επιπλοκών από τον διαβήτη σας. Ακόμα κι αν αρχίσετε να παίρνετε φάρμακα για τον διαβήτη τώρα, είναι σημαντικό να συνεχίσετε να ακολουθείτε τη συνιστώμενη διατροφή και / ή άσκηση.
Αντενδείξεις Όταν το Galvus δεν πρέπει να χρησιμοποιείται
Μην πάρετε το Galvus:
- εάν είστε αλλεργικοί στη βιλνταγλιπτίνη ή σε οποιοδήποτε άλλο συστατικό αυτού του φαρμάκου (αναφέρονται στην παράγραφο 6). Εάν νομίζετε ότι μπορεί να είστε αλλεργικοί στη βιλνταγλιπτίνη ή σε οποιοδήποτε άλλο συστατικό του Galvus, μην πάρετε αυτό το φάρμακο και επικοινωνήστε με το γιατρό σας.
Προφυλάξεις κατά τη χρήση Τι πρέπει να γνωρίζετε πριν πάρετε το Galvus
Μιλήστε με το γιατρό, το φαρμακοποιό ή τη νοσοκόμα σας για τον διαβήτη πριν πάρετε το Galvus
- εάν έχετε διαβήτη τύπου 1 (το σώμα σας δεν παράγει ινσουλίνη) ή εάν έχετε μια κατάσταση που ονομάζεται διαβητική κετοξέωση.
- εάν παίρνετε ένα αντιδιαβητικό φάρμακο γνωστό ως σουλφονυλουρία (εάν το πάρετε μαζί με το Galvus, ο γιατρός σας μπορεί να θέλει να μειώσει τη δόση σουλφονυλουρίας για να αποφύγει τη χαμηλή γλυκόζη στο αίμα [υπογλυκαιμία]).
- εάν έχετε μέτρια ή σοβαρή νεφρική νόσο (θα πρέπει να πάρετε χαμηλότερη δόση Galvus).
- εάν είστε σε αιμοκάθαρση
- εάν έχετε ηπατική νόσο
- εάν πάσχετε από καρδιακή ανεπάρκεια
- εάν έχετε ή είχατε ποτέ παγκρεατική νόσο
Εάν έχετε λάβει προηγουμένως βιλνταγλιπτίνη αλλά έπρεπε να σταματήσετε λόγω ηπατικής νόσου, δεν πρέπει να πάρετε αυτό το φάρμακο.
Οι βλάβες του δέρματος είναι μια συχνή επιπλοκή του διαβήτη. Συνιστάται να ακολουθείτε τις συστάσεις για τη φροντίδα του δέρματος και των ποδιών που σας έδωσε ο γιατρός ή η νοσοκόμα σας. Θα πρέπει επίσης να δώσετε ιδιαίτερη προσοχή στην ανάπτυξη φουσκάλων ή ελκών ενώ παίρνετε το Galvus. Εάν συμβεί αυτό, θα πρέπει να συμβουλευτείτε το γιατρό σας γρήγορα.
Πριν ξεκινήσετε τη θεραπεία με Galvus, θα πραγματοποιηθεί εξέταση για την αξιολόγηση της λειτουργίας του ήπατος, η οποία θα επαναλαμβάνεται κάθε τρεις μήνες κατά τη διάρκεια του πρώτου έτους θεραπείας και περιοδικά στη συνέχεια. Αυτό γίνεται για να ανιχνευθούν σημάδια αυξημένων ηπατικών ενζύμων το συντομότερο δυνατό.
Παιδιά και έφηβοι
Η χρήση του Galvus σε παιδιά και εφήβους έως 18 ετών δεν συνιστάται.
Αλληλεπιδράσεις Ποια φάρμακα ή τρόφιμα μπορούν να τροποποιήσουν την επίδραση του Galvus
Ενημερώστε τον γιατρό ή τον φαρμακοποιό σας εάν παίρνετε, έχετε πάρει πρόσφατα ή μπορεί να πάρετε άλλα φάρμακα.
Ο γιατρός σας μπορεί να θέλει να αλλάξει τη δόση του Galvus εάν παίρνετε άλλα φάρμακα όπως:
- θειαζίδια ή άλλα διουρητικά (που ονομάζονται επίσης δισκία ούρησης) - κορτικοστεροειδή (συνήθως χρησιμοποιούνται για τη θεραπεία της φλεγμονής)
- φάρμακα για τον θυρεοειδή
- ορισμένα φάρμακα που επηρεάζουν το νευρικό σύστημα.
Προειδοποιήσεις Είναι σημαντικό να γνωρίζετε ότι:
Εγκυμοσύνη και θηλασμός
Εάν είστε έγκυος ή θηλάζετε, νομίζετε ότι μπορεί να είστε έγκυος ή σχεδιάζετε να αποκτήσετε παιδί, ζητήστε τη συμβουλή του γιατρού ή του φαρμακοποιού σας πριν πάρετε αυτό το φάρμακο.
Δεν πρέπει να χρησιμοποιείτε το Galvus κατά τη διάρκεια της εγκυμοσύνης. Δεν είναι γνωστό εάν το Galvus περνά στο μητρικό γάλα. Δεν πρέπει να χρησιμοποιείτε το Galvus εάν θηλάζετε ή σκοπεύετε να θηλάσετε.
Οδήγηση και χειρισμός μηχανών
Εάν αισθάνεστε ζάλη όταν παίρνετε το Galvus, μην οδηγείτε ή χειρίζεστε μηχανές.
Το Galvus περιέχει λακτόζη
Το Galvus περιέχει λακτόζη (ζάχαρη γάλακτος). Εάν σας έχει πει ο γιατρός σας ότι έχετε δυσανεξία σε ορισμένα σάκχαρα, επικοινωνήστε με το γιατρό σας πριν πάρετε αυτό το φαρμακευτικό προϊόν.
Δόση, μέθοδος και χρόνος χορήγησης Πώς να χρησιμοποιήσετε το Galvus: Δοσολογία
Πάντοτε να παίρνετε αυτό το φάρμακο σύμφωνα με τις οδηγίες του γιατρού σας. Σε περίπτωση αμφιβολίας, συμβουλευτείτε το γιατρό ή το φαρμακοποιό σας.
Πόσα να πάρετε και πότε
Η ποσότητα Galvus που πρέπει να ληφθεί ποικίλλει ανάλογα με τις μεμονωμένες συνθήκες. Ο γιατρός σας θα σας πει πόσα δισκία Galvus πρέπει να πάρετε. Η μέγιστη ημερήσια δόση είναι 100 mg.
Η συνήθης δόση του Galvus είναι:
- 50 mg ημερησίως ως εφάπαξ δόση το πρωί εάν πάρετε το Galvus με άλλο φάρμακο που ονομάζεται σουλφονυλουρία.
- 100 mg ημερησίως λαμβανόμενα ως 50 mg το πρωί και 50 mg το βράδυ εάν παίρνετε μόνο το Galvus, με άλλο φάρμακο που ονομάζεται μετφορμίνη ή γλιταζόνη, με συνδυασμό μετφορμίνης και σουλφονυλουρίας ή με ινσουλίνη.
- 50 mg ημερησίως το πρωί εάν έχετε μέτρια ή σοβαρή νεφρική νόσο ή είστε σε αιμοκάθαρση.
Πώς να πάρετε το Galvus
- Καταπιείτε τα δισκία με λίγο νερό.
Πόσο καιρό να πάρετε το Galvus
- Πάρτε το Galvus κάθε μέρα για όσο διάστημα σας συστήνει ο γιατρός σας. Σως χρειαστεί να συνεχίσετε αυτήν τη θεραπεία για μεγάλο χρονικό διάστημα.
- Ο γιατρός σας θα ελέγχει τακτικά την κατάστασή σας για να βεβαιωθεί ότι η θεραπεία έχει το επιθυμητό αποτέλεσμα.
Εάν ξεχάσετε να πάρετε το Galvus
Εάν ξεχάσετε να πάρετε μια δόση αυτού του φαρμάκου, πάρτε το μόλις το θυμηθείτε. Στη συνέχεια, πάρτε την επόμενη δόση τη συνήθη ώρα. Εάν πλησιάζει η ώρα για την επόμενη δόση σας, παραλείψτε τη χαμένη δόση. Μην πάρετε διπλή δόση για να αναπληρώσετε το δισκίο που ξεχάσατε.
Εάν σταματήσετε να παίρνετε το Galvus
Μην σταματήσετε να παίρνετε το Galvus εκτός εάν σας το πει ο γιατρός σας. Εάν δεν είστε σίγουροι για το πόσο καιρό θα παίρνετε αυτό το φάρμακο, ρωτήστε το γιατρό σας.
Υπερδοσολογία Τι πρέπει να κάνετε εάν έχετε πάρει πάρα πολύ Galvus
Εάν παίρνετε πάρα πολλά δισκία Galvus ή εάν κάποιος άλλος έχει πάρει το φάρμακό σας, επικοινωνήστε αμέσως με το γιατρό σας. Μπορεί να απαιτείται ιατρική φροντίδα. Εάν πρέπει να δείτε γιατρό ή να πάτε στο νοσοκομείο, πάρτε τη συσκευασία μαζί σας.
Παρενέργειες Ποιες είναι οι παρενέργειες του Galvus
Όπως όλα τα φάρμακα, έτσι και αυτό το φάρμακο μπορεί να προκαλέσει ανεπιθύμητες ενέργειες, αν και δεν παρουσιάζονται σε όλους τους ανθρώπους.
Ορισμένα συμπτώματα απαιτούν άμεση ιατρική φροντίδα:
Πρέπει να σταματήσετε να παίρνετε το Galvus και να επικοινωνήσετε αμέσως με το γιατρό σας εάν εμφανιστεί κάποια από τις ακόλουθες ανεπιθύμητες ενέργειες:
- Αγγειοοίδημα (σπάνιο: μπορεί να επηρεάσει έως 1 στα 1.000 άτομα): Τα συμπτώματα περιλαμβάνουν πρήξιμο του προσώπου, της γλώσσας ή του λαιμού, δυσκολία στην κατάποση, δυσκολία στην αναπνοή, ξαφνικό εξάνθημα ή κνίδωση, που μπορεί να υποδηλώνουν μια αντίδραση που ονομάζεται "αγγειοοίδημα".
- Ηπατική νόσος (ηπατίτιδα) (σπάνια): Τα συμπτώματα περιλαμβάνουν κίτρινο δέρμα και μάτια, ναυτία, απώλεια όρεξης ή σκουρόχρωμα ούρα, που μπορεί να υποδηλώνουν ηπατική νόσο (ηπατίτιδα).
- Φλεγμονή του παγκρέατος (παγκρεατίτιδα) (η συχνότητα δεν είναι γνωστή). Τα συμπτώματα περιλαμβάνουν έντονο και επίμονο πόνο στην κοιλιά (περιοχή του στομάχου) που μπορεί να επεκταθεί στην πλάτη, καθώς και ναυτία και έμετος.
Άλλες παρενέργειες
Μερικοί ασθενείς εμφάνισαν τις ακόλουθες ανεπιθύμητες ενέργειες κατά τη λήψη του Galvus και της μετφορμίνης:
- Συχνές (μπορεί να επηρεάσουν έως 1 στα 10 άτομα): τρόμο, πονοκέφαλο, ζάλη, ναυτία, χαμηλά επίπεδα γλυκόζης στο αίμα.
- Όχι συχνές (μπορεί να επηρεάσουν έως 1 στα 100 άτομα): κόπωση.
Μερικοί ασθενείς εμφάνισαν τις ακόλουθες ανεπιθύμητες ενέργειες κατά τη λήψη του Galvus και μιας σουλφονυλουρίας:
- Συχνές: τρόμος, πονοκέφαλος, ζάλη, αδυναμία, χαμηλά επίπεδα γλυκόζης στο αίμα.
- Όχι συχνές: δυσκοιλιότητα.
- Πολύ σπάνια (μπορεί να επηρεάσει έως 1 στα 10.000 άτομα): πονόλαιμος, καταρροή.
Μερικοί ασθενείς εμφάνισαν τις ακόλουθες ανεπιθύμητες ενέργειες κατά τη λήψη του Galvus και μιας γλιταζόνης:
- Συχνές: αύξηση βάρους, πρήξιμο των χεριών, των αστραγάλων ή των ποδιών (οίδημα).
- Όχι συχνές: πονοκέφαλος, αδυναμία, χαμηλά επίπεδα γλυκόζης στο αίμα.
Μερικοί ασθενείς εμφάνισαν τις ακόλουθες ανεπιθύμητες ενέργειες ενώ έπαιρναν μόνο το Galvus:
- Συχνές: ζάλη.
- Όχι συχνές: πονοκέφαλος, δυσκοιλιότητα, πρήξιμο των χεριών, των αστραγάλων ή των ποδιών (οίδημα), πόνος στις αρθρώσεις, χαμηλά επίπεδα γλυκόζης στο αίμα.
- Πολύ σπάνια: πονόλαιμος, καταρροή, πυρετός.
Μερικοί ασθενείς εμφάνισαν τις ακόλουθες ανεπιθύμητες ενέργειες κατά τη λήψη Galvus, μετφορμίνης και σουλφονυλουρίας:
- Συχνές: ζάλη, τρόμος, αδυναμία, χαμηλή γλυκόζη στο αίμα, υπερβολική εφίδρωση.
Μερικοί ασθενείς εμφάνισαν τις ακόλουθες ανεπιθύμητες ενέργειες κατά τη λήψη Galvus και ινσουλίνης (με ή χωρίς μετφορμίνη):
- Συχνές: πονοκέφαλος, ρίγη, ναυτία (αίσθημα αδιαθεσίας), χαμηλά επίπεδα γλυκόζης στο αίμα, καούρα.
- Όχι συχνές: διάρροια, μετεωρισμός.
Οι ακόλουθες ανεπιθύμητες ενέργειες έχουν επίσης αναφερθεί κατά την κυκλοφορία αυτού του φαρμάκου:
- Η συχνότητα είναι άγνωστη (δεν μπορεί να εκτιμηθεί από τα διαθέσιμα δεδομένα): κνησμώδες εξάνθημα, φλεγμονή του παγκρέατος, εντοπισμένο ξεφλούδισμα του δέρματος ή φουσκάλες, μυϊκός πόνος.
Αναφορά παρενεργειών
Εάν παρατηρήσετε κάποια ανεπιθύμητη ενέργεια, μιλήστε με το γιατρό, το φαρμακοποιό ή τη νοσοκόμα σας για τον διαβήτη. Αυτό περιλαμβάνει τυχόν ανεπιθύμητες ενέργειες που δεν αναφέρονται στο παρόν φύλλο οδηγιών χρήσης. Μπορείτε επίσης να αναφέρετε ανεπιθύμητες ενέργειες απευθείας μέσω του εθνικού συστήματος αναφοράς που παρατίθεται στο Παράρτημα V. Αναφέροντας ανεπιθύμητες ενέργειες μπορείτε να βοηθήσετε στην παροχή περισσότερων πληροφοριών σχετικά με την ασφάλεια αυτού του φαρμάκου.
Λήξη και διατήρηση
- Κρατήστε αυτό το φάρμακο μακριά από τα μάτια και την πρόσβαση των παιδιών.
- Μην χρησιμοποιείτε αυτό το φάρμακο μετά την ημερομηνία λήξης που αναφέρεται στην κυψέλη και στο κουτί μετά το "ΛΗΞΗ" / "ΛΗΞΗ". Η ημερομηνία λήξης αναφέρεται στην τελευταία ημέρα του μήνα.
- Φυλάσσετε στην αρχική συσκευασία για προστασία από την υγρασία.
- Μη χρησιμοποιείτε συσκευασία Galvus που έχει υποστεί ζημιά ή παρουσιάζει σημάδια παραποίησης.
Λήξη "> Άλλες αλληλεπιδράσεις
Τι περιέχει το Galvus
- Το δραστικό συστατικό είναι η βιλνταγλιπτίνη. Κάθε δισκίο περιέχει 50 mg βιλνταγλιπτίνης.
- Τα άλλα συστατικά είναι άνυδρη λακτόζη, μικροκρυσταλλική κυτταρίνη, γλυκολικό άμυλο νατρίου (τύπου Α) και στεατικό μαγνήσιο.
Περιγραφή της εμφάνισης του Galvus και περιεχόμενο της συσκευασίας
Τα δισκία Galvus 50 mg είναι στρογγυλά, επίπεδα, λευκά έως ελαφρώς κιτρινωπά, με "NVR" στη μία πλευρά και "FB" στην άλλη.
Τα δισκία Galvus 50 mg διατίθενται σε συσκευασίες που περιέχουν 7, 14, 28, 30, 56, 60, 90, 112, 180 ή 336 δισκία και σε πολλαπλές συσκευασίες που περιέχουν 3 κουτιά, το καθένα περιέχει 112 δισκία.
Μπορεί να μην κυκλοφορούν όλες οι συσκευασίες στη χώρα σας.
Φύλλο οδηγιών χρήσης: AIFA (Ιταλικός Οργανισμός Φαρμάκων). Περιεχόμενο που δημοσιεύτηκε τον Ιανουάριο 2016. Οι πληροφορίες που υπάρχουν δεν μπορεί να είναι ενημερωμένες.
Για να έχετε πρόσβαση στην πιο ενημερωμένη έκδοση, είναι σκόπιμο να αποκτήσετε πρόσβαση στον ιστότοπο AIFA (Ιταλικός Οργανισμός Φαρμάκων). Αποποίηση ευθυνών και χρήσιμες πληροφορίες.
01.0 ΟΝΟΜΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟDΟΝΤΟΣ -
ΤΑΜΠΛΕΤΕΣ GALVUS 50 MG
02.0 ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ -
Κάθε δισκίο περιέχει 50 mg βιλνταγλιπτίνης.
Έκδοχο με γνωστή δράση: κάθε δισκίο περιέχει 47,82 mg λακτόζης (άνυδρη).
Για τον πλήρη κατάλογο των εκδόχων, ανατρέξτε στην ενότητα 6.1.
03.0 ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ ΜΟΡΦΗ -
Δισκίο.
Στρογγυλό (διάμετρος 8 mm), λευκό έως ελαφρώς κιτρινωπό, επίπεδο δισκίο με λοξότμητες άκρες.
Τα γράμματα "NVR" είναι ανάγλυφα στη μία πλευρά, "FB" στην άλλη.
04.0 ΚΛΙΝΙΚΕΣ ΠΛΗΡΟΦΟΡΙΕΣ -
04.1 Θεραπευτικές ενδείξεις -
Η βιλνταγλιπτίνη ενδείκνυται για τη θεραπεία του σακχαρώδους διαβήτη τύπου 2 σε ενήλικες:
Στη μονοθεραπεία
- σε ασθενείς που δεν ελέγχονται επαρκώς μόνο με δίαιτα και άσκηση και για τους οποίους η θεραπεία με μετφορμίνη είναι ακατάλληλη λόγω αντενδείξεων ή δυσανεξίας.
Σε διπλή στοματική θεραπεία σε συνδυασμό με:
- μετφορμίνη, σε ασθενείς με ανεπαρκή γλυκαιμικό έλεγχο παρά τη χορήγηση της μέγιστης ανεκτής δόσης μετφορμίνης μόνο,
- σουλφονυλουρία, σε ασθενείς με ανεπαρκή γλυκαιμικό έλεγχο παρά τη χορήγηση της μέγιστης ανεκτής δόσης σουλφονυλουρίας και για τους οποίους η θεραπεία με μετφορμίνη είναι ακατάλληλη λόγω αντενδείξεων ή δυσανεξίας,
- μια θειαζολιδινοδιόνη, σε ασθενείς με ανεπαρκή γλυκαιμικό έλεγχο και για τους οποίους η χρήση μιας θειαζολιδινοδιόνης είναι κατάλληλη.
Σε τριπλή από του στόματος θεραπεία σε συνδυασμό με:
- μια σουλφονυλουρία και μετφορμίνη όταν η δίαιτα και η άσκηση που σχετίζονται με διπλή θεραπεία με αυτά τα φάρμακα δεν παρέχουν επαρκή γλυκαιμικό έλεγχο.
Η βιλνταγλιπτίνη ενδείκνυται επίσης για χρήση σε συνδυασμό με ινσουλίνη (με ή χωρίς μετφορμίνη) όταν η δίαιτα και η άσκηση σε συνδυασμό με σταθερή δόση ινσουλίνης δεν παρέχουν επαρκή γλυκαιμικό έλεγχο.
04.2 Δοσολογία και τρόπος χορήγησης -
Δοσολογία
Ενήλικες
Όταν χρησιμοποιείται μόνο του, σε συνδυασμό με μετφορμίνη, σε συνδυασμό με θειαζολιδινοδιόνη, σε συνδυασμό με μετφορμίνη και σουλφονυλουρία ή σε συνδυασμό με ινσουλίνη (με ή χωρίς μετφορμίνη), η συνιστώμενη ημερήσια δόση βιλνταγλιπτίνης είναι 100 mg, χορηγούμενη σε μία δόση. 50 mg το πρωί και δόση 50 mg το βράδυ.
Όταν χρησιμοποιείται σε διπλή θεραπεία σε συνδυασμό με σουλφονυλουρία, η συνιστώμενη δόση βιλνταγλιπτίνης είναι 50 mg μία φορά ημερησίως χορηγούμενη το πρωί. Σε αυτόν τον πληθυσμό ασθενών, η βιλνταγλιπτίνη 100 mg ημερησίως δεν ήταν πιο αποτελεσματική από τη βιλνταγλιπτίνη 50 mg μία φορά την ημέρα.
Όταν χρησιμοποιείται σε συνδυασμό με σουλφονυλουρία, χαμηλότερη δόση σουλφονυλουρίας μπορεί να θεωρηθεί ότι μειώνει τον κίνδυνο υπογλυκαιμίας.
Δεν συνιστώνται δόσεις άνω των 100 mg.
Εάν παραλείψετε μια δόση Galvus, θα πρέπει να ληφθεί μόλις ο ασθενής το θυμηθεί.
Δεν πρέπει να λαμβάνεται διπλή δόση την ίδια ημέρα.
Η ασφάλεια και η αποτελεσματικότητα της βιλνταγλιπτίνης ως από του στόματος τριπλής θεραπείας σε συνδυασμό με μετφορμίνη και θειαζολιδινοδιόνη δεν έχουν τεκμηριωθεί.
Πρόσθετες πληροφορίες για συγκεκριμένους πληθυσμούς ασθενών
Ηλικιωμένοι (≥ 65 ετών)
Δεν απαιτείται προσαρμογή της δόσης σε ηλικιωμένους ασθενείς (βλ. Επίσης παραγράφους 5.1 και 5.2).
Διαταραχή της νεφρικής λειτουργίας
Δεν απαιτείται προσαρμογή της δόσης σε ασθενείς με ήπια διαταραχή της νεφρικής λειτουργίας (εκτελωνισμός κρεατινίνη ≥ 50 ml / min). Σε ασθενείς με μέτρια ή σοβαρή νεφρική δυσλειτουργία ή νεφρική νόσο τελικού σταδίου (ESRD), η συνιστώμενη δόση του Galvus είναι 50 mg άπαξ ημερησίως (βλ. Επίσης παραγράφους 4.4, 5.1 και 5.2).
Διαταραχή της ηπατικής λειτουργίας
Το Galvus δεν πρέπει να χρησιμοποιείται σε ασθενείς με ηπατική δυσλειτουργία, συμπεριλαμβανομένων ασθενών που έχουν αμινοτρανσφεράση αλανίνης (ALT) ή ασπαρτική αμινοτρανσφεράση (AST)> 3x ανώτερο φυσιολογικό όριο (ULN) πριν από τη θεραπεία (βλ. Επίσης παραγράφους 4.4 και 5.2).
Παιδιατρικός πληθυσμός
Η χρήση του Galvus δεν συνιστάται σε παιδιά και εφήβους (
Τρόπος χορήγησης
Χρήση από το στόμα
Το Galvus μπορεί να ληφθεί με ή χωρίς τροφή (βλέπε επίσης παράγραφο 5.2).
04.3 Αντενδείξεις -
Υπερευαισθησία στη δραστική ουσία ή σε κάποιο από τα έκδοχα που αναφέρονται στην παράγραφο 6.1.
04.4 Ειδικές προειδοποιήσεις και κατάλληλες προφυλάξεις κατά τη χρήση -
Γενικός
Το Galvus δεν υποκαθιστά την ινσουλίνη σε ασθενείς που εξαρτώνται από την ινσουλίνη. Το Galvus δεν πρέπει να χρησιμοποιείται σε ασθενείς με διαβήτη τύπου 1 ή για τη θεραπεία της διαβητικής κετοξέωσης.
Διαταραχή της νεφρικής λειτουργίας
Η εμπειρία σε ασθενείς με αιμοκάθαρση με ESRD είναι περιορισμένη. Επομένως, το Galvus πρέπει να χρησιμοποιείται με προσοχή σε αυτούς τους ασθενείς (βλ. Επίσης παραγράφους 4.2, 5.1 και 5.2).
Διαταραχή της ηπατικής λειτουργίας
Το Galvus δεν πρέπει να χρησιμοποιείται σε ασθενείς με ηπατική δυσλειτουργία, συμπεριλαμβανομένων ασθενών με ALT ή AST πριν από τη θεραπεία> 3x ULN (βλ. Επίσης παραγράφους 4.2 και 5.2).
Παρακολούθηση των ηπατικών ενζύμων
Έχουν αναφερθεί σπάνιες περιπτώσεις ηπατικής δυσλειτουργίας (συμπεριλαμβανομένης της ηπατίτιδας). Σε αυτές τις περιπτώσεις, οι ασθενείς ήταν γενικά ασυμπτωματικοί χωρίς κλινικές συνέπειες και οι δοκιμασίες ηπατικής λειτουργίας επανήλθαν στο φυσιολογικό μετά τη διακοπή της θεραπείας. Θα πρέπει να γίνουν δοκιμές ηπατικής λειτουργίας πριν από την έναρξη της θεραπείας με Galvus για να γνωρίζετε την αρχική τιμή του ασθενούς. Κατά τη διάρκεια της θεραπείας με Galvus, η ηπατική λειτουργία πρέπει να ελέγχεται κάθε τρεις μήνες κατά τη διάρκεια του πρώτου έτους θεραπείας και περιοδικά στη συνέχεια. Οι ασθενείς που αναπτύσσουν αυξημένα επίπεδα τρανσαμινασών θα πρέπει να ελέγχονται με μια δεύτερη αξιολόγηση της ηπατικής λειτουργίας για να επιβεβαιώσουν τα αποτελέσματα και στη συνέχεια να παρακολουθούνται με συχνές δοκιμές ηπατικής λειτουργίας έως ότου η ανωμαλία (ες) επιστρέψει στο φυσιολογικό. Εάν η αύξηση του AST ή του ALT επιμένει 3 φορές από το ανώτερο όριο του φυσιολογικού ή άνω, συνιστάται η διακοπή της θεραπείας με Galvus. Οι ασθενείς που εμφανίζουν ίκτερο ή άλλα σημάδια που υποδηλώνουν ηπατική δυσλειτουργία θα πρέπει να διακόψουν τη θεραπεία με Galvus.
Μετά τη διακοπή της θεραπείας με Galvus και την ομαλοποίηση των παραμέτρων της ηπατικής λειτουργίας, η θεραπεία με Galvus δεν πρέπει να επαναληφθεί.
Συγκοπή
Μια κλινική μελέτη της βιλνταγλιπτίνης σε ασθενείς στις λειτουργικές τάξεις Ι-ΙΙΙ της Νέας Υόρκης (NYHA) έδειξε ότι η θεραπεία με βιλνταγλιπτίνη δεν συσχετίστηκε με αλλαγές στη λειτουργία της αριστερής κοιλίας ή επιδείνωση της προϋπάρχουσας συμφορητικής καρδιακής ανεπάρκειας (CHF) σε σύγκριση με το εικονικό φάρμακο. η εμπειρία σε ασθενείς με λειτουργική κλάση III της NYHA που έλαβαν βιλνταγλιπτίνη εξακολουθεί να είναι περιορισμένη και τα αποτελέσματα είναι ασαφή (βλ. παράγραφο 5.1).
Δεν υπάρχει εμπειρία με τη χρήση της βιλνταγλιπτίνης σε κλινικές δοκιμές σε ασθενείς με NYHA λειτουργικής κατηγορίας IV και επομένως η χρήση της δεν συνιστάται σε αυτούς τους ασθενείς.
Διαταραχές του δέρματος
Σε μη κλινικές μελέτες τοξικολογίας, δερματικές βλάβες, συμπεριλαμβανομένων φουσκάλων και εξελκώσεων, έχουν αναφερθεί στα άκρα πιθήκων (βλ. Παράγραφο 5.3). Παρόλο που δεν παρατηρήθηκε «αυξημένη επίπτωση δερματικών βλαβών» σε κλινικές δοκιμές, υπήρξε περιορισμένη εμπειρία σε ασθενείς με διαβητικές επιπλοκές του δέρματος. Επιπλέον, έχουν υπάρξει αναφορές μετά την κυκλοφορία για βολικές και απολεπιστικές βλάβες του δέρματος. Σύμφωνα με τη συνήθη περίθαλψη του διαβητικού ασθενούς, συνιστάται επομένως η παρακολούθηση τυχόν δερματικών παθήσεων, όπως φουσκάλες και έλκη.
Οξεία παγκρεατίτιδα
Η χρήση της βιλνταγλιπτίνης έχει συσχετιστεί με κίνδυνο ανάπτυξης οξείας παγκρεατίτιδας Οι ασθενείς πρέπει να ενημερώνονται για το χαρακτηριστικό σύμπτωμα της οξείας παγκρεατίτιδας.
Εάν υπάρχει υποψία για παγκρεατίτιδα, η βιλνταγλιπτίνη πρέπει να διακόπτεται. εάν επιβεβαιωθεί η οξεία παγκρεατίτιδα, η βιλνταγλιπτίνη δεν πρέπει να ξαναρχίσει. Πρέπει να δίνεται προσοχή σε ασθενείς με ιστορικό οξείας παγκρεατίτιδας.
Υπογλυκαιμία
Οι σουλφονυλουρίες είναι γνωστό ότι προκαλούν υπογλυκαιμία. Ασθενείς που λαμβάνουν βιλνταγλιπτίνη σε συνδυασμό με σουλφονυλουρία μπορεί να διατρέχουν κίνδυνο υπογλυκαιμίας. Επομένως, μια χαμηλότερη δόση σουλφονυλουρίας μπορεί να θεωρηθεί ότι μειώνει τον κίνδυνο υπογλυκαιμίας.
Έκδοχα
Τα δισκία περιέχουν λακτόζη. Ασθενείς με σπάνια κληρονομικά προβλήματα δυσανεξίας στη γαλακτόζη, ανεπάρκεια λακτάσης Lapp ή δυσαπορρόφηση γλυκόζης-γαλακτόζης δεν πρέπει να λαμβάνουν αυτό το φάρμακο.
04.5 Αλληλεπιδράσεις με άλλα φαρμακευτικά προϊόντα και άλλες μορφές αλληλεπίδρασης -
Η βιλνταγλιπτίνη έχει χαμηλές δυνατότητες αλληλεπίδρασης όταν συνδυάζεται με άλλα φαρμακευτικά προϊόντα. Δεδομένου ότι η βιλνταγλιπτίνη δεν είναι υπόστρωμα του ενζύμου κυτοχρώματος P (CYP) 450 και δεν αναστέλλει ή επάγει ένζυμα CYP 450, δεν είναι πιθανή η αλληλεπίδραση με δραστικές ουσίες που είναι υποστρώματα, αναστολείς ή επαγωγείς αυτών των ενζύμων.
Συνδυασμός με πιογλιταζόνη, μετφορμίνη και γλιβενκλαμίδη
Τα αποτελέσματα των μελετών που πραγματοποιήθηκαν με αυτά τα από του στόματος αντιδιαβητικά δεν αποκάλυψαν κλινικά σχετικές φαρμακοκινητικές αλληλεπιδράσεις.
Διγοξίνη (υπόστρωμα ρ-γλυκοπρωτεΐνης), βαρφαρίνη (υπόστρωμα CYP2C9)
Κλινικές μελέτες που πραγματοποιήθηκαν με υγιή άτομα δεν αποκάλυψαν κλινικά σχετικές φαρμακοκινητικές αλληλεπιδράσεις. Ωστόσο, αυτά τα στοιχεία δεν επιβεβαιώθηκαν στον πληθυσμό αναφοράς.
Συνδυασμός με αμλοδιπίνη, ραμιπρίλη, βαλσαρτάνη ή σιμβαστατίνη
Μελέτες αλληλεπίδρασης φαρμάκου με φαρμακευτική αγωγή πραγματοποιήθηκαν με αμλοδιπίνη, ραμιπρίλη, βαλσαρτάνη και σιμβαστατίνη σε υγιή άτομα. Σε αυτές τις μελέτες, δεν παρατηρήθηκαν κλινικά σχετικές φαρμακοκινητικές αλληλεπιδράσεις μετά από συγχορήγηση με βιλνταγλιπτίνη.
Όπως και με άλλα αντιδιαβητικά από το στόμα, η υπογλυκαιμική δράση της βιλνταγλιπτίνης μπορεί να μειωθεί από ορισμένες δραστικές ουσίες, όπως θειαζίδια, κορτικοστεροειδή, φάρμακα για τον θυρεοειδή και συμπαθομιμητικά.
04.6 Κύηση και θηλασμός -
Εγκυμοσύνη
Δεν υπάρχουν επαρκή δεδομένα από τη χρήση της βιλνταγλιπτίνης σε έγκυες γυναίκες. Μελέτες σε ζώα έδειξαν τοξικότητα στην αναπαραγωγή σε υψηλές δόσεις (βλ. Παράγραφο 5.3). Ο δυνητικός κίνδυνος για τους ανθρώπους είναι άγνωστος. Λόγω έλλειψης ανθρώπινων δεδομένων, το Galvus δεν πρέπει να χρησιμοποιείται κατά τη διάρκεια εγκυμοσύνη.
Ωρα ταίσματος
Είναι άγνωστο εάν η βιλνταγλιπτίνη απεκκρίνεται στο ανθρώπινο γάλα. Μελέτες σε ζώα έχουν δείξει απέκκριση της βιλνταγλιπτίνης στο γάλα. Το Galvus δεν πρέπει να χρησιμοποιείται κατά τη διάρκεια της γαλουχίας.
Γονιμότητα
Δεν έχουν διεξαχθεί μελέτες για την επίδραση του Galvus στην ανθρώπινη γονιμότητα (βλ. Παράγραφο 5.3).
04.7 Επιδράσεις στην ικανότητα οδήγησης και χειρισμού μηχανών -
Δεν έχουν πραγματοποιηθεί μελέτες σχετικά με την ικανότητα οδήγησης και χειρισμού μηχανών. Οι ασθενείς που εμφανίζουν ζάλη ως ανεπιθύμητη ενέργεια πρέπει να αποφεύγουν την οδήγηση ή το χειρισμό μηχανών.
04.8 Ανεπιθύμητες ενέργειες -
Περίληψη του προφίλ ασφαλείας
Τα δεδομένα ασφάλειας ελήφθησαν από συνολικά 3.784 ασθενείς που εκτέθηκαν σε ημερήσιες δόσεις βιλνταγλιπτίνης των 50 mg (άπαξ ημερησίως) ή 100 mg (50 mg δύο φορές ημερησίως ή 100 mg μία φορά ημερησίως) σε ελεγχόμενες μελέτες. Διάρκειας τουλάχιστον 12 εβδομάδων. Από αυτούς τους ασθενείς, 2.264 έλαβαν μόνο βιλνταγλιπτίνη και 1.520 έλαβαν βιλνταγλιπτίνη σε συνδυασμό με άλλο φάρμακο. 2.682 ασθενείς έλαβαν θεραπεία με βιλνταγλιπτίνη 100 mg ημερησίως (50 mg δύο φορές ημερησίως ή 100 mg μία φορά ημερησίως) και 1.102 ασθενείς έλαβαν θεραπεία με βιλνταγλιπτίνη 50 mg μία φορά ημερησίως.
Οι περισσότερες ανεπιθύμητες ενέργειες σε αυτές τις κλινικές δοκιμές ήταν ήπιες και παροδικές και δεν απαιτούσαν διακοπή της θεραπείας. Δεν υπήρχε συσχέτιση μεταξύ ανεπιθύμητων ενεργειών και ηλικίας, εθνικότητας, διάρκειας έκθεσης ή ημερήσιας δόσης.
Έχουν αναφερθεί σπάνιες περιπτώσεις ηπατικής δυσλειτουργίας (συμπεριλαμβανομένης της ηπατίτιδας). Σε αυτές τις περιπτώσεις, οι ασθενείς ήταν γενικά ασυμπτωματικοί χωρίς κλινικές συνέπειες και οι δοκιμασίες ηπατικής λειτουργίας επανήλθαν στο φυσιολογικό μετά τη διακοπή της θεραπείας. Από δεδομένα από ελεγχόμενες μονοθεραπείες ή συμπληρωματικές θεραπείες διάρκειας έως 24 εβδομάδων, η συχνότητα εμφάνισης αυξήσεων ALT ή AST times 3 φορές του ανώτερου φυσιολογικού ορίου (ταξινομείται ως παρούσα σε τουλάχιστον 2 διαδοχικούς ελέγχους ή στην τελική επίσκεψη κατά τη διάρκεια της θεραπείας) ήταν 0,2%, 0,3% και 0,2% για τη βιλνταγλιπτίνη 50 mg μία φορά ημερησίως, τη βιλνταγλιπτίνη 50 mg δύο φορές την ημέρα και όλα τα συγκριτικά, αντίστοιχα. Αυτές οι αυξήσεις των τρανσαμινασών ήταν γενικά ασυμπτωματικές, μη προοδευτικής φύσης και δεν σχετίζονται με χολόσταση ή ίκτερο.
Έχουν αναφερθεί σπάνιες περιπτώσεις αγγειοοιδήματος με βιλνταγλιπτίνη, με συχνότητα παρόμοια με την ομάδα ελέγχου. Η πλειονότητα των περιπτώσεων αναφέρθηκε όταν η βιλνταγλιπτίνη χορηγήθηκε σε συνδυασμό με αναστολέα ενζύμου αγγειοτασίνης (αναστολέας ΜΕΑ). Τα περισσότερα συμβάντα ήταν μέτριας σοβαρότητας και επιλύθηκαν κατά τη διάρκεια της θεραπείας με βιλνταγλιπτίνη.
Πίνακας ανεπιθύμητων ενεργειών
Οι ανεπιθύμητες ενέργειες που αναφέρθηκαν σε ασθενείς που έλαβαν Galvus σε διπλές τυφλές μελέτες ως μονοθεραπεία και πρόσθετη θεραπεία παρατίθενται παρακάτω για κάθε ένδειξη ανά κατηγορία οργάνου συστήματος και απόλυτη συχνότητα. Οι συχνότητες ορίζονται ως πολύ συχνές (≥1 / 10), κοινές (≥1 / 100,
Συνδυασμός με μετφορμίνη
Πίνακας 1 Ανεπιθύμητες ενέργειες που αναφέρθηκαν σε ασθενείς που έλαβαν Galvus 100 mg ημερησίως σε πρόσθετο συνδυασμό με μετφορμίνη σε διπλές τυφλές μελέτες (N = 208)
Περιγραφή επιλεγμένων ανεπιθύμητων ενεργειών
Σε ελεγχόμενες κλινικές δοκιμές που πραγματοποιήθηκαν με συνδυασμό βιλνταγλιπτίνης 100 mg ημερησίως + μετφορμίνη, δεν αναφέρθηκαν ανακλήσεις λόγω ανεπιθύμητων ενεργειών είτε στην ομάδα βιλνταγλιπτίνης 100 mg ημερησίως + ομάδα μετφορμίνης είτε στην ομάδα εικονικού φαρμάκου + μετφορμίνη. Σε κλινικές μελέτες, η συχνότητα υπογλυκαιμίας ήταν συχνή σε ασθενείς που έλαβαν βιλνταγλιπτίνη 100 mg ημερησίως σε συνδυασμό με μετφορμίνη (1%) και όχι συχνές σε ασθενείς που έλαβαν εικονικό φάρμακο + μετφορμίνη (0,4%). Δεν αναφέρθηκαν σοβαρά υπογλυκαιμικά συμβάντα στα χέρια της βιλνταγλιπτίνης.
Σε κλινικές μελέτες, το βάρος δεν άλλαξε από την αρχική τιμή όταν βιλνταγλιπτίνη 100 mg ημερησίως προστέθηκε σε μετφορμίνη (+0,2 κιλά και -1,0 κιλά για βιλνταγλιπτίνη και εικονικό φάρμακο, αντίστοιχα).
Κλινικές μελέτες διάρκειας έως και 2 ετών δεν έδειξαν πρόσθετα σήματα ασφαλείας ή απρόβλεπτους κινδύνους όταν η βιλνταγλιπτίνη συνδυάστηκε με μετφορμίνη.
Συνδυασμός με σουλφονυλουρία
Πίνακας 2 Ανεπιθύμητες ενέργειες που αναφέρθηκαν σε ασθενείς που έλαβαν 50 mg Galvus σε συνδυασμό με σουλφονυλουρία σε διπλές τυφλές μελέτες (N = 170)
Περιγραφή επιλεγμένων ανεπιθύμητων ενεργειών
Σε ελεγχόμενες κλινικές δοκιμές που πραγματοποιήθηκαν με το συνδυασμό βιλνταγλιπτίνης 50 mg + σουλφονυλουρίας, η συνολική συχνότητα απόσυρσης λόγω ανεπιθύμητων ενεργειών ήταν 0,6% στην ομάδα βιλνταγλιπτίνης 50 mg + σουλφονυλουρία έναντι 0% στην ομάδα που έλαβε εικονικό φάρμακο + σουλφονυλουρία.
Σε κλινικές μελέτες, όταν προστέθηκε βιλνταγλιπτίνη 50 mg μία φορά ημερησίως στη γλιμεπιρίδη, η συχνότητα υπογλυκαιμίας ήταν 1,2% έναντι 0,6% με εικονικό φάρμακο + γλιμεπιρίδη. Δεν αναφέρθηκαν σοβαρά υπογλυκαιμικά συμβάντα στους βραχίονες με βιλνταγλιπτίνη.
Σε κλινικές μελέτες, το βάρος δεν άλλαξε από την αρχική τιμή όταν βιλνταγλιπτίνη 50 mg ημερησίως προστέθηκε στη γλιμεπιρίδη (-0,1 κιλά και -0,4 κιλά για τη βιλνταγλιπτίνη και το εικονικό φάρμακο, αντίστοιχα).
Σύνδεση με μια θειαζολιδινοδιόνη
Πίνακας 3 Ανεπιθύμητες ενέργειες που αναφέρθηκαν σε ασθενείς που έλαβαν Galvus 100 mg ημερησίως σε συνδυασμό με θειαζολιδινοδιόνη σε διπλές τυφλές μελέτες (N = 158)
Περιγραφή επιλεγμένων ανεπιθύμητων ενεργειών
Σε ελεγχόμενες κλινικές δοκιμές που πραγματοποιήθηκαν με το συνδυασμό βιλνταγλιπτίνης 100 mg ημερησίως + θειαζολιδινοδιόνης, τόσο στις ομάδες βιλνταγλιπτίνης 100 mg ημερησίως + θειαζολιδινοδιόνη όσο και στις ομάδες εικονικού φαρμάκου + θειαζολιδινοδιόνη, δεν αναφέρθηκαν αναλήψεις λόγω ανεπιθύμητων ενεργειών. Σε κλινικές μελέτες, η συχνότητα υπογλυκαιμίας ήταν σπάνιο σε ασθενείς που έλαβαν βιλνταγλιπτίνη + πιογλιταζόνη (0,6%) ενώ ήταν συχνό σε ασθενείς που έλαβαν εικονικό φάρμακο + πιογλιταζόνη (1,9%). Δεν αναφέρθηκαν σοβαρά υπογλυκαιμικά συμβάντα στα χέρια της βιλνταγλιπτίνης. Στις συμπληρωματικές μελέτες με πιογλιταζόνη, η απόλυτη αύξηση βάρους με εικονικό φάρμακο και Galvus 100 mg ημερησίως ήταν 1,4 και 2,7 κιλά, αντίστοιχα.
Η συχνότητα εμφάνισης περιφερικού οιδήματος όταν προστέθηκε βιλνταγλιπτίνη 100 mg ημερησίως στη βασική θεραπεία με πιογλιταζόνη στη μέγιστη δόση (45 mg άπαξ ημερησίως) ήταν 7,0%, έναντι 2,5% μόνο για πιογλιταζόνη..
Μονοθεραπεία
Πίνακας 4 Ανεπιθύμητες ενέργειες που αναφέρθηκαν σε ασθενείς που έλαβαν Galvus 100 mg ημερησίως ως μονοθεραπεία σε διπλές τυφλές μελέτες (Ν = 1,855)
Περιγραφή επιλεγμένων ανεπιθύμητων ενεργειών
Επιπλέον, σε ελεγχόμενες κλινικές δοκιμές που πραγματοποιήθηκαν με βιλνταγλιπτίνη που χορηγήθηκε μόνη της, η συνολική συχνότητα αποχώρησης λόγω ανεπιθύμητων ενεργειών δεν ήταν υψηλότερη για ασθενείς που έλαβαν βιλνταγλιπτίνη στα 100 mg ημερησίως (0,3%) σε σύγκριση με ασθενείς που έλαβαν εικονικό φάρμακο (0,6%) ή συγκριτικό ( 0,5%).
Σε συγκριτικές ελεγχόμενες μελέτες μονοθεραπείας, η υπογλυκαιμία ήταν ασυνήθιστη και αναφέρθηκε στο 0,4% (7 από 1.855) ασθενών που έλαβαν βιλνταγλιπτίνη στα 100 mg ημερησίως σε σύγκριση με το 0,2% (2 από 1.082) των ασθενών στις ενεργές ομάδες σύγκρισης ή εικονικού φαρμάκου, χωρίς σοβαρά ή σοβαρά γεγονότα που αναφέρθηκαν.
Σε κλινικές μελέτες, το βάρος δεν άλλαξε από την αρχική τιμή όταν χορηγήθηκε βιλνταγλιπτίνη 100 mg ημερησίως ως μονοθεραπεία (-0,3 κιλά και -1,3 κιλά για βιλνταγλιπτίνη και εικονικό φάρμακο, αντίστοιχα). Δεν έδειξε πρόσθετα σήματα ασφαλείας ή απροσδόκητους κινδύνους μόνο με τη βιλνταγλιπτίνη.
Συνδυασμός με μετφορμίνη και σουλφονυλουρία
Πίνακας 5 Ανεπιθύμητες ενέργειες που αναφέρθηκαν σε ασθενείς που έλαβαν Galvus 50 mg δύο φορές την ημέρα σε συνδυασμό με μετφορμίνη και σουλφονυλουρία (N = 157)
Περιγραφή επιλεγμένων ανεπιθύμητων ενεργειών
Δεν υπήρξαν ανακλήσεις λόγω ανεπιθύμητων ενεργειών που αναφέρθηκαν στην ομάδα θεραπείας βιλνταγλιπτίνης + μετφορμίνη + γλιμεπιρίδη σε σύγκριση με 0,6% στην ομάδα θεραπείας με εικονικό φάρμακο + μετφορμίνη + γλιμεπιρίδη.
Η συχνότητα εμφάνισης υπογλυκαιμίας ήταν κοινή και στις δύο ομάδες θεραπείας (5,1% για την ομάδα βιλνταγλιπτίνης + μετφορμίνη + γλιμεπιρίδη έναντι 1,9% για την ομάδα του εικονικού φαρμάκου + μετφορμίνη + γλιμεπιρίδη).
Ένα σοβαρό υπογλυκαιμικό συμβάν αναφέρθηκε στην ομάδα της βιλνταγλιπτίνης.
Στο τέλος της μελέτης, η επίδραση στο μέσο σωματικό βάρος ήταν ουδέτερη (+0,6 kg στην ομάδα βιλνταγλιπτίνης και -0,1 kg στην ομάδα του εικονικού φαρμάκου).
Συσχέτιση με την ινσουλίνη
Πίνακας 6 Ανεπιθύμητες ενέργειες που αναφέρθηκαν σε ασθενείς που έλαβαν Galvus 100 mg ημερησίως σε συνδυασμό με ινσουλίνη (με ή χωρίς μετφορμίνη) σε διπλές τυφλές μελέτες (N = 371)
Περιγραφή επιλεγμένων ανεπιθύμητων ενεργειών
Σε ελεγχόμενες κλινικές δοκιμές με συνδυασμό βιλνταγλιπτίνης 50 mg δύο φορές ημερησίως συν ινσουλίνη, με ή χωρίς ταυτόχρονη μετφορμίνη, η συνολική συχνότητα αποχώρησης λόγω ανεπιθύμητων ενεργειών ήταν 0,3% στην ομάδα θεραπείας με βιλνταγλιπτίνη και δεν υπήρξαν αναλήψεις στην ομάδα του εικονικού φαρμάκου.
Η επίπτωση της υπογλυκαιμίας ήταν παρόμοια και στις δύο ομάδες θεραπείας (14,0% στην ομάδα βιλνταγλιπτίνης έναντι 16,4% στην ομάδα του εικονικού φαρμάκου). Δύο ασθενείς στην ομάδα βιλνταγλιπτίνης και 6 ασθενείς στην ομάδα εικονικού φαρμάκου παρουσίασαν σοβαρά υπογλυκαιμικά συμβάντα.
Στο τέλος της μελέτης, η επίδραση στο μέσο σωματικό βάρος ήταν ουδέτερη (+0,6 κιλά από την αρχική ομάδα της ομάδας βιλνταγλιπτίνης και καμία αλλαγή βάρους στην ομάδα του εικονικού φαρμάκου).
Εμπειρία μετά το μάρκετινγκ
Πίνακας 7 Ανεπιθύμητες ενέργειες μετά την κυκλοφορία
Αναφορά υποψίας ανεπιθύμητων ενεργειών
Η αναφορά ύποπτων ανεπιθύμητων ενεργειών που εμφανίζονται μετά την έγκριση του φαρμακευτικού προϊόντος είναι σημαντική καθώς επιτρέπει τη συνεχή παρακολούθηση της ισορροπίας οφέλους / κινδύνου του φαρμακευτικού προϊόντος. Οι επαγγελματίες υγείας καλούνται να αναφέρουν τυχόν υποψίες ανεπιθύμητων ενεργειών μέσω του εθνικού συστήματος αναφοράς.
04.9 Υπερδοσολογία -
Οι πληροφορίες σχετικά με την υπερδοσολογία με βιλνταγλιπτίνη είναι περιορισμένες.
Συμπτώματα
Πληροφορίες για πιθανά συμπτώματα υπερδοσολογίας προέρχονται από μελέτη ανοχής κλιμάκωσης δόσης σε υγιή άτομα που έλαβαν θεραπεία με Galvus για 10 ημέρες. Στα 400 mg, υπήρξαν τρεις περιπτώσεις μυϊκού πόνου και μεμονωμένες περιπτώσεις ήπιας και παροδικής παραισθησίας, πυρετού, οιδήματος και παροδικής αύξησης των επιπέδων λιπάσης. Στα 600 mg, ένα άτομο ανέπτυξε οίδημα στα πόδια και τα χέρια και αύξησε τα επίπεδα φωσφοκινάσης κρεατίνης (CPK), ασπαρτικής αμινοτρανσφεράσης (AST), δημιουργικής πρωτεΐνης (CRP) και μυοσφαιρίνης. Τρία άλλα άτομα ανέπτυξαν οίδημα στα πόδια, με παραισθησία σε δύο περιπτώσεις. Όλα τα συμπτώματα και οι εργαστηριακές ανωμαλίες υποχώρησαν χωρίς θεραπεία μετά τη διακοπή του φαρμάκου της μελέτης.
Θεραπεία
Σε περίπτωση υπερδοσολογίας, συνιστάται υποστηρικτική θεραπεία. Η βιλνταγλιπτίνη δεν μπορεί να αφαιρεθεί με αιμοκάθαρση. Ωστόσο, ο κύριος μεταβολίτης που προέρχεται από υδρόλυση (LAY 151) μπορεί να αποβληθεί με αιμοκάθαρση.
05.0 ΦΑΡΜΑΚΟΛΟΓΙΚΕΣ ΙΔΙΟΤΗΤΕΣ -
05.1 "Φαρμακοδυναμικές ιδιότητες -
Φαρμακοθεραπευτική ομάδα: Φάρμακα που χρησιμοποιούνται σε διαβήτη, αναστολείς της διπεπτιδυλοπεπτιδάσης 4 (DPP-4), κωδικός ATC: A10BH02
Η βιλνταγλιπτίνη ανήκει στην κατηγορία φαρμάκων που ρυθμίζουν τις παγκρεατικές νησίδες και είναι ένας ισχυρός και εκλεκτικός αναστολέας του DPP-4.
Μηχανισμός δράσης
Η χορήγηση βιλνταγλιπτίνης έχει ως αποτέλεσμα την ταχεία και πλήρη αναστολή της δραστηριότητας του DPP-4, με αποτέλεσμα αυξημένα ενδογενή νηστεία και μεταγευματικά επίπεδα GLP-1 (πεπτίδιο-1 που μοιάζει με γλυκαγόνη) και GIP (ινσουλινοτρόπο πολυπεπτίδιο εξαρτώμενο από τη γλυκόζη).
Φαρμακοδυναμικές επιδράσεις
Αυξάνοντας τα ενδογενή επίπεδα ινκρετίνης, η βιλνταγλιπτίνη αυξάνει την ευαισθησία των β-κυττάρων στη γλυκόζη, με αποτέλεσμα τη βελτίωση της έκκρισης ινσουλίνης που εξαρτάται από τη γλυκόζη. Η θεραπεία με βιλνταγλιπτίνη 50-100 mg ημερησίως σε ασθενείς με διαβήτη τύπου 2 βελτίωσε σημαντικά i σημάδι λειτουργία κυττάρων βήτα, συμπεριλαμβανομένου του HOMA -b (Ομοιοστατική Μοντέλο Αξιολόγηση -β), η αναλογία προϊνσουλίνης προς ινσουλίνη και μέτρα απόκρισης βήτα κυττάρων στη δοκιμή ανοχής γεύματος με συχνή δειγματοληψία. Σε μη διαβητικά άτομα (φυσιολογική γλυκόζη αίματος), η βιλνταγλιπτίνη δεν διεγείρει την έκκριση ινσουλίνης ούτε μειώνει τα επίπεδα γλυκόζης.
Με την αύξηση των ενδογενών επιπέδων GLP-1, η βιλνταγλιπτίνη αυξάνει επίσης την ευαισθησία των κυττάρων άλφα στη γλυκόζη, με αποτέλεσμα την επαρκή έκκριση γλυκαγόνης για ποσότητες γλυκόζης.
Η αύξηση της αναλογίας ινσουλίνης / γλυκαγόνης στην υπεργλυκαιμία που προκαλείται από την αύξηση των επιπέδων ινκρετίνης προκαλεί μείωση της νηστείας και της μεταγευματικής παραγωγής ηπατικής γλυκόζης, με αποτέλεσμα τη μείωση της γλυκόζης στο αίμα.
Η γνωστή επίδραση των αυξημένων επιπέδων GLP-1 που επιβραδύνει τη γαστρική κένωση δεν παρατηρείται στη θεραπεία με βιλνταγλιπτίνη.
Κλινική αποτελεσματικότητα και ασφάλεια
Περισσότεροι από 15.000 ασθενείς με διαβήτη τύπου 2 συμμετείχαν σε διπλά τυφλές κλινικές δοκιμές με εικονικό φάρμακο ή ενεργό έλεγχο με διάρκεια θεραπείας έως και 2 χρόνια. Σε αυτές τις μελέτες, η βιλνταγλιπτίνη χορηγήθηκε σε περισσότερους από 9.000 ασθενείς σε ημερήσιες δόσεις των 50 mg άπαξ ημερησίως, 50 mg δύο φορές ημερησίως ή 100 mg μία φορά ημερησίως. Περισσότεροι από 5.000 άνδρες και περισσότερες από 4.000 γυναίκες ασθενείς έλαβαν βιλνταγλιπτίνη 50 mg άπαξ ημερησίως ή 100 mg ημερησίως. Περισσότεροι από 1.900 ασθενείς που έλαβαν βιλνταγλιπτίνη 50 mg μία φορά ημερησίως ή 100 mg ημερησίως ήταν ηλικίας ≥ 65 ετών. Σε αυτές τις μελέτες, η βιλνταγλιπτίνη χορηγήθηκε ως μονοθεραπεία σε ασθενείς με διαβήτη τύπου 2 ή σε συνδυασμό σε ασθενείς που δεν ελέγχθηκαν επαρκώς με άλλα αντιδιαβητικά φάρμακα προϊόντα.
Συνολικά, η βιλνταγλιπτίνη βελτίωσε τον γλυκαιμικό έλεγχο όταν χορηγείται μόνη της ή όταν χρησιμοποιείται σε συνδυασμό με μετφορμίνη, σουλφονυλουρία και θειαζολιδινοδιόνη, όπως αντικατοπτρίζεται από κλινικά σχετικές μειώσεις της "HbA1c από την έναρξη στοτελικό σημείο μελέτη (βλ. Πίνακα 8).
Σε κλινικές μελέτες, το μέγεθος των μειώσεων της HbA1c με τη βιλνταγλιπτίνη ήταν μεγαλύτερο σε ασθενείς με υψηλότερες τιμές αρχικής HbA1c.
Σε μια διπλά τυφλή ελεγχόμενη μελέτη 52 εβδομάδων, η βιλνταγλιπτίνη (50 mg δύο φορές την ημέρα) μείωσε την αρχική HbA1c κατά -1% σε σύγκριση με -1,6% που επιτεύχθηκε με μετφορμίνη (τιτλοποιήθηκε σε 2 g / ημέρα). Στατιστική μη κατωτερότητα δεν ελήφθη Ασθενείς που έλαβαν βιλνταγλιπτίνη ανέφεραν σημαντικά χαμηλότερα περιστατικά γαστρεντερικών ανεπιθύμητων ενεργειών από αυτά που έλαβαν μετφορμίνη.
Σε μια διπλά τυφλή ελεγχόμενη μελέτη 24 εβδομάδων, η βιλνταγλιπτίνη (50 mg δύο φορές την ημέρα) συγκρίθηκε με τη ροσιγλιταζόνη (8 mg μία φορά την ημέρα). Σε ασθενείς με μέση αρχική τιμή HbA1c 8,7%, οι μέσες μειώσεις ήταν -1,20% με βιλνταγλιπτίνη και -1,48% με ροσιγλιταζόνη. Οι ασθενείς που έλαβαν ροσιγλιταζόνη παρουσίασαν μέση αύξηση βάρους (+1,6 κιλά), ενώ όσοι έλαβαν βιλνταγλιπτίνη δεν παρουσίασαν αύξηση βάρους (-0,3 κιλά). Η συχνότητα εμφάνισης περιφερικού οιδήματος ήταν χαμηλότερη στην ομάδα της βιλνταγλιπτίνης σε σχέση με την ομάδα ροσιγλιταζόνης (2,1% έναντι 4,1%, αντίστοιχα).
Σε μια κλινική μελέτη 2 ετών, η βιλνταγλιπτίνη (50 mg δύο φορές την ημέρα) συγκρίθηκε με τη γλυκλαζίδη (έως 320 mg / ημέρα). Μετά από δύο χρόνια, η μέση μείωση της HbA1c ήταν -0,5% για τη βιλνταγλιπτίνη και -0,6% για τη γλυκαζίδη σε σύγκριση με τη μέση αρχική τιμή HbA1c 8,6%. Η στατιστική μη κατωτερότητα δεν επιτεύχθηκε. Η βιλνταγλιπτίνη συσχετίστηκε με λιγότερα υπογλυκαιμικά συμβάντα (0,7%) από τη γλυκαζίδη (1,7%).
Σε κλινική μελέτη 24 εβδομάδων, η βιλνταγλιπτίνη (50 mg δύο φορές την ημέρα) συγκρίθηκε με την πιογλιταζόνη (30 mg μία φορά ημερησίως) σε ασθενείς που δεν ελέγχθηκαν επαρκώς με μετφορμίνη (μέση ημερήσια δόση: 2020 mg). Σε σύγκριση με την αρχική HbA1c 8,4%, οι μέσες μειώσεις ήταν -0,9% με τη βιλνταγλιπτίνη σε συνδυασμό με μετφορμίνη και -1,0% με πιογλιταζόνη σε συνδυασμό με μετφορμίνη. Σε ασθενείς που έλαβαν πιογλιταζόνη σε συνδυασμό με μετφορμίνη είναι μια μέση αύξηση βάρους +1,9 kg παρατηρήθηκε σε σύγκριση με +0,3 kg που παρατηρήθηκαν σε όσους λάμβαναν βιλνταγλιπτίνη σε συνδυασμό με μετφορμίνη.
Σε κλινική μελέτη 2 ετών, η βιλνταγλιπτίνη (50 mg δύο φορές την ημέρα) συγκρίθηκε με τη γλιμεπιρίδη (έως 6 mg / ημέρα-μέση δόση 2 ετών: 4,6 mg) σε ασθενείς που έλαβαν μετφορμίνη (μέση ημερήσια δόση: 1894 mg). Μετά από 1 χρόνο, οι μέσες μειώσεις της HbA1c ήταν -0,4% με τη βιλνταγλιπτίνη σε συνδυασμό με μετφορμίνη και -0,5% με γλιμεπιρίδη σε συνδυασμό με μετφορμίνη, σε σύγκριση με τη μέση αρχική τιμή HbA1c 7,3%. Η μεταβολή του σωματικού βάρους ήταν -0,2 kg με τη βιλνταγλιπτίνη σε σύγκριση με +1,6 kg με τη γλιμεπιρίδη. Η επίπτωση της υπογλυκαιμίας ήταν σημαντικά χαμηλότερη στην ομάδα της βιλνταγλιπτίνης (1,7%) από ό, τι στην ομάδα της γλιμεπιρίδης (16,2%). Στο τελικό σημείο της μελέτης (2 έτη), και στις δύο ομάδες θεραπείας, βρέθηκε ότι η HbA1c ήταν παρόμοια με τις τιμές της αρχικής διατηρήθηκαν αλλαγές σωματικού βάρους και διαφορές στην υπογλυκαιμία.
Σε μια μελέτη 52 εβδομάδων, η βιλνταγλιπτίνη (50 mg δύο φορές την ημέρα) συγκρίθηκε με τη γλυκλαζίδη (μέση ημερήσια δόση: 229,5 mg) σε ασθενείς που δεν ελέγχθηκαν επαρκώς με μετφορμίνη (αρχική δόση μετφορμίνης 1928 mg / ημέρα). Μετά από 1 χρόνο, οι μέσες μειώσεις της HbA1c ήταν -0,81% με τη βιλνταγλιπτίνη σε συνδυασμό με μετφορμίνη (μέση αρχική τιμή HbA1c 8,4%) και -0,85% με γλυκλαζίδη σε συνδυασμό με μετφορμίνη (μέση αρχική τιμή HbA1c 8,5%)). επιτεύχθηκε στατιστική μη κατωτερότητα (95% CI: -0,11 -0,20). Η μεταβολή του σωματικού βάρους ήταν +0,1 kg με τη βιλνταγλιπτίνη σε σύγκριση με την αύξηση βάρους +1,4 kg με τη γλυκλαζίδη.
Η αποτελεσματικότητα του σταθερού συνδυασμού βιλνταγλιπτίνης και μετφορμίνης (τιτλοποιήθηκε σταδιακά σε δόση 50 mg / 500 mg δύο φορές ημερησίως ή 50 mg / 1000 mg δύο φορές ημερησίως) ως θεραπεία αξιολογήθηκε σε μελέτη 24 εβδομάδων. Αρχική σε ασθενείς που δεν είχαν λάβει προηγουμένως θεραπεία ( denovo).
Η HbA1c μειώθηκε κατά -1,82% με βιλνταγλιπτίνη / μετφορμίνη 50 mg / 1000 mg δύο φορές ημερησίως, κατά -1,61% με βιλνταγλιπτίνη / μετφορμίνη 50 mg / 500 mg δύο φορές την ημέρα, κατά -1, 36% με μετφορμίνη 1000 mg δύο φορές την ημέρα και -1,09 % με βιλνταγλιπτίνη 50 mg δύο φορές την ημέρα ξεκινώντας από τη μέση αρχική τιμή HbA1c 8,6%. ≥10,0% ήταν πιο εμφανής.
Διεξήχθη διπλή-τυφλή, τυχαιοποιημένη, πολυκεντρική, ελεγχόμενη με εικονικό φάρμακο μελέτη για την αξιολόγηση της θεραπευτικής επίδρασης της βιλνταγλιπτίνης 50 mg μία φορά ημερησίως έναντι του εικονικού φαρμάκου σε 515 ασθενείς με διαβήτη τύπου 2 και νεφρική δυσλειτουργία. Μέτρια (N = 294) ή σοβαρό (Ν = 221). Το 68,8% και το 80,5% των ασθενών με μέτρια και σοβαρή νεφρική δυσλειτουργία, αντίστοιχα, είχαν λάβει θεραπεία με ινσουλίνη (μέση ημερήσια δόση 56 μονάδων και 51,6 μονάδες αντίστοιχα) στην αρχή. Σε ασθενείς με μέτρια νεφρική δυσλειτουργία, η βιλνταγλιπτίνη μείωσε σημαντικά την HbA1c σε σύγκριση με το εικονικό φάρμακο (διαφορά -0,53%) από τη μέση αρχική τιμή του 7,9%. Σε ασθενείς με σοβαρή νεφρική δυσλειτουργία, η βιλνταγλιπτίνη έχει μειώσει σημαντικά την HbA1c σε σύγκριση με το εικονικό φάρμακο (διαφορά -0,56% ) ξεκινώντας από μια μέση τιμή βάσης 7,7%.
Μια τυχαιοποιημένη, διπλά τυφλή, ελεγχόμενη με εικονικό φάρμακο μελέτη 24 εβδομάδων διεξήχθη σε 318 ασθενείς για την αξιολόγηση της αποτελεσματικότητας και της ασφάλειας της βιλνταγλιπτίνης (50 mg δύο φορές την ημέρα) σε συνδυασμό με μετφορμίνη (≥1500 mg ημερησίως) και γλιμεπιρίδη (≥4 mg η βιλνταγλιπτίνη σε συνδυασμό με μετφορμίνη και γλιμεπιρίδη μείωσε σημαντικά την HbA1c σε σύγκριση με το εικονικό φάρμακο
Η μέση μείωση της HbA1c που προσαρμόστηκε με εικονικό φάρμακο από τη μέση αρχική τιμή του 8,8% ήταν -0,76%.
Μια τυχαιοποιημένη, διπλά τυφλή, ελεγχόμενη με εικονικό φάρμακο μελέτη 24 εβδομάδων διεξήχθη σε 449 ασθενείς για την αξιολόγηση της αποτελεσματικότητας και της ασφάλειας της βιλνταγλιπτίνης (50 mg δύο φορές την ημέρα) σε συνδυασμό με μια σταθερή δόση βασικής ή προαναμεμειγμένης ινσουλίνης (μέση ημερήσια δόση 41 μονάδες), με ταυτόχρονη χρήση μετφορμίνης (Ν = 276) ή χωρίς ταυτόχρονη μετφορμίνη (Ν = 173). Η βιλνταγλιπτίνη σε συνδυασμό με ινσουλίνη μείωσε σημαντικά την HbA1c σε σύγκριση με το εικονικό φάρμακο. Στον γενικό πληθυσμό, η μέση μείωση του HbA1c που προσαρμόστηκε με εικονικό φάρμακο από τη μέση αρχική τιμή HbA1c κατά 8,8% ήταν -0,72%. Στις υποομάδες που έλαβαν ινσουλίνη με ή χωρίς ταυτόχρονη μετφορμίνη, η μέση μείωση του HbA1c προσαρμοσμένη στο εικονικό φάρμακο ήταν -0,63% και -0,84%, αντίστοιχα. Η συχνότητα εμφάνισης υπογλυκαιμίας στο γενικό πληθυσμό ήταν 8,4% και 7,2% στις ομάδες βιλνταγλιπτίνης και εικονικού φαρμάκου, αντίστοιχα. Οι ασθενείς που έλαβαν βιλνταγλιπτίνη δεν παρουσίασαν αύξηση βάρους (+0,2 κιλά) ενώ οι ασθενείς που έλαβαν εικονικό φάρμακο είχαν εκδηλωθεί μείωση βάρους (-0,7 κιλά).
Σε μια άλλη μελέτη 24 εβδομάδων σε ασθενείς με πιο προχωρημένο διαβήτη τύπου 2 που δεν ελέγχονταν επαρκώς στην ινσουλίνη (σύντομη και μεγαλύτερη διάρκεια δράσης, μέση δόση ινσουλίνης 80 IU / ημέρα) η μέση μείωση της HbA1c όταν η βιλνταγλιπτίνη (50 mg δύο φορές την ημέρα) ήταν προστέθηκε στην ινσουλίνη ήταν στατιστικά και σημαντικά μεγαλύτερη από ό, τι με το εικονικό φάρμακο + ινσουλίνη (0,5% έναντι 0,2%). Η επίπτωση της υπογλυκαιμίας ήταν χαμηλότερη στην ομάδα της βιλνταγλιπτίνης σε σχέση με την ομάδα του εικονικού φαρμάκου (22,9% έναντι 29,6%).
Διεξήχθη πολυκεντρική, τυχαιοποιημένη, διπλά τυφλή μελέτη 52 εβδομάδων σε ασθενείς με διαβήτη τύπου 2 και συμφορητική καρδιακή ανεπάρκεια (NYHA λειτουργική κατηγορία Ι-ΙΙΙ) για την αξιολόγηση της επίδρασης της βιλνταγλιπτίνης 50 mg δύο φορές την ημέρα (N = 128) έναντι του εικονικού φαρμάκου (N = 126) στο κλάσμα εξώθησης της αριστερής κοιλίας (LVEF). Η βιλνταγλιπτίνη δεν σχετίζεται με αλλαγή της λειτουργίας της αριστερής κοιλίας ή επιδείνωση της προϋπάρχουσας CHF. Τα κρίσιμα καρδιαγγειακά συμβάντα ήταν συνολικά ισορροπημένα. Σε ασθενείς με θεραπεία καρδιακής ανεπάρκειας κατηγορίας III NYHA με τη βιλνταγλιπτίνη υπήρχαν περισσότερα καρδιακά συμβάντα από ό, τι σε ασθενείς που έλαβαν εικονικό φάρμακο. Ωστόσο, υπήρξαν προκαταλήψεις στον αρχικό καρδιαγγειακό κίνδυνο υπέρ του εικονικού φαρμάκου και ο αριθμός των συμβάντων ήταν χαμηλός, αποκλείοντας οριστικά συμπεράσματα. Η βιλνταγλιπτίνη μείωσε σημαντικά την HbA1c σε σύγκριση με το εικονικό φάρμακο (διαφορά 0,6 %) από μια τιμή μέση τιμή βάσης 7,8% την εβδομάδα 16. Στην υποομάδα NYHA class III, η μείωση της HbA1c ήταν μικρότερη (διαφορά 0,3%) αλλά αυτό το συμπέρασμα είναι περιορισμένο λόγω του μικρού αριθμού ασθενών (N = 44). Η επίπτωση της υπογλυκαιμίας στο συνολικό πληθυσμό ήταν 4,7% και 5,6% στις ομάδες βιλνταγλιπτίνης και εικονικού φαρμάκου, αντίστοιχα.
Καρδιαγγειακός κίνδυνος
Πραγματοποιήθηκε μετα-ανάλυση 25 κλινικών δοκιμών Φάσης ΙΙΙ διάρκειας άνω των 2 ετών ανεξάρτητων και προοπτικά βραβευμένων καρδιαγγειακών συμβάντων. Αυτή η ανάλυση έδειξε ότι η θεραπεία με βιλνταγλιπτίνη δεν συσχετίστηκε με αυξημένο καρδιαγγειακό κίνδυνο σε σύγκριση με συγκρίσεις. Το σύνθετο τελικό σημείο των αποδεδειγμένων καρδιαγγειακών και εγκεφαλοαγγειακών συμβάντων (οξύ στεφανιαίο σύνδρομο (ACS), παροδικό ισχαιμικό επεισόδιο (με ενδείξεις καρδιακής προσβολής σε απεικόνιση), εγκεφαλικό επεισόδιο ή θάνατος από CCV), ήταν παρόμοιο για τη βιλνταγλιπτίνη σε σύγκριση με το συνδυασμό σύγκρισης ενεργό και εικονικό φάρμακο [Λόγος κινδύνου Mantel-Haenszel 0,84 (διάστημα εμπιστοσύνης 95% 0,63-1,12)]. Συνολικά 99 από τους 8.956 ασθενείς της ομάδας βιλνταγλιπτίνης ανέφεραν ένα συμβάν έναντι 91 από τους 6.061 ασθενείς της ομάδας σύγκρισης.
Πίνακας 8 Βασικά αποτελέσματα αποτελεσματικότητας της βιλνταγλιπτίνης σε ελεγχόμενη με εικονικό φάρμακο μονοθεραπεία και πρόσθετες μελέτες (πρωταρχική αποτελεσματικότητα στον πληθυσμό ITT- πρόθεση να φερθεί)
Παιδιατρικός πληθυσμός
Ο Ευρωπαϊκός Οργανισμός Φαρμάκων έχει παραιτηθεί από την υποχρέωση υποβολής των αποτελεσμάτων των μελετών με τη βιλνταγλιπτίνη σε όλα τα υποσύνολα του παιδιατρικού πληθυσμού με σακχαρώδη διαβήτη τύπου 2 (βλέπε παράγραφο 4.2 για πληροφορίες σχετικά με την παιδιατρική χρήση).
05.2 "Φαρμακοκινητικές ιδιότητες -
Απορρόφηση
Μετά τη χορήγηση από το στόμα σε κατάσταση νηστείας, η βιλνταγλιπτίνη απορροφάται γρήγορα, με τις μέγιστες συγκεντρώσεις στο πλάσμα να εμφανίζονται σε 1,7 ώρες. Τα τρόφιμα καθυστερούν ελαφρώς (2,5 ώρες) το χρόνο για την επίτευξη της μέγιστης συγκέντρωσης στο πλάσμα, αλλά δεν μεταβάλλουν τη συνολική έκθεση (AUC). Η χορήγηση βιλνταγλιπτίνης με τροφή οδηγεί σε μειωμένη Cmax (19%). L Ωστόσο, η έκταση της αλλαγής δεν είναι κλινικά σημαντική, επομένως το Galvus μπορεί να ληφθεί ανεξάρτητα από το φαγητό. Η απόλυτη βιοδιαθεσιμότητα είναι 85%.
Κατανομή
Η δέσμευση της βιλνταγλιπτίνης με τις πρωτεΐνες στο πλάσμα είναι χαμηλή (9,3%) και η βιλνταγλιπτίνη κατανέμεται εξίσου μεταξύ του πλάσματος και των ερυθρών αιμοσφαιρίων. Μετά από ενδοφλέβια χορήγηση, ο μέσος όγκος κατανομής του allo της βιλνταγλιπτίνης σταθερή κατάσταση (Vss) είναι 71 λίτρα, υποδηλώνοντας εξωαγγειακή κατανομή.
Βιομετασχηματισμός
Στους ανθρώπους, ο μεταβολισμός είναι η κύρια οδός αποβολής της βιλνταγλιπτίνης και αντιπροσωπεύει το 69% της δόσης. Ο κύριος μεταβολίτης (LAY 151) είναι φαρμακολογικά ανενεργός και είναι το προϊόν υδρόλυσης της ομάδας κυανό και αντιπροσωπεύει το 57% της δόσης, που ακολουθείται από γλυκουρονίδιο (BQS867) και προϊόντα υδρόλυσης αμιδίου (4% της δόσης). Τα δεδομένα in vitro σε μικροσώματα ανθρώπινων νεφρών υποδηλώνουν ότι ο νεφρός μπορεί να είναι ένας από τους κύριους συντελεστές στην υδρόλυση της βιλνταγλιπτίνης στον κύριο ανενεργό μεταβολίτη της, LAY 151. Το DPP-4 συμβάλλει εν μέρει στην υδρόλυση της βιλνταγλιπτίνης σύμφωνα με μελέτη in vivo διεξήχθη χρησιμοποιώντας αρουραίους χωρίς DPP-4. Η βιλνταγλιπτίνη δεν μεταβολίζεται σε ποσοτικό βαθμό από τα ένζυμα CYP 450. Κατά συνέπεια, η μεταβολική κάθαρση της βιλνταγλιπτίνης δεν αναμένεται να επηρεαστεί από ταυτόχρονη χορήγηση αναστολέων CYP 450 ή / και επαγωγικών φαρμάκων. in vitro έδειξε ότι η βιλνταγλιπτίνη δεν αναστέλλει / επάγει ένζυμα CYP 450. Επομένως, η βιλνταγλιπτίνη δεν είναι πιθανό να επηρεάσει τη μεταβολική κάθαρση φαρμακευτικών προϊόντων που μεταβολίζονται από CYP 1A2, CYP 2C8, CYP 2C9, CYP 2C19, CYP 2D6, CYP 2E1 ή CYP 3A4 όταν χορηγείται ταυτόχρονα.
Εξάλειψη
Μετά τη χορήγηση βιλνταγλιπτίνης [14C] από το στόμα, περίπου το 85% της δόσης απεκκρίνεται στα ούρα και το 15% της δόσης ανακτάται με τα κόπρανα. Μετά από στοματική χορήγηση, η νεφρική απέκκριση της αμετάβλητης βιλνταγλιπτίνης ανέρχεται στο 23% της δόσης. Σε υγιή άτομα, μετά από ενδοφλέβια χορήγηση, εκτελωνισμός οι συνολικές τιμές πλάσματος και νεφρών της βιλνταγλιπτίνης είναι 41 και 13 λίτρα / ώρα, αντίστοιχα. Μετά από ενδοφλέβια χορήγηση, ο μέσος χρόνος ημίσειας ζωής αποβολής είναι περίπου 2 ώρες. Μετά την από του στόματος χορήγηση, ο χρόνος ημίσειας ζωής αποβολής είναι περίπου 3 ώρες.
Γραμμικότητα / Μη γραμμικότητα
Εντός του εύρους της θεραπευτικής δόσης, η Cmax της βιλνταγλιπτίνης και η περιοχή κάτω από την καμπύλη συγκέντρωσης-χρόνου πλάσματος (AUC) αυξάνουν περίπου τη δόση αναλογικά.
Συγκεκριμένες ομάδες ασθενών
Φύλο
Δεν παρατηρήθηκαν κλινικά σημαντικές διαφορές στη φαρμακοκινητική της βιλνταγλιπτίνης μεταξύ υγιών ανδρών και γυναικών σε ένα «ευρύ φάσμα ηλικίας και δείκτη μάζας σώματος (ΔΜΣ). Η αναστολή του DPP-4 από τη βιλνταγλιπτίνη δεν επηρεάζεται».
Ατομα της τρίτης ηλικίας
Σε υγιή ηλικιωμένα άτομα (≥ 70 ετών), η συνολική έκθεση της βιλνταγλιπτίνης (100 mg άπαξ ημερησίως) αυξήθηκε κατά 32%, με αύξηση της μέγιστης συγκέντρωσης στο πλάσμα κατά 18%, σε σύγκριση με υγιή νεαρά άτομα (18 Ωστόσο, αυτές οι αλλαγές δεν λαμβάνονται υπόψη Η αναστολή του DPP-4 από τη βιλνταγλιπτίνη δεν επηρεάζεται από την ηλικία.
Διαταραχή της ηπατικής λειτουργίας
Η επίδραση της ηπατικής δυσλειτουργίας στη φαρμακοκινητική της βιλνταγλιπτίνης μελετήθηκε σε ασθενείς με ήπια, μέτρια και σοβαρή ηπατική δυσλειτουργία, με βάση τη βαθμολογία Child-Pugh (στο εύρος 6 για ήπιο έως 12 για σοβαρό), σε σύγκριση με υγιή άτομα. Σε ασθενείς με ήπια και μέτρια ηπατική δυσλειτουργία, η έκθεση στη βιλνταγλιπτίνη μετά από εφάπαξ δόση μειώνεται (κατά 20%και 8%, αντίστοιχα), ενώ για ασθενείς με σοβαρή ηπατική δυσλειτουργία, η έκθεση στη βιλνταγλιπτίνη αυξάνεται κατά 22%. Η μέγιστη αλλαγή (μείωση ή αύξηση ) στη βιλνταγλιπτίνη η έκθεση είναι ≥30%, η οποία δεν θεωρείται κλινικά σχετική. Δεν υπήρχε συσχέτιση μεταξύ της σοβαρότητας της ηπατικής νόσου και των αλλαγών στην έκθεση στη βιλνταγλιπτίνη.
Διαταραχή της νεφρικής λειτουργίας
Διεξήχθη μια ανοιχτή μελέτη πολλαπλών δόσεων για την αξιολόγηση της φαρμακοκινητικής της χαμηλότερης θεραπευτικής δόσης βιλνταγλιπτίνης (50 mg μία φορά ημερησίως) σε ασθενείς με ποικίλους βαθμούς χρόνιας νεφρικής δυσλειτουργίας που καθορίζεται από την κάθαρση κρεατινίνης (ήπια: 50 έως
Η βιλνταγλιπτίνη απομακρύνθηκε με αιμοκάθαρση σε περιορισμένο βαθμό (3% κατά τη διάρκεια μιας συνεδρίας αιμοκάθαρσης 3-4 ωρών ξεκινώντας 4 ώρες μετά τη χορήγηση).
Εθνικές ομάδες
Περιορισμένα δεδομένα υποδηλώνουν ότι η φυλή δεν έχει σημαντική επίδραση στη φαρμακοκινητική της βιλνταγλιπτίνης.
05.3 Προκλινικά δεδομένα ασφάλειας -
Ενδοκαρδιακές καθυστερήσεις αγωγιμότητας παλμών παρατηρήθηκαν σε σκύλους με δόση μη επίδρασης 15 mg / kg (7 φορές την έκθεση του ανθρώπου βάσει Cmax).
Παρατηρήθηκε συσσώρευση αφρωδών φατνιακών μακροφάγων στους πνεύμονες σε αρουραίους και ποντικούς. Η δόση μη επίδρασης ήταν 25 mg / kg (5 φορές η έκθεση στον άνθρωπο με βάση την AUC) σε αρουραίους και 750 mg / kg (142 φορές την ανθρώπινη έκθεση) σε ποντίκια. Γαστρεντερικά συμπτώματα, ιδιαίτερα μαλακά κόπρανα, βλεννογόνα κόπρανα, διάρροια και, σε υψηλότερες δόσεις, αίμα στα κόπρανα έχουν παρατηρηθεί σε σκύλους. Δεν έχει καθοριστεί επίπεδο μη επίδρασης.
Σε συμβατικές μελέτες γονοτοξικότητας in vitro Και in vivo η βιλνταγλιπτίνη δεν ήταν μεταλλαξιογόνος. Σε αρουραίους, μια μελέτη γονιμότητας και πρώιμης εμβρυϊκής ανάπτυξης δεν έδειξε ότι η βιλνταγλιπτίνη προκαλεί βλάβη στη γονιμότητα, την αναπαραγωγική ικανότητα ή την πρώιμη εμβρυϊκή ανάπτυξη. Η εμβρυϊκή τοξικότητα αξιολογήθηκε σε αρουραίους και κουνέλια. Σε αρουραίους, παρατηρήθηκε αυξημένη συχνότητα αιωρούμενων πλευρών σε συνδυασμό με μείωση των παραμέτρων σωματικού βάρους της μητέρας, με δόση χωρίς αποτέλεσμα 75 mg / kg (10 φορές την έκθεση στον άνθρωπο). Σε κουνέλια, μειωμένο βάρος του εμβρύου και σκελετικές αλλαγές, ενδεικτικά καθυστερήσεις στην ανάπτυξη, παρατηρήθηκαν μόνο παρουσία σοβαρής τοξικότητας από τη μητέρα, με δόση μη επίδρασης 50 mg / kg (9 φορές την έκθεση στον άνθρωπο). Διεξήχθη μελέτη για την προ και μετά τη γέννηση ανάπτυξη σε αρουραίους. μόνο σε συνδυασμό με μητρική τοξικότητα ≥ 150 mg / kg και συμπεριλαμβανομένης παροδικής μείωσης του σωματικού βάρους και μειωμένης κινητικής δραστηριότητας στη γενιά F1.
Διετής μελέτη καρκινογένεσης σε αρουραίους πραγματοποιήθηκε με στοματικές δόσεις έως 900 mg / kg (περίπου 200 φορές την ανθρώπινη έκθεση στη μέγιστη συνιστώμενη δόση). Δεν παρατηρήθηκε αύξηση της συχνότητας όγκων που αποδίδονται στη βιλνταγλιπτίνη. Μια άλλη διετής μελέτη καρκινογένεσης διεξήχθη σε ποντίκια με στοματικές δόσεις έως 1.000 mg / kg. Παρατηρήθηκε αύξηση της συχνότητας εμφάνισης αδενοκαρκινωμάτων μαστού. Αιμαγγειοσάρκωμα, χωρίς δόσεις επίδρασης 500 mg / kg (59 φορές την έκθεση στον άνθρωπο) και 100 mg / kg (16 φορές την έκθεση στον άνθρωπο), αντίστοιχα. Η αυξημένη επίπτωση αυτών των όγκων σε ποντίκια δεν θεωρήθηκε ότι αντιπροσωπεύει σημαντικό κίνδυνο για τον άνθρωπο με βάση την έλλειψη γονιδιοτοξικότητας της βιλνταγλιπτίνης και του κύριου μεταβολίτη της, την ανάπτυξη όγκων σε ένα είδος και όλα. Υψηλή αναλογία συστηματικής έκθεσης στην οποία παρατηρήθηκαν όγκοι Το
Σε μια μελέτη τοξικολογίας 13 εβδομάδων σε πιθήκους cynomolgus έχουν αναφερθεί δερματικές βλάβες σε δόσεις ≥ 5 mg / kg / ημέρα. Οι βλάβες εντοπίζονταν σταθερά στα άκρα (χέρια, πόδια, αυτιά και ουρά). Σε δόση 5 mg / kg / ημέρα (περίπου ισοδύναμη με την ανθρώπινη AUC μετά από έκθεση στη δόση των 100 mg) παρατηρήθηκαν μόνο κυστίδια. Αυτά υποχώρησαν παρά τη συνεχιζόμενη θεραπεία και δεν συσχετίστηκαν με ιστοπαθολογικές ανωμαλίες. Σε δόσεις ≥ 20 mg / kg / ημέρα (περίπου 3 φορές το AUC στους ανθρώπους μετά από έκθεση στη δόση των 100 mg), σημειώθηκε ξεφλούδισμα και ξεφλούδισμα του δέρματος, ψώρα και πληγές ουράς, με σχετικές ιστοπαθολογικές αλλαγές. Νεκρωτικές αλλοιώσεις της ουράς παρατηρήθηκαν σε δόσεις ≥ 80 mg / kg / ημέρα.
Κατά τη διάρκεια μιας περιόδου αποκατάστασης 4 εβδομάδων, οι βλάβες του δέρματος δεν υποχώρησαν σε πιθήκους που έλαβαν 160 mg / kg / ημέρα.
06.0 ΦΑΡΜΑΚΕΥΤΙΚΕΣ ΠΛΗΡΟΦΟΡΙΕΣ -
06.1 Έκδοχα -
Άνυδρη λακτόζη
Μικροκρυσταλλική κυτταρίνη
Γλυκολικό άμυλο νατρίου (τύπος Α)
Στεατικό μαγνήσιο
06.2 ασυμβατότητα "-
Ασχετο.
06.3 Περίοδος ισχύος "-
3 χρόνια
06.4 Ειδικές προφυλάξεις κατά την αποθήκευση -
Φυλάσσετε στην αρχική συσκευασία για προστασία από την υγρασία.
06.5 Φύση της άμεσης συσκευασίας και περιεχόμενο της συσκευασίας -
Φουσκάλα αλουμινίου / αλουμινίου (PA / Al / PVC // Al)
Διατίθεται σε συσκευασίες που περιέχουν 7, 14, 28, 30, 56, 60, 90, 112, 180 ή 336 δισκία και σε πολλαπλές συσκευασίες που περιέχουν 336 (3 συσκευασίες των 112) δισκίων.
Μπορεί να μην κυκλοφορούν όλες οι συσκευασίες.
06.6 Οδηγίες χρήσης και χειρισμού -
Χωρίς ειδικές οδηγίες.
07.0 ΚΑΤΟΧΟΣ ΤΗΣ "ΑΔΕΙΑΣ ΜΑΡΚΕΤΙΝΣΗΣ" -
Novartis Europharm Limited
Frimley Business Park
Camberley GU16 7SR
Ηνωμένο Βασίλειο
08.0 ΑΡΙΘΜΟΣ ΑΔΕΙΑΣ ΜΑΡΚΕΤΙΝΓΚ -
ΕΕ / 1/07/414 / 001-010
ΕΕ/1/07/414/018
038144010
038144022
038144034
038144046
038144059
038144061
038144073
038144085
038144097
038144109
038144186
09.0 ΗΜΕΡΟΜΗΝΙΑ ΠΡΩΤΗΣ ΕΓΚΡΙΣΗΣ OR ΑΝΑΝΕΩΣΗΣ ΤΗΣ ΑΔΕΙΑΣ -
Ημερομηνία πρώτης έγκρισης: 26 Σεπτεμβρίου 2007
Ημερομηνία της πιο πρόσφατης ανανέωσης: 26 Σεπτεμβρίου 2012
10.0 ΗΜΕΡΟΜΗΝΙΑ ΑΝΑΘΕΩΡΗΣΗΣ ΤΟΥ ΚΕΙΜΕΝΟΥ -
D.CCE Απρίλιος 2015