Ενεργά συστατικά: Ulipristal (Ulipristal acetate)
Δισκία Esmya 5 mg
Γιατί χρησιμοποιείται το Esmya; Σε τι χρησιμεύει;
Το Esmya περιέχει τη δραστική ουσία ulipristal acetate. Χρησιμοποιείται για τη θεραπεία μέτριων έως σοβαρών συμπτωμάτων ινομυωμάτων της μήτρας (που ονομάζονται επίσης μυώματα), τα οποία είναι καλοήθεις όγκοι της μήτρας.
Το Esmya χρησιμοποιείται σε ενήλικες γυναίκες (άνω των 18 ετών) που δεν έχουν φτάσει στην εμμηνόπαυση.
Σε ορισμένες γυναίκες, τα ινομυώματα της μήτρας μπορεί να προκαλέσουν έντονη εμμηνόρροια αιμορραγία («έμμηνο ρύση»), πυελικό άλγος (δυσφορία στην κάτω κοιλιακή χώρα) και πίεση σε άλλα όργανα.
Αυτό το φάρμακο λειτουργεί τροποποιώντας τη δραστηριότητα της προγεστερόνης, μιας φυσικής ορμόνης στο σώμα.Χρησιμοποιείται πριν από τη χειρουργική επέμβαση για την αφαίρεση των ινομυωμάτων ή για μακροχρόνια θεραπεία των ινομυωμάτων για τη μείωση του μεγέθους τους, τη διακοπή ή τη μείωση της αιμορραγίας και την αύξηση του επιπέδου των ερυθρών αιμοσφαιρίων.
Αντενδείξεις Όταν το Esmya δεν πρέπει να χρησιμοποιείται
Θα πρέπει να γνωρίζετε ότι οι περισσότερες γυναίκες δεν έχουν εμμηνορροϊκή αιμορραγία (έμμηνο ρύση) κατά τη διάρκεια της θεραπείας και για μερικές εβδομάδες μετά.
Μην πάρετε το Esmya
- εάν είστε αλλεργικοί στην οξική ουλιπριστάλη ή σε οποιοδήποτε άλλο συστατικό του Esmya
- εάν είστε έγκυος ή θηλάζετε.
- εάν έχετε κολπική αιμορραγία που δεν προκαλείται από ινομυώματα της μήτρας.
- εάν έχετε καρκίνο της μήτρας, του τραχήλου της μήτρας, των ωοθηκών ή των μαστών.
Προφυλάξεις κατά τη χρήση Τι πρέπει να γνωρίζετε πριν πάρετε το Esmya
- Εάν παίρνετε ορμονικό αντισυλληπτικό (όπως το χάπι ελέγχου των γεννήσεων) (βλέπε "Άλλα φάρμακα και Esmya"), πρέπει να χρησιμοποιείτε μια αξιόπιστη εναλλακτική μέθοδο αντισύλληψης φραγμού (όπως προφυλακτικό) ενώ παίρνετε το Esmya.
- Εάν έχετε ηπατική ή νεφρική νόσο, ενημερώστε το γιατρό ή το φαρμακοποιό σας πριν πάρετε το Esmya.
- Εάν έχετε σοβαρό άσθμα, το Esmya μπορεί να μην είναι κατάλληλο για εσάς. Συζητήστε αυτό με το γιατρό σας.
Η θεραπεία με Esmya γενικά προκαλεί σημαντική μείωση της εμμηνορροϊκής αιμορραγίας (έμμηνο ρύση) ή μπορεί ακόμη και να τη διακόψει εντός των πρώτων 10 ημερών της θεραπείας. Ωστόσο, εάν συνεχίσετε να έχετε υπερβολική αιμορραγία, ενημερώστε το γιατρό σας.
Η εμμηνόρροια θα επανέλθει συνήθως εντός 4 εβδομάδων από τη λήξη της θεραπείας με Esmya. Η επένδυση της μήτρας μπορεί να πυκνώσει ή να αλλάξει ως αποτέλεσμα της θεραπείας με Esmya. Αυτές οι αλλαγές εξαφανίζονται μετά τη λήξη της θεραπείας και την επαναφορά της εμμήνου ρύσεως.
Παιδιά και έφηβοι
Παιδιά κάτω των 18 ετών δεν πρέπει να παίρνουν το Esmya.
Αλληλεπιδράσεις Ποια φάρμακα ή τρόφιμα μπορούν να αλλάξουν την επίδραση του Esmya
Ενημερώστε το γιατρό ή τον φαρμακοποιό σας εάν παίρνετε, έχετε πάρει πρόσφατα ή μπορεί να πάρετε άλλα φάρμακα.
Εάν παίρνετε κάποιο από τα παρακάτω φάρμακα, ενημερώστε το γιατρό ή το φαρμακοποιό σας, καθώς αυτά τα φάρμακα μπορούν να αλληλεπιδράσουν με το Esmya:
- Ορισμένα φάρμακα που χρησιμοποιούνται για τη θεραπεία καρδιακών προβλημάτων (π.χ. διγοξίνη).
- Ορισμένα φάρμακα που χρησιμοποιούνται για την πρόληψη εγκεφαλικών επεισοδίων και θρόμβων αίματος (π.χ. δαβιγατράνη αιθεξυλική).
- Ορισμένα φάρμακα που χρησιμοποιούνται στη θεραπεία της επιληψίας (π.χ. φαινυτοΐνη, φωσφενυτοΐνη, φαινοβαρβιτάλη, καρβαμαζεπίνη, οξκαρβαζεπίνη, πριμιδόνη).
- Ορισμένα φάρμακα που χρησιμοποιούνται στη θεραπεία της λοίμωξης από HIV (π.χ. ριτοναβίρη, εφαβιρένζη, νεβιραπίνη).
- Φάρμακα που χρησιμοποιούνται για τη θεραπεία ορισμένων βακτηριακών λοιμώξεων (π.χ. ριφαμπικίνη, τελιθρομυκίνη, κλαριθρομυκίνη, ερυθρομυκίνη, ριφαμπουτίνη).
- Ορισμένα φάρμακα που χρησιμοποιούνται στη θεραπεία μυκητιασικών λοιμώξεων (π.χ. κετοκοναζόλη (εκτός από το σαμπουάν), ιτρακοναζόλη).
- Φυτικά φάρμακα που περιέχουν St. John's Wort (Hypericum perforatum), που χρησιμοποιούνται στη θεραπεία της κατάθλιψης ή του άγχους.
- Ορισμένα φάρμακα που χρησιμοποιούνται στη θεραπεία της κατάθλιψης (π.χ. νεφαζοδόνη).
- Ορισμένα φάρμακα που χρησιμοποιούνται στη θεραπεία της υπέρτασης (π.χ. βεραπαμίλη).
Το Esmya είναι πιθανό να μειώσει την αποτελεσματικότητα ορισμένων ορμονικών αντισυλληπτικών. Τα ορμονικά αντισυλληπτικά και τα προγεσταγόνα (π.χ. νορεθινδρόνη ή λεβονοργεστρέλη) είναι επίσης πιθανό να μειώσουν την αποτελεσματικότητα του Esmya. Κατά συνέπεια, δεν συνιστώνται ορμονικά αντισυλληπτικά και πρέπει να χρησιμοποιείτε μια αξιόπιστη εναλλακτική μέθοδο αντισύλληψης φραγμού, όπως προφυλακτικό, κατά τη διάρκεια της θεραπείας με Esmya.
Esmya με φαγητό και ποτό
Θα πρέπει να αποφεύγετε να πίνετε χυμό γκρέιπφρουτ ενώ παίρνετε Esmya.
Προειδοποιήσεις Είναι σημαντικό να γνωρίζετε ότι:
Εγκυμοσύνη και θηλασμός
Μην πάρετε το Esmya εάν είστε έγκυος. Η θεραπεία κατά τη διάρκεια της εγκυμοσύνης μπορεί να επηρεάσει την πορεία της (δεν γνωρίζουμε εάν το Esmya μπορεί να βλάψει το έμβρυο ή να προκαλέσει αποβολή). Εάν μείνετε έγκυος ενώ παίρνετε το Esmya, πρέπει να διακόψετε αμέσως τη λήψη του Esmya και να επικοινωνήσετε με το γιατρό ή το φαρμακοποιό σας.
Το Esmya είναι πιθανό να μειώσει την αποτελεσματικότητα ορισμένων ορμονικών αντισυλληπτικών (βλ. "Άλλα φάρμακα και Esmya"). Η Esmya απεκκρίνεται στο μητρικό γάλα. Επομένως, δεν πρέπει να θηλάζετε ενώ παίρνετε Esmya.
Ζητήστε τη συμβουλή του γιατρού ή του φαρμακοποιού σας πριν πάρετε οποιοδήποτε φάρμακο.
Οδήγηση και χειρισμός μηχανών
Το Esmya μπορεί να προκαλέσει ήπια ζάλη (βλ. Παράγραφο 4 "Πιθανές παρενέργειες"). Εάν εμφανίσετε αυτά τα συμπτώματα, μην οδηγείτε ή χειρίζεστε μηχανές.
Δόση, μέθοδος και χρόνος χορήγησης Πώς να χρησιμοποιήσετε το Esmya: Δοσολογία
Πάντοτε να παίρνετε αυτό το φάρμακο ακριβώς όπως σας έχει πει ο γιατρός σας. Σε περίπτωση αμφιβολίας, συμβουλευτείτε το γιατρό ή το φαρμακοποιό σας.
Η συνιστώμενη δόση είναι ένα δισκίο των 5 mg ημερησίως για κύκλους θεραπείας έως 3 μήνες το καθένα. Εάν σας έχουν συνταγογραφηθεί αρκετά μαθήματα 3μηνης θεραπείας με Esmya, θα πρέπει να ξεκινήσετε κάθε μάθημα το συντομότερο δυνατό κατά τη διάρκεια του δεύτερου εμμηνορροϊκού κύκλου μετά την ολοκλήρωση της προηγούμενης θεραπείας.
Θα πρέπει πάντα να ξεκινάτε να παίρνετε το Esmya την πρώτη εβδομάδα του εμμηνορροϊκού σας κύκλου.
Το δισκίο πρέπει να καταπίνεται με νερό και μπορεί να ληφθεί με ή χωρίς τροφή.
Υπερδοσολογία Τι πρέπει να κάνετε εάν έχετε πάρει πάρα πολύ Esmya
Εάν πάρετε μεγαλύτερη δόση Esmya από την κανονική
Η εμπειρία με τη λήψη αρκετών δόσεων Esmya ταυτόχρονα είναι περιορισμένη. Δεν έχουν αναφερθεί σοβαρές επιβλαβείς επιδράσεις κατά τη ταυτόχρονη λήψη πολλαπλών δόσεων αυτού του φαρμάκου. Ωστόσο, εάν παίρνετε μεγαλύτερη δόση Esmya από την κανονική, συνιστάται να συμβουλευτείτε το γιατρό ή τον φαρμακοποιό σας σχετικά.
Εάν ξεχάσετε να πάρετε το Esmya
Εάν ξεχάσετε μια δόση που έπρεπε να πάρετε πριν από λιγότερες από 12 ώρες, πάρτε τη μόλις το παρατηρήσετε. Εάν έχουν περάσει περισσότερες από 12 ώρες, παραλείψτε τη χαμένη δόση και πάρτε μόνο ένα δισκίο ως συνήθως. Μην πάρετε διπλή δόση για να αναπληρώσετε το δισκίο που ξεχάσατε.
Εάν σταματήσετε να παίρνετε το Esmya
Το Esmya πρέπει να λαμβάνεται καθημερινά κατά τη διάρκεια κύκλων θεραπείας έως και 3 μηνών. Κατά τη διάρκεια κάθε πορείας θεραπείας, μην σταματήσετε να παίρνετε τα δισκία χωρίς τη συμβουλή του γιατρού σας, ακόμη και αν αισθάνεστε καλύτερα, καθώς τα συμπτώματα μπορεί να επιστρέψουν αργότερα.
Εάν έχετε περαιτέρω απορίες σχετικά με τη χρήση αυτού του φαρμάκου, ρωτήστε το γιατρό ή το φαρμακοποιό σας.
Παρενέργειες Ποιες είναι οι παρενέργειες του Esmya
Όπως όλα τα φάρμακα, αυτό το φάρμακο μπορεί να προκαλέσει παρενέργειες, αν και δεν παρουσιάζονται σε όλους τους ανθρώπους.
Πολύ συχνές ανεπιθύμητες ενέργειες (επηρεάζουν περισσότερα από 1 στα 10 άτομα):
- μείωση ή απουσία εμμηνορροϊκής αιμορραγίας (αμηνόρροια)
- πάχυνση του βλεννογόνου της μήτρας (πάχυνση του ενδομητρίου)
Συχνές ανεπιθύμητες ενέργειες (επηρεάζουν έως 1 στα 10 άτομα):
- πονοκέφαλο
- αίσθημα ζάλης (ίλιγγος)
- πόνος στο στομάχι, αίσθημα αδιαθεσίας (ναυτία)
- ακμή
- πόνος στους μυς και τα οστά (μυοσκελετικά)
- σάκος υγρού στις ωοθήκες (κύστη ωοθηκών), ένταση / πόνος στο στήθος, πόνος στην κάτω κοιλιακή χώρα (πυελική)
- εξάψεις
- κούραση (κούραση)
- αύξηση βάρους.
Όχι συχνές ανεπιθύμητες ενέργειες (επηρεάζουν έως 1 στα 100 άτομα):
- ανησυχία
- αλλαγές διάθεσης
- ζάλη
- ξηροστομία, δυσκοιλιότητα
- τριχόπτωση, ξηροδερμία, αυξημένη εφίδρωση
- οσφυαλγία
- απώλεια ούρων
- αιμορραγία της μήτρας (αιμορραγία μήτρας), κολπική έκκριση, μη φυσιολογική κολπική αιμορραγία, δυσφορία στο στήθος
- οίδημα λόγω κατακράτησης νερού (οίδημα)
- υπερβολική κόπωση (ασθένεια)
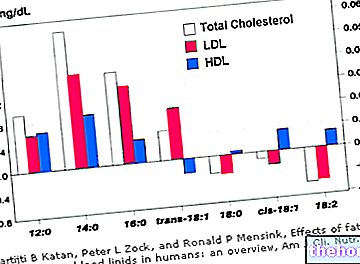
- αύξηση της χοληστερόλης στο αίμα που ανιχνεύεται με εξετάσεις, αύξηση των λιπών στο αίμα (τριγλυκερίδια) που ανιχνεύεται με δοκιμές.
Σπάνιες ανεπιθύμητες ενέργειες (επηρεάζουν έως 1 στα 1.000 άτομα):
- ρινορραγίες
- δυσπεψία, φούσκωμα
- ρήξη υγρού σάκου στις ωοθήκες (ρήξη κύστης ωοθηκών)
- πρήξιμο του στήθους.
Αναφορά παρενεργειών
Εάν παρατηρήσετε κάποια ανεπιθύμητη ενέργεια, ενημερώστε το γιατρό ή το φαρμακοποιό σας. Αυτό περιλαμβάνει τυχόν ανεπιθύμητες ενέργειες που δεν αναφέρονται στο παρόν φύλλο οδηγιών. Μπορείτε επίσης να αναφέρετε ανεπιθύμητες ενέργειες απευθείας μέσω του εθνικού συστήματος αναφοράς που παρατίθεται στο Παράρτημα V. Αναφέροντας ανεπιθύμητες ενέργειες μπορείτε να βοηθήσετε στην παροχή περισσότερων πληροφοριών σχετικά με την ασφάλεια αυτού του φαρμάκου.
Λήξη και διατήρηση
Κρατήστε αυτό το φάρμακο μακριά από τα μάτια και την πρόσβαση των παιδιών.
Μη χρησιμοποιείτε αυτό το φάρμακο μετά την ημερομηνία λήξης που αναφέρεται στο κουτί και στην κυψέλη μετά τη "ΛΗΞΗ". Η ημερομηνία λήξης αναφέρεται στην τελευταία ημέρα του μήνα.
Φυλάξτε την κυψέλη στο εξωτερικό κουτί για να προστατεύσετε το φάρμακο από το φως.
Μην πετάτε φάρμακα μέσω λυμάτων ή οικιακών απορριμμάτων. Ρωτήστε τον φαρμακοποιό σας πώς να πετάξετε φάρμακα που δεν χρησιμοποιείτε πια. Αυτό θα βοηθήσει στην προστασία του περιβάλλοντος.
Τι περιέχει το Esmya
- Το δραστικό συστατικό είναι η οξική ουλιπριστάλη. Ένα δισκίο περιέχει 5 mg οξικής ουλιπριστάλης.
- Τα άλλα συστατικά είναι μικροκρυσταλλική κυτταρίνη, μαννιτόλη, νατριούχος κροσκαρμελλόζη, τάλκης και στεατικό μαγνήσιο.
Περιγραφή της εμφάνισης του Esmya και περιεχόμενο της συσκευασίας
Το Esmya είναι ένα λευκό έως υπόλευκο κυρτό δισκίο 7 mm με χαραγμένο το "ES5" στη μία πλευρά.
Το Esmya διατίθεται σε κυψέλες Al / PVC / PE / PVDC σε κουτιά από χαρτόνι που περιέχουν 28, 30 και 84 δισκία ή σε κυψέλες Al / PVC / PVDC σε κουτιά από χαρτόνι που περιέχουν 28 και 84 δισκία.
Μπορεί να μην κυκλοφορούν όλες οι συσκευασίες.
Φύλλο οδηγιών χρήσης: AIFA (Ιταλικός Οργανισμός Φαρμάκων). Περιεχόμενο που δημοσιεύτηκε τον Ιανουάριο του 2016. Οι πληροφορίες που υπάρχουν δεν μπορεί να είναι ενημερωμένες.
Για να έχετε πρόσβαση στην πιο ενημερωμένη έκδοση, είναι σκόπιμο να αποκτήσετε πρόσβαση στον ιστότοπο AIFA (Ιταλικός Οργανισμός Φαρμάκων). Αποποίηση ευθυνών και χρήσιμες πληροφορίες.
01.0 ΟΝΟΜΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟDΟΝΤΟΣ
ESMYA 5 MG TABLETS
02.0 ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ
Ένα δισκίο περιέχει 5 mg οξικής ουλιπριστάλης.
Για τον πλήρη κατάλογο των εκδόχων, ανατρέξτε στην ενότητα 6.1.
03.0 ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ ΜΟΡΦΗ
Δισκίο.
Στρογγυλό, λευκό έως υπόλευκο, αμφίκυρτο δισκίο 7 mm, με χαραγμένο το "ES5" στη μία πλευρά.
04.0 ΚΛΙΝΙΚΕΣ ΠΛΗΡΟΦΟΡΙΕΣ
04.1 Θεραπευτικές ενδείξεις
Το Ulipristal acetate ενδείκνυται για την προεγχειρητική θεραπεία μέτριων έως σοβαρών συμπτωμάτων ινομυωμάτων της μήτρας σε ενήλικες γυναίκες σε αναπαραγωγική ηλικία.
Το Ulipristal acetate ενδείκνυται για τη διαλείπουσα θεραπεία μέτριων έως σοβαρών συμπτωμάτων ινομυωμάτων της μήτρας σε ενήλικες γυναίκες σε αναπαραγωγική ηλικία.
04.2 Δοσολογία και τρόπος χορήγησης
Δοσολογία
Η θεραπεία αποτελείται από ένα δισκίο των 5 mg που πρέπει να λαμβάνεται από το στόμα μία φορά την ημέρα για κύκλους θεραπείας έως 3 μήνες το καθένα.
Οι θεραπείες πρέπει να ξεκινούν μόνο όταν έχει εμφανιστεί έμμηνος ρύση:
- Η πρώτη πορεία θεραπείας πρέπει να ξεκινήσει κατά την πρώτη εβδομάδα της εμμήνου ρύσεως.
- Τα επόμενα μαθήματα θα πρέπει να ξεκινούν όσο το δυνατόν νωρίτερα κατά την πρώτη εβδομάδα της δεύτερης εμμήνου ρύσεως μετά την ολοκλήρωση του προηγούμενου κύκλου θεραπείας.
Ο θεράπων ιατρός πρέπει να εξηγήσει στον ασθενή ότι πρέπει να τηρούνται τα διαστήματα διακοπής της θεραπείας.
Η διαλείπουσα επαναλαμβανόμενη θεραπεία έχει μελετηθεί για έως και 4 κύκλους διαλείπουσας θεραπείας.
Εάν ένας ασθενής ξεχάσει να πάρει μια δόση, θα πρέπει να λάβει οξική ουλιπριστάλη το συντομότερο δυνατό. Εάν έχουν περάσει περισσότερες από 12 ώρες από τη χαμένη δόση, η ασθενής δεν πρέπει πλέον να παίρνει τη χαμένη δόση, αλλά απλώς να συνεχίσει το συνηθισμένο πρόγραμμα δοσολογίας.
Ειδικοί πληθυσμοί
Νεφρική ανεπάρκεια
Δεν συνιστάται προσαρμογή της δόσης σε ασθενείς με ήπια ή μέτρια νεφρική δυσλειτουργία. Ελλείψει ειδικών μελετών, το ulipristal acetate δεν συνιστάται σε ασθενείς με σοβαρή νεφρική δυσλειτουργία, εκτός εάν ο ασθενής παρακολουθείται στενά (βλ. Παραγράφους 4.4 και 5.2).
Ηπατική ανεπάρκεια
Δεν συνιστάται προσαρμογή της δόσης σε ασθενείς με ήπια ηπατική δυσλειτουργία. Ελλείψει ειδικών μελετών, το ulipristal acetate δεν συνιστάται σε ασθενείς με μέτρια ή σοβαρή ηπατική δυσλειτουργία, εκτός εάν ο ασθενής παρακολουθείται στενά (βλ. Παραγράφους 4.4 και 5.2).
Παιδιατρικός πληθυσμός
Δεν υπάρχει ένδειξη για συγκεκριμένη χρήση του ulipristal acetate στον παιδιατρικό πληθυσμό. Η ασφάλεια και η αποτελεσματικότητα του ulipristal acetate έχουν προσδιοριστεί μόνο σε γυναίκες ηλικίας τουλάχιστον 18 ετών.
Τρόπος χορήγησης
Τα δισκία μπορούν να ληφθούν με ή χωρίς τροφή.
04.3 Αντενδείξεις
Υπερευαισθησία στη δραστική ουσία ή σε κάποιο από τα έκδοχα που αναφέρονται στην παράγραφο 6.1.
Εγκυμοσύνη και θηλασμός.
Κολπική αιμορραγία άγνωστης αιτιολογίας ή για λόγους άλλους από το ινομύωμα της μήτρας.
Καρκίνος της μήτρας, του τραχήλου της μήτρας, των ωοθηκών ή του μαστού.
04.4 Ειδικές προειδοποιήσεις και κατάλληλες προφυλάξεις κατά τη χρήση
Το Ulipristal acetate πρέπει να συνταγογραφείται μόνο μετά από προσεκτική διάγνωση. Πριν από τη θεραπεία είναι απαραίτητο να αποκλειστεί η εγκυμοσύνη. Εκτελέστε ένα τεστ εγκυμοσύνης εάν υπάρχει υποψία εγκυμοσύνης πριν ξεκινήσετε μια νέα πορεία θεραπείας.
Αντισύλληψη
Δεν συνιστάται ταυτόχρονη χρήση ενδομήτριας συσκευής απελευθέρωσης προγεστογόνου, ενδομήτριας συσκευής απελευθέρωσης προγεσταγόνου ή συνδυασμένου αντισυλληπτικού χαπιού (βλ. Παράγραφο 4.5). Παρόλο που η πλειοψηφία των γυναικών που λαμβάνουν θεραπευτική δόση οξικής ουλιπριστάλης παρουσιάζουν αναιμία, κατά τη διάρκεια της θεραπείας συνιστά τη χρήση μη ορμονικής μεθόδου αντισύλληψης.
Ενδομητρικές αλλοιώσεις
Το Ulipristal acetate ασκεί μια συγκεκριμένη φαρμακοδυναμική δράση στο ενδομήτριο:
Αλλαγές στην ιστολογία του ενδομητρίου μπορεί να παρατηρηθούν σε ασθενείς που λαμβάνουν θεραπεία με οξική ουλιπριστάλη. Αυτές οι αλλαγές είναι αναστρέψιμες μετά τη διακοπή της θεραπείας.
Αυτές οι ιστολογικές αλλαγές αναφέρονται ως "ενδομητρικές αλλαγές που σχετίζονται με τον ρυθμιστή του υποδοχέα προγεστερόνης" (PAEC) και δεν πρέπει να συγχέονται με την υπερπλασία του ενδομητρίου (βλέπε παραγράφους 4.8 και 5.1).
Μια αναστρέψιμη αύξηση του πάχους του ενδομητρίου μπορεί επίσης να συμβεί κατά τη διάρκεια της θεραπείας.
Σε περίπτωση επαναλαμβανόμενης διαλείπουσας θεραπείας, συνιστάται περιοδική παρακολούθηση του ενδομητρίου. Αυτό περιλαμβάνει ετήσιο υπερηχογράφημα, το οποίο πρέπει να πραγματοποιείται μετά την επανέναρξη της εμμήνου ρύσεως κατά τη διάρκεια της περιόδου αναστολής της θεραπείας.
Εάν υπάρχει πάχυνση του ενδομητρίου που επιμένει μετά την επανέναρξη της εμμήνου ρύσεως κατά τη διάρκεια των περιόδων διακοπής της θεραπείας ή για περισσότερο από 3 μήνες μετά το τέλος των θεραπευτικών μαθημάτων ή / και παρατηρείται αλλοιωμένο προφίλ αιμορραγίας (βλέπε "προφίλ αιμορραγίας" ") , θα πρέπει να διεξαχθούν έρευνες που περιλαμβάνουν βιοψία ενδομητρίου για να αποκλείσουν άλλες υποκείμενες καταστάσεις, συμπεριλαμβανομένης της κακοήθειας του ενδομητρίου.
Σε περίπτωση υπερπλασίας (χωρίς ατυπία), συνιστάται παρακολούθηση σύμφωνα με τη συνήθη κλινική πρακτική (π.χ. έλεγχος παρακολούθησης μετά από 3 μήνες). Σε περιπτώσεις άτυπης υπερπλασίας, πρέπει να διεξάγονται έρευνες και διαδικασίες που απαιτούνται από τη συνήθη κλινική πρακτική.
Τα μαθήματα θεραπείας δεν πρέπει να υπερβαίνουν τους 3 μήνες το καθένα, καθώς ο κίνδυνος ανεπιθύμητων ενεργειών στο ενδομήτριο εάν συνεχιστεί χωρίς διακοπή της θεραπείας είναι άγνωστος.
Προφίλ αιμορραγίας
Οι ασθενείς πρέπει να ενημερώνονται ότι η θεραπεία με οξική ουλιπριστάλη γενικά οδηγεί σε σημαντική μείωση της εμμηνορροϊκής απώλειας αίματος ή αμηνόρροιας εντός των πρώτων 10 ημερών της θεραπείας. Εάν η υπερβολική αιμορραγία επιμένει, η ασθενής πρέπει να ενημερώσει το γιατρό της. Η εμμηνόρροια θα επανέλθει γενικά μέσα σε 4 εβδομάδες από το τέλος κάθε κύκλου θεραπείας.
Εάν, κατά τη διάρκεια επαναλαμβανόμενης διαλείπουσας θεραπείας, μετά από αρχική μείωση της αιμορραγίας ή αμηνόρροια, ανιχνευθεί επίμονο ή απροσδόκητο τροποποιημένο σχήμα αιμορραγίας, όπως η εμμηνορρυσιακή αιμορραγία, θα πρέπει να διεξαχθούν περαιτέρω έρευνες του ενδομητρίου, συμπεριλαμβανομένης της βιοψίας του ενδομητρίου, για να αποκλειστούν άλλες υποκείμενες καταστάσεις, συμπεριλαμβανομένης της κακοήθειας του ενδομητρίου.
Η διαλείπουσα επαναλαμβανόμενη θεραπεία έχει μελετηθεί για έως και 4 κύκλους διαλείπουσας θεραπείας.
Νεφρική ανεπάρκεια
Η νεφρική ανεπάρκεια δεν αναμένεται να μεταβάλλει σημαντικά την αποβολή της οξικής ουλιπριστάλης. Ελλείψει ειδικών μελετών, το ulipristal acetate δεν συνιστάται σε ασθενείς με σοβαρή νεφρική δυσλειτουργία, εκτός εάν ο ασθενής παρακολουθείται αυστηρά (βλ. Παράγραφο 4.2).
Ηπατική ανεπάρκεια
Δεν υπάρχει θεραπευτική εμπειρία με την οξική ουλιπριστάλη σε ασθενείς με ηπατική ανεπάρκεια. Η ηπατική ανεπάρκεια αναμένεται να μεταβάλλει την αποβολή του ulipristal acetate, με αποτέλεσμα αυξημένη έκθεση (βλ. Παράγραφο 5.2). Αυτή η επίδραση δεν θεωρείται κλινικά σχετική για ασθενείς με ήπια ηπατική δυσλειτουργία. Η χρήση του ulipristal acetate σε ασθενείς με μέτρια ή σοβαρή ηπατική δυσλειτουργία εκτός εάν ο ασθενής παρακολουθείται στενά (βλ. παράγραφο 4.2).
Ταυτόχρονες θεραπείες
Η συγχορήγηση μέτριων (π.χ. ερυθρομυκίνη, χυμός γκρέιπφρουτ, βεραπαμίλη) ή ισχυρών (π.χ. κετοκοναζόλη, ριτοναβίρη, νεφαζοδόνη, ιτρακοναζόλη, τελιθρομυκίνη, κλαριθρομυκίνη) δεν συνιστάται (βλ. Παράγραφο 4.5).
Ταυτόχρονη χρήση οξικής ουλιπριστάλης και ισχυρών επαγωγέων του CYP3A4 (π.χ. ριφαμπικίνη, ριφαμπουτίνη, καρβαμαζεπίνη, οξκαρβαζεπίνη, φαινυτοΐνη, φωσφενυτοΐνη, φαινοβαρβιτάλη, πριμιδόνη, βαλσαμόχορτο, εφαβιρένζη, νεβιραπίνη, μακροχρόνια χρήση του ritonav δεν συνιστάται) ).
Ασθματικοί ασθενείς
Δεν συνιστάται η χρήση σε γυναίκες με σοβαρό άσθμα ανεπαρκώς ελεγχόμενο από του στόματος γλυκοκορτικοειδή.
04.5 Αλληλεπιδράσεις με άλλα φαρμακευτικά προϊόντα και άλλες μορφές αλληλεπίδρασης
Δυνατότητα άλλων φαρμάκων να επηρεάσουν την ολιπριστική οξική:
Ορμονικά αντισυλληπτικά
Το Ulipristal acetate έχει στεροειδή δομή και δρα ως εκλεκτικός ρυθμιστής υποδοχέων προγεστερόνης, με κυρίως ανασταλτικές επιδράσεις στον υποδοχέα προγεστερόνης. Συνεπώς, τα ορμονικά και προγεσταγόνα αντισυλληπτικά είναι πιθανό να μειώσουν την αποτελεσματικότητα του ulipristal acetate λόγω ανταγωνιστικής δράσης στον υποδοχέα προγεστερόνης. Συνεπώς, δεν συνιστάται η ταυτόχρονη χορήγηση φαρμακευτικών προϊόντων που περιέχουν προγεσταγόνο (βλέπε παραγράφους 4.4 και 4.6).
Αναστολείς του CYP3A4
Μετά τη χορήγηση του μέτριου αναστολέα CYP3A4 προπιονικής ερυθρομυκίνης (500 mg δύο φορές ημερησίως για 9 ημέρες) σε υγιείς εθελοντές, η οξική ουλιπρισταλική Cmax και η AUC αυξήθηκαν κατά 1,2 και 2,9 φορές, αντίστοιχα. Του ενεργού μεταβολίτη της οξικής ουλιπριστάλης αυξήθηκε 1,5 φορές, ενώ η Cmax του ενεργού μεταβολίτη μειώθηκε (αλλαγή 0,52 φορές).
Μετά τη χορήγηση του ισχυρού αναστολέα CYP3A4 κετοκοναζόλης (400 mg άπαξ ημερησίως για 7 ημέρες) σε υγιείς εθελοντές, η Cmax και η AUC του οξικού ουλιπριστάλ αυξήθηκαν 2 φορές και 5,9 φορές, αντίστοιχα. Η AUC του ενεργού μεταβολίτη της ολιπρισταλικής οξικής αυξήθηκε 2,4- διπλώθηκε ενώ η Cmax του ενεργού μεταβολίτη μειώθηκε (αλλαγή 0,53 φορές).
Δεν απαιτείται προσαρμογή της δόσης όταν χορηγείται οξική ουλιπριστάλη σε ασθενείς που λαμβάνουν ταυτόχρονα ήπιους αναστολείς του CYP3A4. Δεν συνιστάται ταυτόχρονη χορήγηση μέτριων ή ισχυρών αναστολέων του CYP3A4 και της οξικής ουλιπριστάλης (βλ. Παράγραφο 4.4).
Επαγωγείς CYP3A4
Η χορήγηση του ισχυρού επαγωγέα CYP3A4 ριφαμπικίνης (300 mg δύο φορές ημερησίως για 9 ημέρες) σε υγιείς εθελοντές μείωσε σημαντικά την Cmax και την AUC της οξικής ουλιπριστάλης και του ενεργού μεταβολίτη της κατά 90% ή περισσότερο και μείωσε τον χρόνο ημίσειας ζωής της ουλιπριστάλης. Οξική 2,2 φορές, που αντιστοιχεί σε περίπου 10 φορές μείωση της έκθεσης στην ολιπρισταλική οξική. Ταυτόχρονη χρήση οξικής ουλιπριστάλης και ισχυρών επαγωγέων του CYP3A4 (π.χ. ριφαμπικίνη, ριφαμπουτίνη, καρβαμαζεπίνη, οξκαρβαζεπίνη, φαινυτοΐνη, φωσφενυτοΐνη, φαινοβαρβιτάλη, πριμιδερένη, St. John's w, St. μακροχρόνια χρήση ριτοναβίρης) δεν συνιστάται (βλ. παράγραφο 4.4).
Φαρμακευτικά προϊόντα που επηρεάζουν το γαστρικό pH
Η χορήγηση οξικής ουλιπριστάλης (δισκία 10 mg) σε συνδυασμό με τον αναστολέα της αντλίας πρωτονίων εσομεπραζόλη (20 mg ημερησίως για 6 ημέρες) οδήγησε σε μείωση κατά περίπου 65% στη μέση Cmax, καθυστέρηση στο Tmax (από το μέσο 0,75 ώρες σε 1,0 ώρες) και αύξηση 13% στη μέση τιμή της AUC. Αυτή η επίδραση των φαρμακευτικών προϊόντων που αυξάνουν το γαστρικό pH δεν αναμένεται να είναι κλινικά σχετική με την καθημερινή χορήγηση οξικής ουλιπριστάλης σε δισκία.
Δυνατότητα ολιπριστικής οξικής ουσίας να επηρεάσει άλλα φαρμακευτικά προϊόντα:
Ορμονικά αντισυλληπτικά
Το Ulipristal acetate μπορεί να επηρεάσει τη δράση των ορμονικών αντισυλληπτικών προϊόντων (μόνο προγεσταγόνα, συσκευές απελευθέρωσης προγεσταγόνου ή συνδυασμένα από του στόματος αντισυλληπτικά χάπια) και προγεσταγόνων που χορηγούνται για άλλους λόγους. Συνεπώς, δεν συνιστάται η ταυτόχρονη χορήγηση φαρμακευτικών προϊόντων που περιέχουν προγεσταγόνο (βλ. Παραγράφους 4.4 και 4.6 ) Φαρμακευτικά προϊόντα που περιέχουν προγεσταγόνα δεν πρέπει να λαμβάνονται για 12 ημέρες μετά τη διακοπή της θεραπείας με οξική ουλιπριστάλη.
Υποστρώματα P-gp
Δεδομένα in vitro υποδεικνύουν ότι η οξική ουλιπριστάλη μπορεί να είναι αναστολέας της P-gp σε κλινικά σχετικές συγκεντρώσεις στο γαστρεντερικό τοίχωμα κατά τη διάρκεια της απορρόφησης. Τα αποτελέσματα in vivo δείχνουν ότι η οξική ουλιπριστάλη (χορηγείται ως ένα μόνο δισκίο των 10 mg) 1,5 ώρες πριν από τη χορήγηση του υποστρώματος P-gp φεξοφεναδίνη (60 mg) δεν έχει κλινικά σημαντική επίδραση στη φαρμακοκινητική της φεξοφεναδίνης. Συνεπώς, συνιστάται η συγχορήγηση ολιπρισταλικών οξέων και υποστρωμάτων P-gp (π.χ. δαβιγατράνη αιθεξυλική, διγοξίνη, φεξοφεναδίνη) να απέχει τουλάχιστον 1,5 ώρα.
04.6 Κύηση και γαλουχία
Γυναικεία αντισύλληψη
Το Ulipristal acetate είναι πιθανό να αλληλεπιδρά αρνητικά με χάπια μόνο προγεσταγόνου, συσκευές απελευθέρωσης προγεσταγόνου ή συνδυασμένα από του στόματος αντισυλληπτικά χάπια. Συνεπώς, δεν συνιστάται η ταυτόχρονη χρήση. Παρόλο που η πλειοψηφία των γυναικών που λαμβάνουν θεραπευτική δόση οξικού ουλιπριστάλης παρουσιάζουν ωορρηξία, συνιστάται η χρήση μη ορμονικής μεθόδου αντισύλληψης κατά τη διάρκεια της θεραπείας (βλ. Παραγράφους 4.4 και 4.5).
Εγκυμοσύνη
Το Ulipristal acetate αντενδείκνυται κατά τη διάρκεια της εγκυμοσύνης (βλ. Παράγραφο 4.3).
Δεν υπάρχουν ή υπάρχουν περιορισμένα δεδομένα σχετικά με τη χρήση του ulipristal acetate σε έγκυες γυναίκες.
Παρόλο που δεν βρέθηκε τερατογόνο δυναμικό, τα δεδομένα για τα ζωικά είδη είναι ανεπαρκή για την εκτίμηση της τοξικότητας στην αναπαραγωγή (βλ. Παράγραφο 5.3).
Ωρα ταίσματος
Τα διαθέσιμα τοξικολογικά δεδομένα σε ζώα έδειξαν ότι η οξική ουλιπριστάλη απεκκρίνεται στο γάλα (για λεπτομέρειες βλέπε παράγραφο 5.3). Η οξική ουλιπριστάλη απεκκρίνεται στο ανθρώπινο γάλα. Οι επιδράσεις στα βρέφη δεν έχουν μελετηθεί. Η παρουσία κινδύνων για το νεογέννητο δεν μπορεί να αποκλειστεί. Το Ulipristal acetate αντενδείκνυται κατά τη διάρκεια της γαλουχίας (βλ. Παραγράφους 4.3 και 5.2).
Γονιμότητα
Η πλειοψηφία των γυναικών που λαμβάνουν θεραπευτική δόση οξικής ουλιπριστάλης παρουσιάζουν αφαίρεση του όγκου, ωστόσο, το επίπεδο γονιμότητας ενώ λαμβάνει πολλαπλές δόσεις οξικού ουλιπριστάλης δεν έχει μελετηθεί.
04.7 Επιδράσεις στην ικανότητα οδήγησης και χειρισμού μηχανών
Το Ulipristal acetate μπορεί να επηρεάσει ελαφρά την ικανότητα οδήγησης ή χειρισμού μηχανών, καθώς έχει παρατηρηθεί ήπια ζάλη μετά τη λήψη οξικής ulipristal.
04.8 Ανεπιθύμητες ενέργειες
Περίληψη του προφίλ ασφαλείας
Η ασφάλεια της οξικής ουλιπριστάλης αξιολογήθηκε σε 1.053 γυναίκες με ινομυώματα της μήτρας που έλαβαν θεραπεία με 5 mg ή 10 mg οξικής ουλιπριστάλης κατά τη διάρκεια των μελετών φάσης III. Η πιο συχνή επίδραση σε κλινικές δοκιμές ήταν η αμηνόρροια (79,2%), η οποία θεωρήθηκε επιθυμητό αποτέλεσμα για τους ασθενείς (βλ. Παράγραφο 4.4).
Η πιο συχνή ανεπιθύμητη ενέργεια ήταν η εξάψεις. Η συντριπτική πλειοψηφία των ανεπιθύμητων ενεργειών ήταν ήπιες και μέτριες (95,0%), δεν προκάλεσαν διακοπή του φαρμακευτικού προϊόντος (98,0%) και υποχώρησαν αυθόρμητα.
Σε αυτήν την ομάδα 1.053 γυναικών, η ασφάλεια των επαναλαμβανόμενων διαλείποντων μαθημάτων θεραπείας (το καθένα περιορίζεται σε 3 μήνες) αξιολογήθηκε σε 551 γυναίκες με ινομυώματα της μήτρας που έλαβαν θεραπεία με 5 ή 10 mg οξικού ουλιπριστάλ σε δύο μελέτες φάσης ΙΙΙ (συμπεριλαμβανομένων 457 εκτεθειμένων γυναικών τεσσάρων μαθημάτων) διαλείπουσας θεραπείας), κατά την οποία το φάρμακο παρουσίασε ένα προφίλ ασφάλειας παρόμοιο με αυτό που παρατηρήθηκε μόνο σε μία πορεία θεραπείας.
Πίνακας ανεπιθύμητων ενεργειών
Με βάση τα συγκεντρωτικά δεδομένα από τέσσερις μελέτες φάσης ΙΙΙ σε ασθενείς με ινομυώματα μήτρας που έλαβαν θεραπεία για 3 μήνες, αναφέρθηκαν οι ακόλουθες ανεπιθύμητες ενέργειες. Οι ανεπιθύμητες ενέργειες που αναφέρονται παρακάτω ταξινομούνται ανά συχνότητα και ανά όργανο του συστήματος. Σε κάθε κατηγορία συχνοτήτων, οι ανεπιθύμητες ενέργειες αναφέρονται με σειρά φθίνουσας σοβαρότητας. Οι συχνότητες ορίζονται ως πολύ συχνές (/1 / 10), κοινές (≥1 / 100 έως
* δείτε την ενότητα "Περιγραφή ορισμένων ανεπιθύμητων ενεργειών"
** ο κυριολεκτικός όρος "ήπια τριχόπτωση" έχει κωδικοποιηθεί με τον όρο "αλωπεκία"
Κατά τη σύγκριση επαναλαμβανόμενων μαθημάτων θεραπείας, η συχνότητα των ανεπιθύμητων ενεργειών ήταν συνολικά χαμηλότερη στους επόμενους κύκλους θεραπείας από ό, τι στο πρώτο κύκλο και κάθε ανεπιθύμητη ενέργεια ήταν λιγότερο συχνή ή παρέμεινε στην ίδια κατηγορία συχνότητας (εκτός από τη δυσπεψία που ταξινομήθηκε ως ασυνήθιστη στον κύκλο θεραπείας 3 όπως συνέβη σε έναν ασθενή).
Περιγραφή ορισμένων ανεπιθύμητων ενεργειών
Πάχυνση του ενδομητρίου
Σε 10-15% των ασθενών, παρατηρήθηκε πάχυνση του ενδομητρίου (> 16 mm με υπερηχογράφημα ή μαγνητική τομογραφία στο τέλος της θεραπείας) με ολιπριστική οξική στο τέλος της πρώτης θεραπείας 3 μηνών. Το ενδομήτριο ήταν λιγότερο συχνό ( 4,9% και 3,5% των ασθενών, αντίστοιχα στο τέλος του δεύτερου και του τέταρτου κύκλου θεραπείας) Η πάχυνση του ενδομητρίου εξαφανίζεται όταν σταματήσει η θεραπεία και ξαναρχίσουν οι έμμηνοι κύκλοι.
Επιπλέον, οι αναστρέψιμες αλλοιώσεις του ενδομητρίου ονομάζονται PAEC και διαφέρουν από την υπερπλασία του ενδομητρίου. Κατά την αποστολή δειγμάτων υστερεκτομής ή βιοψίας ενδομητρίου για ιστολογική εξέταση, ο παθολόγος πρέπει να ενημερώνεται ότι ο ασθενής έχει λάβει οξική ουλιπριστάλη (βλ. Παραγράφους 4.4 και 5.1).
Ζεστό εξάπλωση
Αναφέρθηκαν εξάψεις από το 8,1% των ασθενών, αλλά η συχνότητα ήταν διαφορετική από δοκιμή σε δοκιμή. Στην ενεργή συγκριτική ελεγχόμενη μελέτη, τα ποσοστά ήταν 24% (10,5% μέτρια ή σοβαρά) με οξική ουλιπριστάλη και 60,4% (39,6% μέτρια ή σοβαρή ) σε ασθενείς που έλαβαν θεραπεία με λευπρορελίνη. Στη μελέτη που ελεγχόταν με εικονικό φάρμακο, ο ρυθμός εξάψεως ήταν 1,0% για την οξική ουλιπριστάλη και 0% για το εικονικό φάρμακο. Στον πρώτο κύκλο θεραπείας 3 μηνών των δύο μακροχρόνιων δοκιμών Φάσης ΙΙΙ, η συχνότητα ήταν 5,3% και 5,8% με οξική ουλιπριστάλη, αντίστοιχα.
Πονοκέφαλο
Πονοκέφαλος ήπιας ή μέτριας σοβαρότητας αναφέρθηκε από το 5,8% των ασθενών.
Κύστη ωοθηκών
Λειτουργικές κύστεις ωοθηκών παρατηρήθηκαν κατά τη διάρκεια και μετά τη θεραπεία στο 1,0% των ασθενών · στις περισσότερες περιπτώσεις οι κύστεις εξαφανίστηκαν αυθόρμητα μέσα σε λίγες εβδομάδες.
Αιμορραγία μήτρας
Ασθενείς με βαριά εμμηνορροϊκή αιμορραγία λόγω ινομυωμάτων της μήτρας κινδυνεύουν από υπερβολική αιμορραγία, η οποία μπορεί να απαιτήσει χειρουργική επέμβαση. Μερικές περιπτώσεις έχουν αναφερθεί κατά τη διάρκεια της θεραπείας με οξική ουλιπριστάλη και εντός 2-3 μηνών από τη διακοπή της θεραπείας με οξική ουλιπριστάλη.
Αναφορά ύποπτων ανεπιθύμητων ενεργειών
Η αναφορά ύποπτων ανεπιθύμητων ενεργειών που συνέβησαν μετά την έγκριση του φαρμακευτικού προϊόντος είναι σημαντική καθώς επιτρέπει τη συνεχή παρακολούθηση της ισορροπίας οφέλους / κινδύνου του φαρμακευτικού προϊόντος. Οι επαγγελματίες υγείας καλούνται να αναφέρουν τυχόν υποψίες ανεπιθύμητων ενεργειών μέσω του εθνικού συστήματος αναφοράς. Στο "Παράρτημα V Ε
04,9 Υπερδοσολογία
Η εμπειρία με την υπερδοσολογία του ulipristal acetate είναι φτωχή.
Σε περιορισμένο αριθμό ατόμων χορηγήθηκαν εφάπαξ δόσεις του φαρμάκου έως 200 mg και ημερήσιες δόσεις 50 mg για 10 συνεχόμενες ημέρες χωρίς να παρατηρηθούν σοβαρές ή σοβαρές ανεπιθύμητες ενέργειες.
05.0 ΦΑΡΜΑΚΟΛΟΓΙΚΕΣ ΙΔΙΟΤΗΤΕΣ
05.1 Φαρμακοδυναμικές ιδιότητες
Φαρμακοθεραπευτική ομάδα: ορμόνες φύλου και ρυθμιστές του γεννητικού συστήματος, ρυθμιστές υποδοχέων προγεστερόνης.
Κωδικός ATC: G03XB02.
Το Ulipristal acetate είναι ένας από του στόματος ενεργός συνθετικός εκλεκτικός ρυθμιστής υποδοχέα προγεστερόνης που χαρακτηρίζεται από μερική ανταγωνιστική δράση για τον ιστό έναντι της προγεστερόνης.
Ενδομήτριο
Το Ulipristal acetate έχει άμεση επίδραση στο ενδομήτριο. Εάν η καθημερινή χορήγηση δόσης 5 mg ξεκινήσει κατά τη διάρκεια ενός εμμηνορροϊκού κύκλου, τα περισσότερα άτομα (συμπεριλαμβανομένων των ασθενών με μυώμα) θα ολοκληρώσουν την πρώτη τους περίοδο αλλά δεν θα έχουν την επόμενη περίοδο μέχρι το τέλος της θεραπείας Μόλις σταματήσει η θεραπεία με οξική ουλιπριστάλη, οι εμμηνορροϊκοί κύκλοι συνήθως ξαναρχίζουν εντός 4 εβδομάδων.
Η άμεση δράση στο ενδομήτριο προκαλεί συγκεκριμένες ιστολογικές αλλοιώσεις αυτής της κατηγορίας φαρμάκων και καθορισμένου PAEC. Συνήθως, η ιστολογική πλευρά είναι ένα αδρανές και ασθενώς πολλαπλασιαστικό επιθήλιο που σχετίζεται με την ασυμμετρία της στρωματικής και επιθηλιακής ανάπτυξης που παράγει εξέχοντες αδένες με κυστική διαστολή και συνδυασμένα οιστρογόνα ( μιτωτική) και προγεστερόνη (εκκριτική) επιθηλιακή δράση. Αυτό το πρότυπο παρατηρήθηκε σε περίπου 60% των ασθενών που έλαβαν οξική ουλιπριστάλη για 3 μήνες. Αυτές οι αλλαγές είναι αναστρέψιμες μετά τη διακοπή της θεραπείας. Αυτές οι αλλαγές δεν πρέπει να συγχέονται με την υπερπλασία του ενδομητρίου.
Περίπου το 5% των ασθενών στην αναπαραγωγική ηλικία με βαριά έμμηνο ρύση έχουν πάχος ενδομητρίου μεγαλύτερο από 16 mm. Σε περίπου 10-15% των ασθενών που έλαβαν θεραπεία με οξική ουλιπριστάλη, το ενδομήτριο μπορεί να πυκνώσει (> 16 mm) κατά τη διάρκεια της πρώτης θεραπείας 3 μηνών. Σε περίπτωση επαναλαμβανόμενων θεραπευτικών μαθημάτων, η συχνότητα πάχυνσης του ενδομητρίου βρέθηκε να είναι μικρή (4,9 % των ασθενών μετά τη δεύτερη πορεία θεραπείας και 3,5% μετά την τέταρτη πορεία θεραπείας). Η πάχυνση εξαφανίζεται μετά τη διακοπή της θεραπείας και την επανέναρξη της εμμήνου ρύσεως. Σε περίπτωση που η πάχυνση του ενδομητρίου επιμένει μετά την επανέναρξη της εμμήνου ρύσεως κατά τη διάρκεια της περιόδου αναστολής της θεραπείας ή μετά τους 3 μήνες μετά το τέλος των κύκλων θεραπείας, μπορεί να χρειαστεί να διεξαχθούν περαιτέρω έρευνες σύμφωνα με τη συνήθη κλινική πρακτική για να αποκλειστούν άλλες υποκείμενες παθολογίες Το
Ινομυώματα
Το Ulipristal acetate ασκεί άμεση δράση στα ινομυώματα μειώνοντας το μέγεθός τους αναστέλλοντας τον πολλαπλασιασμό των κυττάρων και προκαλώντας απόπτωση.
Βλεννογόνος
Μια ημερήσια δόση 5 mg ulipristal acetate αναστέλλει την ωορρηξία στην πλειοψηφία των ασθενών, όπως υποδεικνύεται από τα σταθερά επίπεδα προγεστερόνης περίπου 0,3 ng / mL.
Η ημερήσια δόση των 5 mg οξικής ουλιπριστάλης καταστέλλει εν μέρει τα επίπεδα της FSH, αλλά τα επίπεδα της οιστραδιόλης στον ορό διατηρούνται στο μεσαίο ωοθυλάκιο στην πλειοψηφία των ασθενών και είναι παρόμοια με τα επίπεδα που βρέθηκαν σε ασθενείς που έλαβαν εικονικό φάρμακο.
Η οξική ουλιπριστάλη δεν επηρεάζει τα επίπεδα TSH, ACTH ή προλακτίνης στον ορό.
Κλινική αποτελεσματικότητα και ασφάλεια
Προεγχειρητική χρήση:
Η αποτελεσματικότητα των σταθερών δόσεων ulipristal acetate 5 mg και 10 mg μία φορά ημερησίως αξιολογήθηκε σε δύο τυχαιοποιημένες, διπλά τυφλές μελέτες Φάσης 3 των 13 εβδομάδων σε ασθενείς με έντονη εμμηνόρροια που σχετίζονται με ινομυώματα της μήτρας. Η μελέτη 1 ήταν διπλά τυφλή, ελεγχόμενη με εικονικό φάρμακο Οι ασθενείς σε αυτήν τη δοκιμή αναμενόταν να είναι αναιμικοί κατά την έναρξη της μελέτης (Hb σιδήρου από το στόμα, 80 mg Fe ++, συν ερευνητικό φάρμακο. Η μελέτη 2 περιελάμβανε έναν ενεργό συγκριτή, λευπρορελίνη 3,75 mg χορηγούμενη μία φορά το μήνα με ενδομυϊκή ένεση. Το εικονικό φάρμακο χρησιμοποιήθηκε για τη διατήρηση της τυφλής Μελέτης 2. Και στις δύο μελέτες, η απώλεια εμμηνορροϊκού αίματος εκτιμήθηκε χρησιμοποιώντας το Διάγραμμα Εικαστικής Αιμορραγίας, PBAC) Μια τιμή PBAC> 100 στις πρώτες 8 ημέρες της εμμήνου ρύσεως θεωρήθηκε ενδεικτική υπερβολικής απώλειας αίματος εμμήνου ρύσεως.
Στη Μελέτη 1, παρατηρήθηκε μια στατιστικά σημαντική διαφορά στη μείωση της εμμηνορροϊκής απώλειας αίματος υπέρ των ασθενών που έλαβαν οξική ουλιπριστάλη σε σύγκριση με το εικονικό φάρμακο (βλ. Πίνακα 1 παρακάτω), η οποία οδήγησε σε πιο γρήγορη και αποτελεσματική διόρθωση της αναιμίας σε σύγκριση με Ομοίως, οι ασθενείς που έλαβαν θεραπεία με οξική ουλιπριστάλη παρουσίασαν μεγαλύτερη μείωση του μεγέθους των μυωμάτων στην μαγνητική τομογραφία.
Στη Μελέτη 2, η μείωση της εμμηνορροϊκής απώλειας αίματος ήταν παρόμοια σε ασθενείς που έλαβαν θεραπεία με οξική ουλιπριστάλη και αγωνιστή της ορμόνης απελευθέρωσης γοναδοτροπίνης (λευπρορελίνη). Οι περισσότεροι ασθενείς που έλαβαν θεραπεία με οξική ουλιπριστάλη σταμάτησαν να χάνουν αίμα κατά την πρώτη εβδομάδα θεραπείας (αμηνόρροια).
Το μέγεθος των τριών μεγαλύτερων μυωμάτων εκτιμήθηκε με υπερηχογράφημα στο τέλος της θεραπείας (Εβδομάδα 13) και για επιπλέον 25 εβδομάδες χωρίς θεραπεία σε ασθενείς που δεν υποβλήθηκαν σε υστερεκτομή ή μυομεκτομή.Η μείωση του μεγέθους των μυωμάτων διατηρήθηκε γενικά κατά τη διάρκεια αυτής της περιόδου παρακολούθησης σε ασθενείς που έλαβαν οξική ουλιπριστάλη, ενώ κάποια αναγέννηση εμφανίστηκε σε ασθενείς που έλαβαν θεραπεία με λευπροπρολίνη.
Πίνακας 1: Αποτελέσματα πρωτογενών αξιολογήσεων αποτελεσματικότητας και ορισμένων δευτερογενών εκτιμήσεων αποτελεσματικότητας σε μελέτες φάσης III
α Στη Μελέτη 1, η μεταβολή από την αρχική τιμή στον συνολικό όγκο μυώματος μετρήθηκε με μαγνητική τομογραφία. Στη Μελέτη 2, η μεταβολή του όγκου των τριών μεγαλύτερων μυωμάτων μετρήθηκε με υπερηχογράφημα. Οι τιμές με έντονα γράμματα στα σκιασμένα πλαίσια υποδεικνύουν μια σημαντική διαφορά στις συγκρίσεις μεταξύ της οξικής ουλιπριστάλης και της μάρτυρας. Αυτές οι διαφορές ήταν πάντα υπέρ του ulipristal acetate.
Ρ-τιμές: 1 =
Διαλείπουσα επαναλαμβανόμενη χρήση:
Η αποτελεσματικότητα των επαναλαμβανόμενων μαθημάτων θεραπείας με σταθερές δόσεις ολιπρισταλικής οξικής 5 mg ή 10 mg άπαξ ημερησίως αξιολογήθηκε σε δύο μελέτες Φάσης 3 που αναλύουν έως και 4 διαλείποντες κύκλους θεραπείας 3 μηνών σε ασθενείς με πολύ βαριά έμμηνο ρύση που σχετίζεται με ινομυώματα της μήτρας. Η μελέτη 3 ήταν μια ανοιχτή μελέτη που αξιολόγησε την οξική ουλιπριστάλη 10 mg, στην οποία κάθε θεραπεία 3 μηνών ακολουθήθηκε από 10 ημέρες διπλής τυφλής θεραπείας με προγεσταγόνο ή εικονικό φάρμακο. Η μελέτη 4 ήταν μια τυχαιοποιημένη κλινική δοκιμή διπλής τυφλής μελέτης που αξιολόγησε την ολιπριστική οξική 5 ή 10 mg
Οι μελέτες 3 και 4 απέδειξαν αποτελεσματικότητα στον έλεγχο των συμπτωμάτων των ινομυωμάτων της μήτρας (π.χ. αιμορραγία της μήτρας) και στη μείωση του μεγέθους του ινομυώματος μετά από 2 και 4 κύκλους θεραπείας.
Στη μελέτη 3, η αποτελεσματικότητα της θεραπείας αποδείχθηκε για περισσότερο από 18 μήνες επαναλαμβανόμενης διαλείπουσας θεραπείας (4 μαθήματα των 10 mg άπαξ ημερησίως). Το 89,7% των ασθενών είχε αμηνόρροια στο τέλος της πορείας της θεραπείας 4.
Στη μελέτη 4, το 61,9% και το 72,7% των ασθενών είχαν αμηνόρροια στο τέλος των κύκλων θεραπείας 1 και 2 σε συνδυασμό (δόση 5 mg και δόση 10 mg, αντίστοιχα, p = 0,032). Το 48,7% και το 60,5% των ασθενών είχαν αμηνόρροια στο τέλος και των τεσσάρων κύκλων θεραπείας (δόση 5 mg και δόση 10 mg, αντίστοιχα, p = 0.027). Στο τέλος του κύκλου θεραπείας 4, 158 άτομα (69,6%) και 164 άτομα (74,5%) είχαν αμηνόρροια με τη δόση των 5 mg και 10 mg, αντίστοιχα (p = 0,290).
Πίνακας 2: Αποτελέσματα πρωτογενών αξιολογήσεων αποτελεσματικότητας και ορισμένες δευτερογενείς αξιολογήσεις αποτελεσματικότητας σε μακροπρόθεσμες μελέτες Φάσης ΙΙΙ
μια αξιολόγηση κύκλου θεραπείας 2 αντιστοιχεί στον κύκλο θεραπείας 2 συν μία εμμηνορροϊκή αιμορραγία.
β Οι ασθενείς για τους οποίους έλειπαν δεδομένα εξαιρέθηκαν από την ανάλυση.
c Ν και% περιλαμβάνουν ασθενείς που έχουν αποσυρθεί
Η ελεγχόμενη αιμορραγία ορίστηκε ως χωρίς επεισόδια βαριάς αιμορραγίας και κατ 'ανώτατο όριο 8 ημερών αιμορραγίας (εξαιρουμένων των ημερών κηλίδωσης) κατά τους δύο τελευταίους μήνες της θεραπείας.
Ενδομητρικά ευρήματα:
Σε όλες τις μελέτες της Φάσης ΙΙΙ, συμπεριλαμβανομένων των περιοδικών επαναλαμβανόμενων θεραπειών, παρατηρήθηκαν συνολικά 7 περιπτώσεις υπερπλασίας σε 789 ασθενείς με επαρκή βιοψία (0,89%). Στη συντριπτική πλειοψηφία των περιπτώσεων, το ενδομήτριο επανήλθε αυθόρμητα στο φυσιολογικό μετά την επανέναρξη της εμμήνου ρύσεως κατά την περίοδο διακοπής της θεραπείας. Η συχνότητα υπερπλασίας δεν αυξήθηκε με επαναλαμβανόμενες θεραπείες. Η παρατηρούμενη συχνότητα αντιστοιχεί σε εκείνη των ομάδων ελέγχου και στον επιπολασμό που αναφέρεται στη βιβλιογραφία για συμπτωματικές προεμμηνοπαυσιακές γυναίκες αυτής της ηλικιακής ομάδας (μέσος όρος 40 ετών).
Ο Ευρωπαϊκός Οργανισμός Φαρμάκων παραιτήθηκε από την υποχρέωση υποβολής των αποτελεσμάτων των μελετών με το Esmya σε όλα τα υποσύνολα του παιδιατρικού πληθυσμού σε ινομυώματα της μήτρας (βλ. Παράγραφο 4.2 για πληροφορίες σχετικά με την παιδιατρική χρήση).
05.2 Φαρμακοκινητικές ιδιότητες
Απορρόφηση
Μετά την από του στόματος χορήγηση μίας μόνο δόσης 5 ή 10 mg, η οξική ουλιπριστάλη απορροφάται ταχέως, με Cmax 23,5 ± 14,2 ng / mL και 50,0 ± 34,4 ng / mL περίπου 1 ώρα μετά την κατάποση 1 "και με AUC0-∞ 61,3 31,7 ng.h / mL και 134,0 ± 83,8 ng.h / mL, αντίστοιχα. Η οξική ουλιπριστάλη μετατρέπεται γρήγορα σε φαρμακολογικά ενεργό μεταβολίτη με Cmax 9,0 ± 4,4 ng / mL και 20,6 ± 10,9 ng / mL, πάλι περίπου 1 ώρα μετά κατάποση, και AUC0-26,0 ± 12,0 ng.h / mL και 63, 6 ± 30,1 ng.h / mL, αντίστοιχα.
Η χορήγηση οξικής ουλιπριστάλης (δισκίο 30 mg) συνοδευόμενη από πρωινό υψηλής περιεκτικότητας σε λιπαρά είχε ως αποτέλεσμα τη μείωση της μέσης Cmax κατά περίπου 45%, καθυστέρηση του Tmax (διάμεσος 0,75 έως 3 ώρες) και αύξηση της μέσης τιμής AUC0-25 κατά 25% σε σύγκριση με τη δοσολογία σε κατάσταση νηστείας. Παρόμοια αποτελέσματα ελήφθησαν για τον ενεργό μονο-Ν-δεσμεθυλο μεταβολίτη. Αυτή η κινητική επίδραση των τροφίμων δεν αναμένεται να είναι κλινικά σχετική στην καθημερινή χορήγηση δισκίων οξικής ουλιπριστάλης.
Κατανομή
Η οξική ουλιπριστάλη συνδέεται ισχυρά (> 98%) με τις πρωτεΐνες του πλάσματος, συμπεριλαμβανομένης της λευκωματίνης, της γλυκοπρωτεΐνης άλφα-1-οξέος, της λιποπρωτεΐνης υψηλής πυκνότητας και της λιποπρωτεΐνης χαμηλής πυκνότητας.
Η οξική ουλιπριστάλη και ο ενεργός μονο-Ν-απομεθυλιωμένος μεταβολίτης της εκκρίνονται στο μητρικό γάλα με αναλογία AUCt γάλακτος / πλάσματος 0,74 ± 0,32 για την οξική ουλιπριστάλη.
Βιομετασχηματισμός / Εξάλειψη
Η οξική ουλιπριστάλη μετατρέπεται ταχέως στους μονο-Ν-απομεθυλιωμένους και στη συνέχεια στους δι-Ν-απομεθυλιωμένους μεταβολίτες της. Τα δεδομένα in vitroυποδεικνύουν ότι αυτή η μετατροπή μεσολαβείται κυρίως από το ισόμορφο κυτόχρωμα P450 3A4 (CYP3A4). Η κύρια οδός αποβολής είναι μέσω των κοπράνων και λιγότερο από το 10% απεκκρίνεται με τα ούρα. Ο εκτιμώμενος τελικός χρόνος ημιζωής της ολιπρισταλικής οξικής στο πλάσμα μετά από μία Η δόση των 5 ή 10 mg εκτιμάται ότι είναι περίπου 38 ώρες, με μέση από του στόματος κάθαρση (CL / F) περίπου 100 L / h.
Τα δεδομένα in vitro υποδεικνύουν ότι η οξική ουλιπριστάλη και ο ενεργός μεταβολίτης της δεν αναστέλλουν τα CYP1A2, 2A6, 2C9, 2C19, 2D6, 2E1 και 3A4, ούτε προκαλούν το CYP1A2 σε κλινικά σχετικές συγκεντρώσεις. Επομένως, η οξική ουλιπριστάλη είναι απίθανο να μεταβάλει την κάθαρση των φαρμακευτικών προϊόντων που μεταβολίζονται από αυτά τα ένζυμα.
Τα δεδομένα in vitro υποδεικνύουν ότι η οξική ουλιπριστάλη και ο ενεργός μεταβολίτης της δεν είναι υποστρώματα της P-gp (ABCB1).
Ειδικοί πληθυσμοί
Φαρμακοκινητικές μελέτες για την οξική ουλιπριστάλη δεν έχουν διεξαχθεί σε γυναίκες με διαταραγμένη νεφρική ή ηπατική λειτουργία. Λόγω του μεταβολισμού που διαμεσολαβείται από το CYP, η ηπατική ανεπάρκεια αναμένεται να μεταβάλλει την αποβολή της οξικής ουλιπριστάλης, με αποτέλεσμα αυξημένη έκθεση (βλέπε παραγράφους 4.2 και 4.4).
05.3 Προκλινικά δεδομένα ασφάλειας
Μη κλινικά δεδομένα δεν αποκαλύπτουν ιδιαίτερο κίνδυνο για τον άνθρωπο με βάση συμβατικές μελέτες φαρμακολογία ασφάλειας, τοξικότητα και γονοτοξικότητα επαναλαμβανόμενων δόσεων.
Τα περισσότερα από τα αποτελέσματα που ελήφθησαν σε γενικές μελέτες τοξικότητας σχετίζονται με δράση σε υποδοχείς προγεστερόνης (και υψηλότερες συγκεντρώσεις σε υποδοχείς γλυκοκορτικοειδών) και έδειξαν δράση αντιπρογεστερόνης σε εκθέσεις παρόμοιες με τα θεραπευτικά επίπεδα. Σε μια μελέτη 39 εβδομάδων σε πιθήκους cynomolgus. σημειώνεται σε χαμηλές δόσεις.
Λόγω του μηχανισμού δράσης του, το ulipristal acetate έχει εμβρυοεθνητική δράση σε αρουραίους, κουνέλια (σε επαναλαμβανόμενες δόσεις άνω του 1 mg / kg), ινδικά χοιρίδια και πιθήκους. Δεν υπάρχουν δεδομένα για την ασφάλεια του ανθρώπινου εμβρύου. Σε δόσεις αρκετά χαμηλές για να διατηρηθεί η κύηση σε είδη ζώων, δεν παρατηρήθηκε τερατογόνο δυναμικό.
Μελέτες αναπαραγωγής που διεξήχθησαν σε αρουραίους σε δόσεις όπως η παραγωγή παρόμοιας με τη δόση που χρησιμοποιήθηκε σε ανθρώπους δεν έδειξαν καμία ένδειξη βλάβης στη γονιμότητα που προκλήθηκε από την οξική ουλιπριστάλη σε ζώα που έλαβαν θεραπεία ή στους απογόνους θηλυκών που έλαβαν θεραπεία.
Μελέτες καρκινογένεσης (σε αρουραίους και ποντικούς) έδειξαν ότι η οξική ουλιπριστάλη δεν είναι καρκινογόνος.
06.0 ΦΑΡΜΑΚΕΥΤΙΚΕΣ ΠΛΗΡΟΦΟΡΙΕΣ
06.1 Έκδοχα
Μικροκρυσταλλική κυτταρίνη
Μαννιτόλη
Νάτριο κροσκαρμελόζη
Τάλκης
Στεατικό μαγνήσιο
06.2 Ασυμβατότητα
Ασχετο.
06.3 Περίοδος ισχύος
3 χρόνια.
06.4 Ειδικές προφυλάξεις κατά την αποθήκευση
Φυλάξτε τις φουσκάλες στο εξωτερικό κουτί για να προστατεύσετε το φάρμακο από το φως.
06.5 Φύση της άμεσης συσκευασίας και περιεχόμενο της συσκευασίας
Κυψέλες Al / PVC / PE / PVDC ή Al / PVC / PVDC.
Συσκευασίες των 28, 30 και 84 δισκίων.
Μπορεί να μην κυκλοφορούν όλες οι συσκευασίες.
06.6 Οδηγίες χρήσης και χειρισμού
Χωρίς ειδικές οδηγίες.
07.0 ΚΑΤΟΧΟΣ ΑΔΕΙΑΣ ΜΑΡΚΕΤΙΝΓΚ
Gedeon Richter Plc.
Gyömroi 19t 19-21.
1103 Βουδαπέστη
Ουγγαρία
08.0 ΑΡΙΘΜΟΣ ΑΔΕΙΑΣ ΜΑΡΚΕΤΙΝΓΚ
ΕΕ/1/12/750/001
042227013
ΕΕ/1/12/750/002
042227025
ΕΕ/1/12/750/003
042227037
ΕΕ/1/12/750/004
042227049
ΕΕ/1/12/750/005
042227052
09.0 ΗΜΕΡΟΜΗΝΙΑ ΠΡΩΤΗΣ ΕΓΚΡΙΣΗΣ OR ΑΝΑΝΕΩΣΗΣ ΤΗΣ ΑΔΕΙΑΣ
Ημερομηνία πρώτης έγκρισης: 23 Φεβρουαρίου 2012
10.0 ΗΜΕΡΟΜΗΝΙΑ ΑΝΑΘΕΩΡΗΣΗΣ ΤΟΥ ΚΕΙΜΕΝΟΥ
D.CCE Μάιος 2015