Ενεργά συστατικά: Κυταραβίνη
Cytarabine Accord 100 mg / ml ενέσιμο διάλυμα ή έγχυση
Γιατί χρησιμοποιείται το Cytarabine - Generic φάρμακο; Σε τι χρησιμεύει;
- Η ενέσιμη κυταραβίνη χρησιμοποιείται σε ενήλικες και παιδιά. Το δραστικό συστατικό είναι η κυταραβίνη.
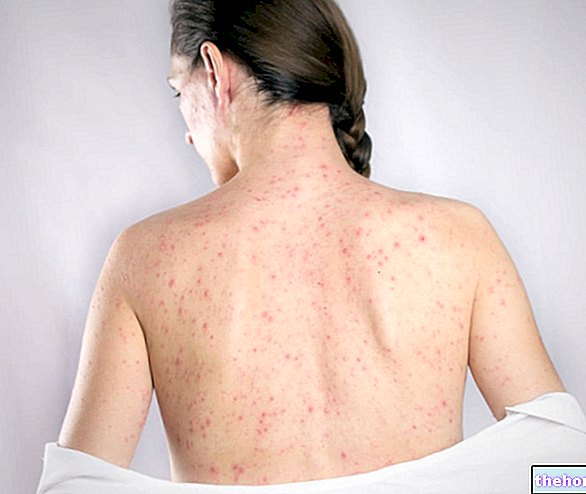
- Η κυταραβίνη ανήκει σε μια ομάδα φαρμάκων που είναι γνωστό ότι είναι κυτταροτοξικά. Αυτά τα φάρμακα χρησιμοποιούνται για τη θεραπεία της οξείας λευχαιμίας (καρκίνος του αίματος, όπου υπάρχουν πάρα πολλά λευκά αιμοσφαίρια στο αίμα). Η κυταραβίνη παρεμβαίνει στην ανάπτυξη καρκινικών κυττάρων, τα οποία τελικά καταστρέφονται.
- Η πρόκληση ύφεσης είναι μια εντατική θεραπεία για να τεθεί η λευχαιμία σε ύφεση. Όταν λειτουργεί, η ισορροπία των κυττάρων στο αίμα γίνεται πιο φυσιολογική, γεγονός που βελτιώνει την υγεία σας. Αυτή η περίοδος σχετικά υγιούς υγείας ονομάζεται «ύφεση».
- Η θεραπεία συντήρησης είναι μια ελαφρύτερη θεραπεία για να διαρκέσει η ύφεση όσο το δυνατόν περισσότερο. Μάλλον χαμηλές δόσεις κυταραβίνης χρησιμοποιούνται για τη διατήρηση της λευχαιμίας υπό έλεγχο και την αποφυγή υποτροπής.
Αντενδείξεις Όταν δεν πρέπει να χρησιμοποιείται το Cytarabine - Γενόσημο φάρμακο
Δεν πρέπει να λαμβάνετε ενέσιμη κυταραβίνη
- Εάν είστε αλλεργικοί (υπερευαίσθητοι) στο citara bine ή σε οποιοδήποτε από τα συστατικά του Cytarabine Injectable.
- Εάν ο αριθμός των κυττάρων του αίματός σας είναι πολύ χαμηλός λόγω άλλων αιτιών εκτός από τον καρκίνο ή απόφαση γιατρού.
- Εάν αισθάνεστε αύξηση των δυσκολιών συντονισμού του σώματος μετά από θεραπεία με ακτινοβολία με άλλα αντικαρκινικά φάρμακα όπως η μεθοτρεξάτη.
Προφυλάξεις κατά τη χρήση Τι πρέπει να γνωρίζετε πριν πάρετε το Cytarabine - Generic φάρμακο
Μιλήστε με το γιατρό, το φαρμακοποιό ή τη νοσοκόμα σας πριν πάρετε το Cytarabine Injectable.
Προσέξτε ιδιαίτερα με τη χορήγηση της ενέσιμης κυταραβίνης:
- Εάν ο μυελός των οστών σας είναι σε κακή κατάσταση, η θεραπεία πρέπει να ξεκινήσει υπό στενή ιατρική παρακολούθηση.
- Εάν έχετε ηπατικά προβλήματα.
- Η κυταραβίνη μειώνει σημαντικά την παραγωγή αιμοσφαιρίων στο μυελό των οστών. Αυτή η μείωση μπορεί να αυξήσει την πιθανότητα να είστε επιρρεπείς σε μόλυνση ή αιμορραγία. Ο αριθμός των κυττάρων του αίματός σας μπορεί να συνεχίσει να μειώνεται έως και μία εβδομάδα μετά τη διακοπή της θεραπείας. Ο γιατρός σας θα κάνει τακτικές εξετάσεις αίματος και θα εξετάσει τον μυελό των οστών σας εάν είναι απαραίτητο.
- Σοβαρές και μερικές φορές απειλητικές για τη ζωή παρενέργειες μπορεί να εμφανιστούν στο κεντρικό νευρικό σύστημα, στο έντερο ή στους πνεύμονες
- Οι λειτουργίες του ήπατος και των νεφρών σας θα πρέπει να παρακολουθούνται κατά τη διάρκεια της θεραπείας με κυταραμπίνη. Εάν το συκώτι σας δεν λειτουργεί καλά πριν από τη θεραπεία, θα σας χορηγηθεί κυταραβίνη μόνο με τη μέγιστη προσοχή.
- Τα επίπεδα ουρικού οξέος (που καταδεικνύουν την καταστροφή των καρκινικών κυττάρων) στο αίμα (υπερουριχαιμία) μπορεί να είναι υψηλά κατά τη διάρκεια της θεραπείας. Ο γιατρός σας θα σας πει εάν πρέπει να πάρετε φάρμακα για τον έλεγχο αυτής της επίδρασης.
- Η χορήγηση ζωντανών ή εξασθενημένων εμβολίων δεν συνιστάται κατά τη διάρκεια της θεραπείας με κυταραβίνη. Εάν απαιτείται, συμβουλευτείτε το γιατρό σας. Η χρήση σκοτωμένων ή αδρανοποιημένων εμβολίων μπορεί να μην έχει το επιθυμητό αποτέλεσμα λόγω της καταστολής του ανοσοποιητικού συστήματος κατά τη διάρκεια της θεραπείας με κυτταραμπίνη.
- Μην ξεχάσετε να ενημερώσετε το γιατρό σας εάν είχατε ακτινοθεραπεία.
Αλληλεπιδράσεις Ποια φάρμακα ή τρόφιμα μπορούν να τροποποιήσουν την επίδραση του Cytarabine - Generic φάρμακο
Ενημερώστε τον γιατρό ή τον φαρμακοποιό σας εάν παίρνετε, έχετε πάρει πρόσφατα ή μπορεί να πάρετε άλλα φάρμακα.
- Φάρμακα που περιέχουν 5-φθοροκυτοσίνη (φάρμακο που χρησιμοποιείται για τη θεραπεία λοιμώξεων που προκαλούνται από μύκητες).
- Λήψη φαρμάκων που περιέχουν διγοτοξίνη ή βήτα-ακετυλ διγοξίνη, τα οποία χρησιμοποιούνται για τη θεραπεία ορισμένων καρδιακών διαταραχών.
- Λήψη γενταμικίνης (αντιβιοτικό που χρησιμοποιείται για τη θεραπεία βακτηριακών λοιμώξεων).
- Φάρμακα που δίνονται που περιέχουν κυκλοφωσφαμίδη, βινκριστίνη και πρεδνιζόνη τα οποία χρησιμοποιούνται σε προγράμματα θεραπείας του καρκίνου.
Προειδοποιήσεις Είναι σημαντικό να γνωρίζετε ότι:
Εγκυμοσύνη, θηλασμός και γονιμότητα
Εγκυμοσύνη
Αποφύγετε να μείνετε έγκυος ενώ εσείς ή ο σύντροφός σας λαμβάνετε θεραπεία με κυταραβίνη. Εάν είστε σεξουαλικά δραστήριοι, είτε άνδρες είτε γυναίκες, σας συνιστάται να χρησιμοποιείτε αποτελεσματική αντισύλληψη για την πρόληψη της εγκυμοσύνης κατά τη διάρκεια της θεραπείας. Η κυταραβίνη μπορεί να προκαλέσει γενετικές ανωμαλίες, επομένως είναι σημαντικό να ενημερώσετε το γιατρό σας εάν νομίζετε ότι είστε έγκυος. Άνδρες και γυναίκες πρέπει να χρησιμοποιούν αποτελεσματικές αντισυλληπτικές μεθόδους κατά τη διάρκεια της θεραπείας και για έως και 6 μήνες μετά τη θεραπεία.
Ωρα ταίσματος
Πρέπει να διακόψετε τον θηλασμό πριν ξεκινήσετε τη θεραπεία με κυταραβίνη, επειδή αυτό το φάρμακο μπορεί να είναι επιβλαβές για βρέφη που θηλάζουν.
Γονιμότητα
Η κυταραβίνη μπορεί να οδηγήσει σε διακοπή του εμμηνορροϊκού κύκλου στις γυναίκες και να οδηγήσει σε αμηνόρροια και μπορεί να καταστέλλει την παραγωγή σπέρματος σε άνδρες ασθενείς. Τα αρσενικά που λαμβάνουν θεραπεία με κυταραβίνη πρέπει να χρησιμοποιούν αξιόπιστη αντισύλληψη.
Ζητήστε τη συμβουλή του γιατρού ή του φαρμακοποιού σας πριν πάρετε οποιοδήποτε φάρμακο.
Οδήγηση και χειρισμός μηχανών
Το Citara bine δεν επηρεάζει την ικανότητα οδήγησης ή χειρισμού μηχανών. Ωστόσο, η θεραπεία του καρκίνου μπορεί συνήθως να επηρεάσει την ικανότητα ορισμένων ασθενών να οδηγούν ή να χειρίζονται μηχανήματα. Εάν επηρεαστείτε, δεν πρέπει να οδηγείτε ή να χειρίζεστε μηχανές.
Δοσολογία και τρόπος χρήσης Τρόπος χρήσης του Cytarabine - Generic φάρμακο: Δοσολογία
Τρόπος και τρόποι χορήγησης
Το Cytarabine θα χορηγηθεί ως έγχυση σε φλέβα (μέσω "στάγδην") ή με ένεση σε φλέβα ή υποδόρια ένεση υπό την καθοδήγηση ειδικών στο νοσοκομείο. Ο γιατρός σας θα αποφασίσει ποια δόση θα σας δώσει και τον αριθμό των ημερών ανάλογα με την κατάστασή του.
Η συνιστώμενη δόση είναι
Με βάση την κατάστασή σας, ο γιατρός σας θα αποφασίσει τη δόση της κυταραβίνης, εάν θα λάβετε θεραπεία επαγωγής ή συντήρησης και την επιφάνεια του σώματός σας. Το βάρος και το ύψος του σώματός σας θα χρησιμοποιηθούν για τον υπολογισμό της επιφάνειάς σας.
Θα χρειαστεί να κάνετε τακτικούς ελέγχους, συμπεριλαμβανομένων εξετάσεων αίματος, κατά τη διάρκεια της θεραπείας σας. Ο γιατρός σας θα σας πει πόσο συχνά θα γίνονται αυτοί οι έλεγχοι. Ο γιατρός θα πραγματοποιεί τακτικούς ελέγχους:
- Αίμα, για έλεγχο για χαμηλό αριθμό κυττάρων αίματος που μπορεί να χρειαστούν θεραπεία. • Το συκώτι, πάλι χρησιμοποιώντας αιματολογικές εξετάσεις, για να ελέγξει ότι η κυταραβίνη δεν επηρεάζει αρνητικά τη λειτουργία του ήπατος.
- Από τα νεφρά, και πάλι χρησιμοποιώντας αιματολογικές εξετάσεις, για να ελέγξετε ότι η κυταραβίνη δεν επηρεάζει αρνητικά τη λειτουργία των νεφρών.
- Επίπεδα ουρικού οξέος στο αίμα. Η κυταραβίνη μπορεί να αυξήσει τα επίπεδα ουρικού οξέος στο αίμα. Ένα άλλο φάρμακο μπορεί να χορηγηθεί εάν τα επίπεδα ουρικού οξέος είναι πολύ υψηλά.
- Εάν είστε σε αιμοκάθαρση, ο γιατρός σας μπορεί να διαφέρει στον χρόνο που παίρνετε το φάρμακο, διότι η αιμοκάθαρση μπορεί να μειώσει την αποτελεσματικότητα του φαρμάκου.
Υπερδοσολογία Τι πρέπει να κάνετε εάν έχετε πάρει υπερδοσολογία Cytarabine - Generic φάρμακο
Οι υψηλές δόσεις μπορούν να επιδεινώσουν τις παρενέργειες, όπως στοματικά έλκη ή να μειώσουν τον αριθμό των λευκών αιμοσφαιρίων και των αιμοπεταλίων (αυτά βοηθούν στο πήγμα του αίματος) στο αίμα. Σε αυτή την περίπτωση, πιθανότατα θα χρειαστεί αντιβιοτικά ή μεταγγίσεις αίματος. Τα στοματικά έλκη μπορούν να αντιμετωπιστούν για να γίνουν λιγότερο ενοχλητικά καθώς επουλώνονται.
Εάν έχετε περαιτέρω απορίες σχετικά με τη χρήση αυτού του φαρμάκου, ρωτήστε το γιατρό ή το φαρμακοποιό σας.
Παρενέργειες Ποιες είναι οι παρενέργειες του Cytarabine - Generic φάρμακο
Όπως όλα τα φάρμακα, έτσι και το Cytarabine Injectable μπορεί να προκαλέσει παρενέργειες, αν και δεν παρουσιάζονται σε όλους τους ανθρώπους.
Οι ανεπιθύμητες ενέργειες της κυταραβίνης εξαρτώνται από τη δόση. Το πεπτικό σύστημα επηρεάζεται συχνότερα, αλλά επηρεάζεται και το αίμα.
Ενημερώστε αμέσως το γιατρό ή τη νοσοκόμα σας που θα σας παρακολουθεί κατά τη διάρκεια αυτής της περιόδου εάν υποφέρετε από τα ακόλουθα συμπτώματα μετά τη λήψη αυτού του φαρμάκου:
- Αλλεργική αντίδραση, όπως «ξαφνική δύσπνοια, δυσκολία στην αναπνοή, πρήξιμο των βλεφάρων, του προσώπου ή των χειλιών, εξάνθημα ή κνησμός (ιδιαίτερα σε ολόκληρο το σώμα).
- Σοβαρή αλλεργική αντίδραση (αναφυλαξία): εξάνθημα που περιλαμβάνει φαγούρα στο κόκκινο δέρμα, πρήξιμο των χεριών, των ποδιών, των αστραγάλων, του προσώπου, των χειλιών ή του λαιμού (που μπορεί να προκαλέσει δυσκολία στην κατάποση ή την αναπνοή), βρογχόσπασμο και αίσθημα λιποθυμίας (αυθόρμητη απώλεια συνείδησης που προκαλείται από ανεπαρκής παροχή αίματος στον εγκέφαλο). Μπορεί να είναι θανατηφόρο (σπάνιο).
- Κλινικά σημεία πνευμονικού οιδήματος / ARDS μπορεί να αναπτυχθούν, ιδιαίτερα σε θεραπεία υψηλής δόσης: έχουν παρατηρηθεί οξείες, ενοχλητικές αναπνευστικές δυσκολίες και νερό στους πνεύμονες (πνευμονικό οίδημα), ιδιαίτερα σε υψηλές δόσεις (συχνές).
- Νιώθει κουρασμένος και νυστάζει.
- Έχει συμπτώματα που μοιάζουν με γρίπη, π.χ. αύξηση της θερμοκρασίας ή πυρετό ή ρίγη.
- Έντονος πόνος στο στήθος.
- Έντονος πόνος στην κοιλιά.
- Απώλεια όρασης, απώλεια αίσθησης αφής, ψυχική διαταραχή ή απώλεια της φυσιολογικής κίνησης (αυτό το φάρμακο μπορεί να προκαλέσει παρενέργειες στον εγκέφαλο και τα μάτια, οι οποίες είναι συνήθως αναστρέψιμες αλλά μπορεί να είναι πολύ σοβαρές).
- Το δέρμα της μελανιάζει πιο εύκολα ή αιμορραγεί περισσότερο από το κανονικό αν πονάει.
Αυτά είναι τα συμπτώματα του χαμηλού αριθμού των κυττάρων του αίματος. Ενημερώστε αμέσως το γιατρό ή τη νοσοκόμα σας εάν έχετε αυτά τα συμπτώματα. Αυτές είναι σοβαρές παρενέργειες. Μάλλον χρειάζεται επείγουσα ιατρική φροντίδα.
Συχνές (επηρεάζουν 1 έως 10 χρήστες στους 100):
- Πυρετός
- Ανεπαρκής αριθμός λευκών και ερυθρών αιμοσφαιρίων ή αιμοπεταλίων στο αίμα, γεγονός που μπορεί να αυξήσει την πιθανότητα να είστε επιρρεπείς σε μόλυνση ή αιμορραγία
- μια πτώση των λευκών αιμοσφαιρίων μπορεί να συνοδεύεται από ρίγη και πυρετό που απαιτούν αμέσως ιατρική αξιολόγηση.
- μια πτώση αιμοπεταλίων μπορεί να συνοδεύεται από αιμορραγία η οποία απαιτεί άμεση ιατρική αξιολόγηση
- Μη φυσιολογικά κύτταρα του αίματος (μεγαλοβλάστωση)
- Απώλεια της όρεξης
- Δυσκολία στην κατάποση
- Πόνος στην κοιλιά (κοιλιακό άλγος)
- Ναυτία (αίσθημα ναυτίας)
- Έκανε ρετσέ
- Διάρροια
- Φλεγμονή ή εξέλκωση του στόματος ή του πρωκτού
- Αναστρέψιμες επιδράσεις στο δέρμα, όπως ερυθρότητα (ερύθημα), φουσκάλες, εξάνθημα, κνίδωση, φλεγμονή των αιμοφόρων αγγείων (αγγειίτιδα), τριχόπτωση
- Αναστρέψιμες επιδράσεις στο ήπαρ, όπως αύξηση των επιπέδων ενζύμων
- Αναστρέψιμες επιπτώσεις στα μάτια, όπως πονόλαιμα με αιμορραγία (αιμορραγική επιπεφυκίτιδα) με μειωμένη όραση, ευαισθησία στο φως (φωτοφοβία), υδαρή ή καύση των ματιών και φλεγμονή του κερατοειδούς (κερατίτιδα)
- Μειωμένη κατάσταση συνείδησης (σε υψηλές δόσεις)
- Δυσκολία στην ομιλία (σε υψηλές δόσεις)
- Μη φυσιολογικές κινήσεις των ματιών (υψηλή δόση νυσταγμού)
- Φλεγμονή της φλέβας στο σημείο της ένεσης
- Μη φυσιολογικά υψηλά επίπεδα ουρικού οξέος στο αίμα (υπερουριχαιμία)
Όχι συχνές (επηρεάζουν 1 έως 10 χρήστες στους 1.000):
- Πονόλαιμος
- Πονοκέφαλο
- Σοβαρές αλλεργικές αντιδράσεις (αναφυλαξία), οι οποίες προκαλούν, για παράδειγμα, δυσκολία στην αναπνοή ή ζάλη
- Δηλητηρίαση αίματος (σήψη)
- Φλεγμονή και έλκη του οισοφάγου
- Σοβαρή φλεγμονή του εντέρου (νεκρωτική κολίτιδα)
- Κύστεις εντέρου
- Έλκος του δέρματος
- Κνησμός • Φλεγμονή στο σημείο της ένεσης • Καφέ / μαύρες κηλίδες στο δέρμα (φακοειδές) • Κιτρίνισμα του δέρματος και των βολβών των ματιών (ίκτερος) • Πνευμονική λοίμωξη (πνευμονία) • Δυσκολίες στην αναπνοή • Παράλυση των ποδιών και του κάτω μέρους του σώματος μπορεί να εμφανιστεί όταν δίνεται κιθάρα στο χώρο που περιβάλλει το νωτιαίο μυελό • Πόνος στους μυς και στις αρθρώσεις • Φλεγμονή του βλεννογόνου που περιβάλλει την καρδιά (περικαρδίτιδα) • Διαταραχή της λειτουργίας των νεφρών • Αδυναμία ούρησης (κατακράτηση ούρων) • Πόνος στο στήθος • Πόνος στο κάψιμο στις παλάμες των χεριών και στα πέλματα τα πόδια
Πολύ σπάνια (επηρεάζει λιγότερους από 1 στους 10.000 χρήστες):
- Φλεγμονή των σιελογόνων αδένων • Ακανόνιστος καρδιακός παλμός (αρρυθμίες)
Άγνωστο (η συχνότητα δεν μπορεί να εκτιμηθεί από τα διαθέσιμα δεδομένα):
- Βλάβη στον νευρικό ιστό (νευρική τοξικότητα) και φλεγμονή ενός ή περισσότερων νεύρων (νευρίτιδα) • Φλεγμονή του παγκρέατος (παγκρεατίτιδα) • Πονόλαιμος οφθαλμός (επιπεφυκίτιδα)
Άλλες παρενέργειες:
Το σύνδρομο Cytarabine μπορεί να εμφανιστεί 6-12 ώρες μετά την έναρξη της θεραπείας. Τα συμπτώματα περιλαμβάνουν:
- Πυρετός
- Πόνος στα οστά και στους μυς
- Περιστασιακός πόνος στο στήθος
- Εξάνθημα
- Πονόλαιμα μάτια (επιπεφυκίτιδα)
- Ναυτία (αίσθημα ναυτίας)
Ο γιατρός σας μπορεί να συνταγογραφήσει κορτικοστεροειδή (αντιφλεγμονώδη φάρμακα) για την πρόληψη ή τη θεραπεία αυτών των συμπτωμάτων. Εάν είναι αποτελεσματικά, η θεραπεία με citara bine μπορεί να συνεχιστεί.
Αντιδράσεις που παρατηρήθηκαν με θεραπεία υψηλότερης δόσης
Κεντρικό νευρικό σύστημα:
Τα ακόλουθα συμπτώματα, τα οποία είναι συνήθως αναστρέψιμα, μπορεί να εμφανιστούν στο ένα τρίτο των ασθενών μετά από θεραπεία με υψηλές δόσεις κυταραμπίνης:
- Αλλάζει η προσωπικότητα
- Διαταραγμένη διαύγεια
- Δυσκολία στην ομιλία
- Προβλήματα με τον συντονισμό
- Τρόμος
- Μη φυσιολογικές κινήσεις των ματιών (νυσταγμός)
- Πονοκέφαλο
- Περιφερικές κινητικές και αισθητηριακές νευροπάθειες (βλάβη στα νεύρα του περιφερικού νευρικού συστήματος)
- Σύγχυση
- Υπνηλία
- Ζάλη
- Κώμα
- Σπασμοί
Αυτές οι ανεπιθύμητες ενέργειες μπορεί να εμφανιστούν συχνότερα:
- σε ηλικιωμένους ασθενείς (> 55 ετών)
- σε ασθενείς με μειωμένη ηπατική και νεφρική λειτουργία
- μετά από προηγούμενη θεραπεία για καρκίνο του εγκεφάλου και του νωτιαίου μυελού, όπως ακτινοθεραπεία ή ένεση κυτταροστατικών
- με κατάχρηση αλκοόλ
Ο κίνδυνος βλάβης των νεύρων αυξάνεται εάν η θεραπεία με κυτταραμπίνη:
- χορηγείται σε υψηλές δόσεις ή σε σύντομα διαστήματα
- συνδυάζεται με άλλες θεραπείες που είναι τοξικές για το νευρικό σύστημα (όπως ακτινοθεραπεία ή μεθοτρεξάτη)
Πεπτικό σύστημα:
Ιδιαίτερα στη θεραπεία με υψηλές δόσεις κυταραβίνης, ενδέχεται να προκύψουν πιο σοβαρές αντιδράσεις εκτός από τα κοινά συμπτώματα. Έχουν αναφερθεί διάτρηση, θάνατος ιστού (νέκρωση) και απόφραξη του εντέρου και φλεγμονή της εσωτερικής επένδυσης της κοιλιάς. Έχουν παρατηρηθεί αποστήματα στο ήπαρ, διεύρυνση του ήπατος, απόφραξη των φλεβών του ήπατος και φλεγμονή του παγκρέατος μετά από θεραπεία με υψηλές δόσεις.
Οι ανεπιθύμητες ενέργειες στο πεπτικό σύστημα είναι μικρές εάν το citara bine χορηγείται με έγχυση.
Πνεύμονες:
Έχουν παρατηρηθεί οξείες ενοχλητικές αναπνευστικές δυσκολίες και νερό στους πνεύμονες (πνευμονικό οίδημα), ιδιαίτερα σε υψηλές δόσεις.
Οι υπολοιποι:
- Καρδιοπάθεια (μυοκαρδιοπάθεια)
- Μη φυσιολογική διάσπαση των μυϊκών κυττάρων (ραβδομυόλυση)
- Μόλυνση αίματος (σήψη)
- Τοξικότητα στον κερατοειδή
- Ιογενείς, βακτηριακές λοιμώξεις κ.λπ.
- Απώλεια σπέρματος και έμμηνος ρύση
Εάν παρατηρήσετε κάποια ανεπιθύμητη ενέργεια, ενημερώστε το γιατρό ή το φαρμακοποιό σας. Αυτό περιλαμβάνει τυχόν ανεπιθύμητες ενέργειες που δεν αναφέρονται στο παρόν φύλλο οδηγιών.
Αναφορά παρενεργειών
Εάν παρατηρήσετε κάποια ανεπιθύμητη ενέργεια, ενημερώστε τον γιατρό, τον φαρμακοποιό ή τον νοσοκόμο σας. Αυτό περιλαμβάνει τυχόν ανεπιθύμητες ενέργειες που δεν αναφέρονται στο παρόν φύλλο οδηγιών χρήσης. Μπορείτε επίσης να αναφέρετε ανεπιθύμητες ενέργειες απευθείας μέσω του εθνικού συστήματος αναφοράς: www.agenziafarmaco.it Αναφέροντας ανεπιθύμητες ενέργειες μπορείτε να βοηθήσετε στην παροχή περισσότερων πληροφοριών σχετικά με την ασφάλεια αυτού του φαρμάκου.
Λήξη και διατήρηση
Να φυλάσσεται σε μέρη που δεν το βλέπουν και δεν το φθάνουν τα παιδιά.
Μην φυλάσσετε σε θερμοκρασία μεγαλύτερη των 25 ° C.
Μην ψύχετε ή παγώνετε.
Μη χρησιμοποιείτε το Cytarabine Injectable μετά την ημερομηνία λήξης που αναφέρεται στο φιαλίδιο ή στο κουτί (mm / yy).
Η ημερομηνία λήξης αναφέρεται στην τελευταία ημέρα του μήνα.
Σταθερότητα κατά τη χρήση:
Χημική-φυσική σταθερότητα κατά τη χρήση έχει αποδειχθεί σε ενέσιμο διάλυμα χλωριούχου νατρίου (0,9% β / ο) και ενέσιμο διάλυμα δεξτρόζης (5% β / ο) για έως και 24 ώρες σε θερμοκρασία κάτω των 25 ° C και έως 72 ώρες σε θερμοκρασία 2 έως 8 ° C.
Από μικροβιολογική άποψη, το προϊόν πρέπει να χρησιμοποιείται αμέσως. Εάν δεν χρησιμοποιηθεί αμέσως, οι χρόνοι και οι συνθήκες αποθήκευσης πριν από τη χρήση είναι ευθύνη του χρήστη και κανονικά δεν θα υπερβαίνουν τις 24 ώρες στους 2-8 ° C, εκτός εάν η αραίωση έχει πραγματοποιηθεί υπό ελεγχόμενες και επικυρωμένες άσηπτες συνθήκες.
Μη χρησιμοποιείτε το Cytarabine Injectable εάν παρατηρήσετε ότι το διάλυμα δεν είναι διαυγές, άχρωμο και χωρίς σωματίδια.
Μην πετάτε φάρμακα μέσω λυμάτων ή οικιακών απορριμμάτων. Ρωτήστε τον φαρμακοποιό σας πώς να πετάξετε φάρμακα που δεν χρησιμοποιείτε πια. Αυτό θα βοηθήσει στην προστασία του περιβάλλοντος.
Αλλες πληροφορίες
Τι περιέχει το Cytarabine Injectable
Η ενέσιμη κυταραβίνη περιέχει τη δραστική ουσία κυταραβίνη.
1 ml περιέχει 100 mg κυταραβίνη.
- Κάθε φιαλίδιο 1 ml περιέχει 100 mg κυταραβίνη.
- Κάθε φιαλίδιο των 5 ml περιέχει 500 mg κυταραβίνης.
- Κάθε φιαλίδιο των 10 ml περιέχει 1 g κυταραβίνης.
- Κάθε φιαλίδιο των 20 ml περιέχει 2 g κυταραβίνης.
- Κάθε φιαλίδιο των 40 ml περιέχει 4 g κυταραβίνης.
- Κάθε φιαλίδιο των 50 ml περιέχει 5 g κυταραβίνης.
Τα άλλα συστατικά είναι μακρογόλη 400, τρομεταμόλη και ενέσιμο νερό.
Εμφάνιση του Cytarabine Injectable και περιεχόμενο της συσκευασίας
Το Cytarabine Injectable είναι ένα διαυγές και άχρωμο ενέσιμο διάλυμα ή έγχυση.
- 1 ml
Το ενέσιμο διάλυμα περιέχεται σε ένα φιαλίδιο διαυγούς γυαλιού τύπου I των 2 ml κλειστό με γκρι ελαστικό πώμα 13 mm και αποσπώμενη στεγανοποίηση αλουμινίου από διαφανές μπλε ή γαλάζιο μπλε χρώμα.
- 5 ml
Το ενέσιμο διάλυμα περιέχεται σε διαυγές σωληνωτό γυάλινο φιαλίδιο τύπου 5 των 5 ml κλειστό με γκρι ελαστικό πώμα 20 mm και διαφανή στεγανοποίηση αλουμινίου με διαφανή μπλε ή μπλε-γαλάζιο χρώμα.
- 10 ml
Το ενέσιμο διάλυμα περιέχεται σε ένα διαυγές σωληνοειδές γυάλινο φιαλίδιο τύπου 10 των 10 ml κλειστό με γκρι ελαστικό πώμα 20 mm και ένα διαφανές μπλε ή μπλε-γαλάζιο σφραγιστικό αλουμινίου 20 mm.
- 20 ml
Το ενέσιμο διάλυμα περιέχεται σε φιαλίδιο διαυγούς γυαλιού τύπου I των 20 ml κλειστό με γκρι ελαστικό πώμα 20 mm και μπλε-μπλε απόχρωση αλουμινίου 20 mm.
- 40 ml
Το ενέσιμο διάλυμα περιέχεται σε φιαλίδιο διαυγούς γυαλιού τύπου I των 50 ml, κλειστό με γκρι ελαστικό πώμα 20 mm και 20 mm μπλε-μπλε αλουμινένιο στεγανοποιητικό πώμα.
- 50 ml
Το ενέσιμο διάλυμα περιέχεται σε φιαλίδιο διαυγούς γυαλιού τύπου Ι των 50 ml κλειστό με γκρι ελαστικό πώμα 20 mm και αποσπώμενη σφραγίδα ιώδους αλουμινίου 20 mm.
Συσκευασία:
- 1 φιαλίδιο του 1 ml, 5 φιαλίδια του 1 ml
- 1 φιαλίδιο των 5 ml, 5 φιαλίδια των 5 ml
- 1 φιαλίδιο των 10 ml 1 φιαλίδιο των 20 ml
- 1 φιαλίδιο των 40 ml
- 1 φιαλίδιο των 50 ml
Μπορεί να μην κυκλοφορούν όλες οι συσκευασίες.
Οι ακόλουθες πληροφορίες προορίζονται μόνο για ιατρούς ή επαγγελματίες υγείας
Δοσολογία και τρόπος χορήγησης
Με ενδοφλέβια έγχυση ή ένεση ή υποδόρια ένεση.
Το Cytarabine 100 mg / ml δεν πρέπει να χορηγείται ενδορραχικά.
Οι συστάσεις για τη δοσολογία μπορούν να μετατραπούν από εκείνες που αφορούν το σωματικό βάρος (mg / kg) σε αυτές που σχετίζονται με την επιφάνεια του σώματος (mg / m2) με τη βοήθεια ονογραμμάτων.
- Πρόκληση ύφεσης:
α) Συνεχής θεραπεία:
θ) Ταχεία ένεση - 2 mg / kg / ημέρα είναι μια εύλογη αρχική δόση. Διαχείριση για 10 ημέρες. Εκτελέστε μετρήσεις αίματος καθημερινά. Εάν δεν παρατηρηθεί αντιλευκαιμική επίδραση και δεν είναι εμφανής η τοξικότητα, αυξήστε τη δόση στα 4 mg / kg / ημέρα και διατηρήστε έως ότου είναι εμφανής η θεραπευτική ανταπόκριση ή η τοξικότητα. Σχεδόν όλοι οι ασθενείς μπορεί να οδηγήσουν σε τοξικότητα με αυτές τις δόσεις.
ii) 0,5-1,0 mg / kg / ημέρα μπορούν να χορηγηθούν ως "έγχυση διάρκειας έως 24 ώρες. Τα αποτελέσματα των εγχύσεων μίας ώρας ήταν ικανοποιητικά στους περισσότερους ασθενείς. Μετά από 10 ημέρες, αυτή η αρχική ημερήσια δόση μπορεί να αυξηθεί σε 2 mg / kg / ημέρα ανάλογα με την τοξικότητα. Συνεχίστε μέχρι την τοξικότητα ή μέχρι να συμβεί ύφεση.
β) Διαλείπουσα θεραπεία:
θ) 3-5 mg / kg / ημέρα χορηγούνται ενδοφλεβίως σε κάθε μία από τις πέντε συνεχόμενες ημέρες. Μετά από περίοδο ανάπαυσης 2-9 ημερών, δίνεται ένα επιπλέον μάθημα. Συνεχίστε μέχρι να εμφανιστεί ανταπόκριση ή τοξικότητα.
Τα πρώτα στοιχεία βελτίωσης του μυελού των οστών έχουν αναφερθεί ότι εμφανίζονται 7-64 ημέρες (μέσος όρος 28 ημέρες) μετά την έναρξη της θεραπείας.
Γενικά, εάν ένας ασθενής δεν παρουσιάσει ούτε τοξικότητα ούτε ύφεση μετά από επαρκή δοκιμαστική περίοδο, απαιτείται προσεκτική χορήγηση υψηλότερων δόσεων. Κανονικά, οι ασθενείς έχουν αποδειχθεί ότι ανέχονται υψηλότερες δόσεις όταν χορηγούνται με ταχεία ενδοφλέβια ένεση και όχι με αργή έγχυση. Αυτή η διαφορά οφείλεται στον γρήγορο μεταβολισμό της κυταραβίνης και στη σύντομη διάρκεια δράσης της υψηλής δόσης που προκύπτει.
ii) Η κυταραβίνη 100-200 mg / m2 / 24 ώρες έχει χρησιμοποιηθεί ως συνεχής έγχυση για 5-7 ημέρες μόνη της ή σε συνδυασμό με άλλους κυτταροστατικούς παράγοντες, συμπεριλαμβανομένης, για παράδειγμα, μιας «ανθρακυκλίνης». Επιπρόσθετα μαθήματα μπορούν να χορηγηθούν σε 2 διαστήματα. -4 εβδομάδες, έως ότου επιτευχθεί ύφεση ή αφόρητη τοξικότητα.
- Θεραπεία συντήρησης:
θ) Οι υποχωρήσεις, που προκλήθηκαν από την κυταραβίνη ή άλλα φαρμακευτικά προϊόντα, μπορούν να διατηρηθούν με ενδοφλέβια ή υποδόρια ένεση 1 mg / kg μία ή δύο φορές την εβδομάδα.
ii) Η κυταραβίνη χορηγήθηκε επίσης σε δόσεις 100-200 mg / m2, ως συνεχής έγχυση για 5 ημέρες σε μηνιαία διαστήματα ως μονοθεραπεία ή σε συνδυασμό με άλλα κυτταροστατικά.
Σε υψηλές δόσεις η κυταραμπίνη χορηγείται 2-3 g / m2 υπό στενή ιατρική παρακολούθηση, ως μονοθεραπεία ή σε συνδυασμό με άλλα κυτταροστατικά, ως ενδοφλέβια έγχυση, για 1-3 ώρες κάθε 12 ώρες για 2-6 ημέρες (συνολικά 12 δόσεις ανά κύκλος.). Δεν πρέπει να γίνεται υπέρβαση της συνολικής δόσης των 36 g / m2.
Παιδιατρικοί ασθενείς:
Η ασφάλεια στα βρέφη δεν έχει τεκμηριωθεί.
Ασθενείς με ηπατική και νεφρική δυσλειτουργία:
Ασθενείς με διαταραγμένη ηπατική ή νεφρική λειτουργία: η δοσολογία πρέπει να μειωθεί.
Ηλικιωμένοι ασθενείς:
Δεν υπάρχουν διαθέσιμες πληροφορίες που να υποδηλώνουν ότι απαιτείται αλλαγή στη δοσολογία στους ηλικιωμένους. Παρ 'όλα αυτά, όπως και ο νεότερος ασθενής, ο ηλικιωμένος ασθενής δεν ανέχεται τοξικότητα από τα ναρκωτικά. Η θεραπεία με υψηλές δόσεις σε ασθενείς άνω των 60 ετών πρέπει να χορηγείται μόνο μετά από "προσεκτική εκτίμηση κινδύνου-οφέλους".
Ασυμφωνία
Ασυμβατότητα με: νάτριο καρβενικιλλίνη, νάτριο κεφαλοθίνη, θειική γενταμικίνη, ηπαρίνη νατρίου, ηλεκτρική νάτριο υδροκορτιζόνη, κανονική ινσουλίνη, μεθοτρεξάτη, 5-φθοροουρακίλη, ναφικιλίνη νάτριο, οξακιλλίνη νάτριο, ηλεκτρική ηλεκτρική πενικιλίνη νατρίου (βενζυλοπενικιλλίνη πρεδνιζολόνη)
Οδηγίες χρήσης / χειρισμού
Μόνο για μία χρήση.
Εάν το διάλυμα φαίνεται αποχρωματισμένο ή περιέχει ορατά σωματίδια, θα πρέπει να απορριφθεί.
Μόλις ανοίξει, το περιεχόμενο κάθε φιαλιδίου πρέπει να χρησιμοποιηθεί αμέσως. Πετάξτε το αχρησιμοποίητο προϊόν.
Τα συχνά χρησιμοποιούμενα υγρά έγχυσης για την κυταραβίνη (βλ. Παράγραφο 6.3) είναι ενέσιμο νερό, 0,9% β / ο φυσιολογικό ορό ή 5% β / ο δεξτρόζη. Η ενέσιμη κυταραβίνη δεν πρέπει να αναμειγνύεται με άλλα φαρμακευτικά προϊόντα εκτός από αυτά που αναφέρονται στην παράγραφο 6.6.
Οδηγίες για τον χειρισμό των κυτταροτοξικών
Διαχείριση:
Πρέπει να χορηγείται από ή υπό την άμεση επίβλεψη ειδικευμένου ιατρού με εμπειρία στη χρήση χημειοθεραπευτικών παραγόντων για τον καρκίνο.
Παρασκευή:
- Οι χημειοθεραπευτικοί παράγοντες πρέπει να παρασκευάζονται για χορήγηση μόνο από επαγγελματίες εκπαιδευμένους στην ασφαλή χρήση του σκευάσματος.
- Λειτουργίες όπως η αραίωση και η μεταφορά στη σύριγγα πρέπει να πραγματοποιούνται μόνο στην κατάλληλη περιοχή.
- Το προσωπικό που εκτελεί αυτές τις διαδικασίες πρέπει να προστατεύεται επαρκώς με ρόμπες, γάντια και γυαλιά.
- Συνιστάται στο έγκυο προσωπικό να μην χειρίζεται τα φάρμακα χημειοθεραπείας.
Απόρριψη και μόλυνση:
Τα αχρησιμοποίητα φάρμακα και τα απόβλητα που προέρχονται από αυτό το φάρμακο πρέπει να απορρίπτονται σύμφωνα με τους τοπικούς κανονισμούς.
Για καταστροφή, τοποθετήστε σε σακούλα / δοχείο διάθεσης απορριμμάτων υψηλού κινδύνου (για κυτταροτοξικά) και αποτέφρωση στους 1100oC.
Σε περίπτωση διασποράς, περιορίστε την πρόσβαση στην πληγείσα περιοχή και φορέστε κατάλληλο προστατευτικό εξοπλισμό, συμπεριλαμβανομένων γαντιών και γυαλιών ασφαλείας. Περιορίστε το άπλωμα και καθαρίστε την περιοχή με χαρτί / απορροφητικό υλικό.
Οι διασπορές μπορούν επίσης να υποβληθούν σε επεξεργασία με 5% υποχλωριώδες νάτριο. Η περιοχή διασποράς πρέπει να καθαριστεί με άφθονο νερό. Τοποθετήστε το μολυσμένο υλικό σε αεροστεγή σακούλα / δοχείο για κυτταροτοξική απόρριψη και αποτέφρωση στους 1100 ° C.
Περίοδος ισχύος
2 χρόνια
Σταθερότητα κατά τη χρήση:
Φυσικοχημική σταθερότητα κατά τη χρήση έχει αποδειχθεί σε ενέσιμο διάλυμα χλωριούχου νατρίου (0,9% β / ο) και δεξτρόζης (5% β / ο) για 24 ώρες κάτω των 25 ° C για έως 72 ώρες. Σε θερμοκρασία 2 έως 8 ° C Από μικροβιολογική άποψη, το φαρμακευτικό προϊόν πρέπει να χρησιμοποιείται αμέσως. Εάν δεν χρησιμοποιηθεί αμέσως, οι χρόνοι και οι συνθήκες αποθήκευσης πριν από τη χρήση είναι ευθύνη του χρήστη και κανονικά δεν θα υπερβαίνουν τις 24 ώρες στους 2 έως 8 ° C, εκτός εάν έχει γίνει αραίωση σε συνθήκες άσηπτης ελεγχόμενης και επικυρωμένης.
αποθήκευση
Μην φυλάσσετε σε θερμοκρασία μεγαλύτερη των 25 ° C.
Μην ψύχετε ή παγώνετε.
Φύλλο οδηγιών χρήσης: AIFA (Ιταλικός Οργανισμός Φαρμάκων). Περιεχόμενο που δημοσιεύτηκε τον Ιανουάριο 2016. Οι πληροφορίες που υπάρχουν δεν μπορεί να είναι ενημερωμένες.
Για να έχετε πρόσβαση στην πιο ενημερωμένη έκδοση, είναι σκόπιμο να αποκτήσετε πρόσβαση στον ιστότοπο AIFA (Ιταλικός Οργανισμός Φαρμάκων). Αποποίηση ευθυνών και χρήσιμες πληροφορίες.
01.0 ΟΝΟΜΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟDΟΝΤΟΣ
CITARABIAN ACCORD 100 MG / ML ΛΥΣΗ ΓΙΑ ΕΝΕΣΗ FOR ΓΙΑ ΕΝΔΟΞΗ
02.0 ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ
1 ml περιέχει 100 mg κυταραβίνη.
Κάθε φιαλίδιο 1 ml περιέχει 100 mg κυταραβίνη.
Κάθε φιαλίδιο των 5 ml περιέχει 500 mg κυταραβίνης.
Κάθε φιαλίδιο των 10 ml περιέχει 1 g κυταραβίνης.
Κάθε φιαλίδιο των 20 ml περιέχει 2 g κυταραβίνης.
Κάθε φιαλίδιο των 40 ml περιέχει 4 g κυταραβίνης
Κάθε φιαλίδιο των 50 ml περιέχει 5 g κυταραβίνης
Για τον πλήρη κατάλογο των εκδόχων, ανατρέξτε στην ενότητα 6.1.
03.0 ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ ΜΟΡΦΗ
Ενέσιμο διάλυμα ή έγχυση.
Το προϊόν είναι ένα διαυγές, άχρωμο διάλυμα πρακτικά απαλλαγμένο από σωματίδια.
ρΗ: 7,0-9,5
04.0 ΚΛΙΝΙΚΕΣ ΠΛΗΡΟΦΟΡΙΕΣ
04.1 Θεραπευτικές ενδείξεις
Για την πρόκληση ύφεσης στην οξεία μυελογενή λευχαιμία σε ενήλικες και για άλλες μορφές οξείας λευχαιμίας σε ενήλικες και παιδιά.
04.2 Δοσολογία και τρόπος χορήγησης
Δοσολογία
Η θεραπεία με κυταραμπίνη θα πρέπει να ξεκινά ή να συνεννοείται με γιατρό με ειδική εμπειρία στη θεραπεία κυτταροστατικών. Μπορούν να δοθούν μόνο γενικές συστάσεις καθώς η οξεία λευχαιμία αντιμετωπίζεται σχεδόν αποκλειστικά με συνδυασμούς κυτταροστατικών.
Οι συστάσεις για τη δοσολογία μπορούν να γίνουν ανάλογα με το σωματικό βάρος (mg / kg) ή ανάλογα με την επιφάνεια του σώματος (BSA, mg / m2).
Οι συστάσεις για τη δοσολογία μπορούν να μετατραπούν από εκείνες που αφορούν το βάρος του σώματος σε εκείνες που σχετίζονται με την επιφάνεια του σώματος με τη βοήθεια ονογραμμάτων.
1. Επαγωγή ύφεσης:
Η επαγωγική δοσολογία της θεραπείας και το πρόγραμμα θεραπείας ποικίλλουν ανάλογα με το σχήμα που χρησιμοποιείται.
α) Συνεχής θεραπεία:
Τα ακόλουθα σχήματα δοσολογίας έχουν χρησιμοποιηθεί για συνεχή θεραπεία για την πρόκληση ύφεσης.
θ) Ταχεία ένεση - μια δόση έναρξης 2 mg / kg / ημέρα είναι επαρκής. Διαχείριση για 10 ημέρες. Εκτελέστε μετρήσεις αίματος καθημερινά. Εάν δεν παρατηρηθεί αντιλευκαιμική επίδραση και δεν είναι εμφανής η τοξικότητα, αυξήστε τη δόση στα 4 mg / kg / ημέρα και διατηρήστε έως ότου είναι εμφανής η θεραπευτική ανταπόκριση ή η τοξικότητα. Για σχεδόν όλους τους ασθενείς αυτές οι δόσεις μπορεί να είναι τοξικές.
ii) 0,5-1,0 mg / kg / ημέρα μπορούν να χορηγηθούν ως έγχυση διάρκειας έως 24 ωρών. Τα αποτελέσματα των εγχύσεων μίας ώρας ήταν ικανοποιητικά για τους περισσότερους ασθενείς.Μετά από 10 ημέρες, αυτή η αρχική ημερήσια δόση μπορεί να αυξηθεί σε 2 mg / kg / ημέρα ανάλογα με την τοξικότητα. Συνεχίστε μέχρι την τοξικότητα ή έως ότου εμφανιστεί ύφεση.
β) Διαλείπουσα θεραπεία:
Τα ακόλουθα σχήματα δόσης έχουν χρησιμοποιηθεί για θεραπεία που προκαλεί διαλείπουσα ύφεση.
θ) 3-5 mg / kg / ημέρα χορηγούνται ενδοφλεβίως κάθε μία από τις πέντε συνεχόμενες ημέρες. Μετά από περίοδο ανάπαυσης 2-9 ημερών, δίνεται ένα επιπλέον μάθημα. Συνεχίστε μέχρι να εμφανιστεί ανταπόκριση ή τοξικότητα.
Τα πρώτα στοιχεία βελτίωσης του μυελού των οστών έχουν αναφερθεί ότι εμφανίζονται 7-64 ημέρες (μέσος όρος 28 ημέρες) μετά την έναρξη της θεραπείας.
Γενικά, εάν ένας ασθενής δεν παρουσιάσει ούτε τοξικότητα ούτε ύφεση μετά από επαρκή δοκιμαστική περίοδο, είναι δικαιολογημένο να χορηγούνται υψηλότερες δόσεις με προσοχή. Κανονικά, οι ασθενείς έχουν αποδειχθεί ότι ανέχονται υψηλότερες δόσεις όταν χορηγούνται με ταχεία ενδοφλέβια ένεση σε σύγκριση με την αργή έγχυση. Αυτή η διαφορά οφείλεται στον γρήγορο μεταβολισμό της κυταραμπίνης και στη σύντομη διάρκεια δράσης της υψηλής δόσης που προκύπτει.
ii) Η κυταραβίνη 100-200 mg / m2 / 24 ώρες έχει χρησιμοποιηθεί ως συνεχής έγχυση για 5-7 ημέρες μόνη της ή σε συνδυασμό με άλλους κυτταροστατικούς παράγοντες, συμπεριλαμβανομένης, για παράδειγμα, μιας «ανθρακυκλίνης». Επιπρόσθετα μαθήματα μπορούν να χορηγηθούν σε 2 διαστήματα. -4 εβδομάδες, έως ότου επιτευχθεί ύφεση ή αφόρητη τοξικότητα.
2. Θεραπεία συντήρησης:
Η δοσολογία συντήρησης και το πρόγραμμα διαφέρουν ανάλογα με το σχήμα που χρησιμοποιείται.
Τα ακόλουθα σχήματα δοσολογίας έχουν χρησιμοποιηθεί για συνεχή θεραπεία για την πρόκληση ύφεσης.
θ) Οι υποχωρήσεις, που προκλήθηκαν από την κυταραβίνη ή άλλα φαρμακευτικά προϊόντα, μπορούν να διατηρηθούν με ενδοφλέβια ή υποδόρια ένεση 1 mg / kg μία ή δύο φορές την εβδομάδα.
ii) Η κυταραβίνη χορηγήθηκε επίσης σε δόσεις 100-200 mg / m2, ως συνεχής έγχυση για 5 ημέρες σε μηνιαία διαστήματα ως μονοθεραπεία ή σε συνδυασμό με άλλα κυτταροστατικά.
Υψηλές δόσεις :
Η κυταραμπίνη χορηγείται στα 2-3 g / m2 υπό στενή ιατρική παρακολούθηση, ως μονοθεραπεία ή σε συνδυασμό με άλλα κυτταροστατικά, ως ενδοφλέβια έγχυση, για 1-3 ώρες κάθε 12 ώρες για 2-6 ημέρες (συνολικά 12 δόσεις ανά κύκλο) Το Δεν πρέπει να γίνεται υπέρβαση της συνολικής δόσης των 36 g / m2. Η συχνότητα των κύκλων θεραπείας εξαρτάται από την ανταπόκριση στη θεραπεία και από την αιματολογική και μη αιματολογική τοξικότητα. Ανατρέξτε επίσης στις προφυλάξεις για τις απαιτήσεις διακοπής της θεραπείας.
Παιδιατρικοί ασθενείς :
Η ασφάλεια στα βρέφη δεν έχει τεκμηριωθεί.
Ασθενείς με ηπατική και νεφρική δυσλειτουργία :
Ασθενείς με διαταραγμένη ηπατική ή νεφρική λειτουργία: η δοσολογία πρέπει να μειωθεί.
Η κυταραβίνη μπορεί να υποβληθεί σε διαπίδυση. Επομένως, η κυταραβίνη δεν πρέπει να χορηγείται αμέσως πριν ή μετά την αιμοκάθαρση.
Ηλικιωμένοι ασθενείς :
Θεραπεία υψηλής δόσης σε ασθενείς άνω των 60 ετών πρέπει να χορηγείται μόνο μετά από προσεκτική εκτίμηση κινδύνου-οφέλους.
Τρόπος χορήγησης :
Για οδηγίες σχετικά με την αραίωση του φαρμακευτικού προϊόντος πριν από τη χορήγηση, βλέπε παράγραφο 6.6.
Η ενέσιμη κυταραβίνη προορίζεται για ενδοφλέβια έγχυση ή ένεση ή υποδόρια ένεση.
Η υποδόρια ένεση είναι γενικά καλά ανεκτή και μπορεί να συνιστάται όταν χρησιμοποιείται στη θεραπεία συντήρησης.
Το Cytarabine 100 mg / ml δεν πρέπει να χορηγείται ενδορραχικά.
04.3 Αντενδείξεις
Υπερευαισθησία στην κυταραβίνη ή σε κάποιο από τα έκδοχα της ενέσιμης κυταραβίνης.
Αναιμία, λευκοπενία και θρομβοπενία μη κακοήθους αιτιολογίας (π.χ. απλασία μυελού των οστών), εκτός εάν ο γιατρός θεωρήσει ότι αυτή η θεραπεία είναι η καλύτερη εναλλακτική λύση για τον ασθενή.
Εκφυλιστικές και τοξικές εγκεφαλοπάθειες, ειδικά μετά τη χρήση μεθοτρεξάτης ή θεραπεία με ιονίζουσα ακτινοβολία.
04.4 Ειδικές προειδοποιήσεις και κατάλληλες προφυλάξεις κατά τη χρήση
Παιδιατρικοί ασθενείς
Η ασφάλεια αυτού του φαρμάκου δεν έχει τεκμηριωθεί σε βρέφη.
Προειδοποιήσεις:
Η κυταραμπίνη είναι ένα ισχυρό μυελοκατασταλτικό. Η θεραπεία πρέπει να ξεκινά με προσοχή σε ασθενείς με προϋπάρχουσα κατάθλιψη του μυελού των οστών που προκαλείται από φάρμακα. Οι ασθενείς που λαμβάνουν θεραπεία με αυτό το φαρμακευτικό προϊόν θα πρέπει να βρίσκονται υπό στενή ιατρική παρακολούθηση και, κατά τη διάρκεια της επαγωγικής θεραπείας, θα πρέπει να γίνονται καθημερινά μετρήσεις λευκών αιμοσφαιρίων και αιμοπεταλίων. Θα πρέπει να γίνονται συχνά εξετάσεις μυελού των οστών μετά την εξαφάνιση των μορφών έκρηξης. Από περιφερικό αίμα.
Πρέπει να υπάρχουν όλα τα κατάλληλα μέτρα για τη διαχείριση των επιπλοκών, συμπεριλαμβανομένων των θανατηφόρων, της καταστολής του μυελού των οστών (λοιμώξεις που προκύπτουν από την κοκκιοκυτταροπενία και τη βλάβη άλλων αμυντικών συστημάτων του σώματος και δευτερογενή αιμορραγία λόγω θρομβοπενίας).
Έχουν αναφερθεί αναφυλακτικές αντιδράσεις μετά από θεραπεία με κυταραβίνη. Αναφέρθηκε ένα περιστατικό αναφυλαξίας που οδήγησε σε οξεία καρδιοπνευμονική ανακοπή και που απαιτούσε ανάνηψη του ασθενούς. Αυτό το συμβάν εμφανίστηκε αμέσως μετά την ενδοφλέβια χορήγηση κυταραμπίνης.
Η κυταραβίνη που χορηγείται σύμφωνα με πειραματικά σχήματα δοσολογίας έχει προκαλέσει σοβαρή και μερικές φορές θανατηφόρα τοξικότητα του ΚΝΣ, του γαστρεντερικού σωλήνα και των πνευμόνων (διαφορετική από αυτή που παρατηρείται με τα συμβατικά σχήματα κυτταραμπίνης). Αυτές οι αντιδράσεις περιλαμβάνουν: αναστρέψιμη τοξικότητα του κερατοειδούς, εγκεφαλική και εγκεφαλική δυσλειτουργία. Συνήθως αναστρέψιμη παρεγκεφαλίδα, υπνηλία, σπασμοί, σοβαρό γαστρεντερικό έλκος συμπεριλαμβανομένης της εντερικής κυστοειδούς πνεύμονας με αποτέλεσμα περιτονίτιδα, σήψη και αποστήματα ήπατος και πνευμονικό οίδημα.
Η κυταραβίνη έχει αποδειχθεί ότι είναι καρκινογόνος σε ζώα. Η πιθανότητα παρόμοιου αποτελέσματος θα πρέπει να λαμβάνεται υπόψη κατά τον προγραμματισμό της μακροχρόνιας θεραπείας του ασθενούς.
Προφυλάξεις:
Οι ασθενείς που λαμβάνουν κυταραβίνη πρέπει να βρίσκονται υπό στενή ιατρική παρακολούθηση. Ο αριθμός των αιμοπεταλίων και των λευκών αιμοσφαιρίων πρέπει να γίνεται συχνά. Η θεραπεία πρέπει να διακοπεί ή να τροποποιηθεί όταν η προκαλούμενη από φάρμακα καταστολή του μυελού των οστών έχει ως αποτέλεσμα τον αριθμό αιμοπεταλίων κάτω από 50.000 mm3 ή αριθμό αιμοπεταλίων κάτω από 50.000 mm3. πολυμορφοπυρηνικά λευκοκύτταρα κάτω από 1.000 mm3. Οι αριθμοί περιφερικού σχηματισμού αίματος μπορεί να συνεχίσουν να μειώνονται μετά την απόσυρση του φαρμάκου και να φτάνουν στις χαμηλότερες τιμές τους μετά από διαστήματα χωρίς φάρμακα πέντε έως επτά ημερών. Εάν υποδεικνύεται, η θεραπεία μπορεί να συνεχιστεί όταν εμφανιστούν ακριβή σημάδια ανάκτησης μυελού των οστών (σε επόμενες εξετάσεις μυελού των οστών). Ο έλεγχος της νόσου μπορεί να χαθεί για εκείνους τους ασθενείς που έχουν σταματήσει να παίρνουν το φάρμακο έως ότου δεν επιτευχθούν οι "φυσιολογικές" τιμές περιφερικού αίματος Το
Περιφερική κινητική και αισθητηριακή νευροπάθεια έχει αναφερθεί μετά από ενοποίηση με υψηλές δόσεις κυταραβίνης, δαουνορουμπικίνης και ασπαραγινάσης σε ενήλικες ασθενείς με οξεία μη λεμφοκυτταρική λευχαιμία. Ασθενείς που λαμβάνουν υψηλές δόσεις κυταραβίνης θα πρέπει να παρακολουθούνται για νευροπάθεια, καθώς μπορεί να υπάρξουν αλλαγές στο πρόγραμμα δοσολογίας. απαραίτητο για την αποφυγή εμφάνισης μη αναστρέψιμων νευρολογικών διαταραχών.
Έχουν αναφερθεί σοβαρή και σε ορισμένες περιπτώσεις θανατηφόρα πνευμονική τοξικότητα, σύνδρομο αναπνευστικής δυσχέρειας ενηλίκων και πνευμονικό οίδημα μετά από υψηλή δόση κυταραμπίνης.
Μετά από ταχεία ενδοφλέβια χορήγηση, οι ασθενείς συχνά επηρεάζονται από ναυτία και έμετο που μπορεί να διαρκέσουν έως και αρκετές ώρες. Αυτό το πρόβλημα είναι συνήθως λιγότερο όταν το φάρμακο χορηγείται με έγχυση.
Κοιλιακός πόνος (περιτονίτιδα) και δοκιμασία θετικής κολίτιδας guaiac, με σχετιζόμενη ουδετεροπενία και θρομβοπενία, έχουν αναφερθεί σε ασθενείς που έλαβαν θεραπεία με συμβατικές δόσεις κυταραβίνης σε συνδυασμό με άλλα φαρμακευτικά προϊόντα. Οι ασθενείς ανταποκρίθηκαν σε μη χειρουργική ιατρική παρέμβαση.
Σε παιδιά με ΟΜΛ έχει αναφερθεί καθυστερημένη προοδευτική ανερχόμενη παράλυση, η οποία ήταν θανατηφόρα, μετά από ενδορραχιαία και ενδοφλέβια χορήγηση συμβατικών δόσεων κυταραβίνης σε συνδυασμό με άλλα φαρμακευτικά προϊόντα.
Ασθενείς με προϋπάρχουσα ηπατική δυσλειτουργία
Τόσο η ηπατική όσο και η νεφρική λειτουργία πρέπει να παρακολουθούνται κατά τη διάρκεια της θεραπείας με κυτταραμπίνη. Σε ασθενείς με προϋπάρχουσα ηπατική ανεπάρκεια, η κυταραβίνη πρέπει να χορηγείται μόνο με εξαιρετική προσοχή.
Θα πρέπει να πραγματοποιούνται περιοδικοί έλεγχοι της δραστηριότητας του μυελού των οστών και της ηπατικής και νεφρικής λειτουργίας σε ασθενείς που λαμβάνουν κυταραβίνη.
Όπως και άλλα κυτταροτοξικά φάρμακα, η κυταραβίνη μπορεί να προκαλέσει υπερουριχαιμία δευτερογενή σε ταχεία λύση των καρκινικών κυττάρων. Οι γιατροί πρέπει να παρακολουθούν τα επίπεδα ουρικού οξέος στο αίμα του ασθενούς και να είναι προετοιμασμένοι να ξεκινήσουν υποστηρικτικά και φαρμακολογικά μέτρα που μπορεί να χρειαστούν για τον έλεγχο αυτού του προβλήματος.
Εμβόλια / Ανοσοκατασταλτικά αποτελέσματα / Αυξημένη ευαισθησία σε λοιμώξεις.
Η χορήγηση ζωντανών ή ζωντανών εξασθενημένων εμβολίων σε ασθενείς ανοσοκατεσταλμένους από χημειοθεραπευτικούς παράγοντες, συμπεριλαμβανομένης της κυταραβίνης, μπορεί να οδηγήσει σε σοβαρές ή θανατηφόρες λοιμώξεις. Ο εμβολιασμός με ζωντανό εμβόλιο πρέπει να αποφεύγεται σε ασθενείς που λαμβάνουν κυταραβίνη. Μπορούν να χορηγηθούν σκοτωμένα ή αδρανοποιημένα εμβόλια. Ωστόσο, η ανταπόκριση σε τέτοια εμβόλια θα μπορούσε να μειωθεί.
Υψηλές δόσεις
Ο κίνδυνος παρενεργειών του ΚΝΣ είναι υψηλότερος σε ασθενείς που έχουν ήδη υποβληθεί σε θεραπεία του ΚΝΣ, όπως ενδορραχιαία χημειοθεραπεία ή ακτινοθεραπεία.
Η ταυτόχρονη μετάγγιση κοκκιοκυττάρων πρέπει να αποφεύγεται καθώς έχει αναφερθεί σοβαρή αναπνευστική ανεπάρκεια.
Έχουν αναφερθεί περιπτώσεις καρδιομυοπάθειας με επακόλουθο θάνατο μετά από πειραματική θεραπεία με υψηλές δόσεις κυταραβίνης σε συνδυασμό με κυκλοφωσφαμίδη όταν χρησιμοποιούνται για προετοιμασία για μεταμόσχευση μυελού των οστών.
04.5 Αλληλεπιδράσεις με άλλα φαρμακευτικά προϊόντα και άλλες μορφές αλληλεπίδρασης
5-φθοροκυτοσίνη
Η 5-φθοροκυτοσίνη δεν πρέπει να χορηγείται με κυταραβίνη, επειδή η θεραπευτική αποτελεσματικότητα της 5-φθοροκυτοσίνης έχει αποδειχθεί ότι καταργείται κατά τη διάρκεια αυτής της θεραπείας.
Διγοξίνη
Αναστρέψιμες μειώσεις των συγκεντρώσεων διγοξίνης σε σταθερή κατάσταση και έκκριση νεφρικού γλυκοζιδίου έχουν παρατηρηθεί σε ασθενείς που λαμβάνουν βήτα-ακετυλοδιγοξίνη με χημειοθεραπευτικά σχήματα που περιέχουν κυκλοφωσφαμίδη, βινκριστίνη και πρεδνιζόνη με ή χωρίς κυταραβίνη ή προκαρβαζίνη. Οι συγκεντρώσεις διγοξίνης στο πλάσμα σε σταθερή κατάσταση δεν φαίνεται να αλλάζουν Ως εκ τούτου, η παρακολούθηση των επιπέδων διγοξίνης στο πλάσμα μπορεί να ενδείκνυται σε ασθενείς που λαμβάνουν παρόμοια χημειοθεραπεία. Η χρήση της ψηφιοξίνης σε αυτούς τους ασθενείς μπορεί να θεωρηθεί ως εναλλακτική λύση.
Γενταμικίνη
Μελέτη αλληλεπίδρασης in vitro μεταξύ γενταμικίνης και κυταραβίνης κατέδειξαν ανταγωνισμό που σχετίζεται με την κυταραβίνη στην ευαισθησία των στελεχών του Κ. pneumoniae. Σε ασθενείς που έλαβαν θεραπεία με κυταραβίνη και έλαβαν γενταμικίνη για «μόλυνση από Κ. Πνευμονία», η απουσία άμεσης θεραπευτικής απόκρισης μπορεί να υποδηλώνει την ανάγκη επανεκτίμησης της αντιβακτηριακής θεραπείας.
Χρήση της κυταραβίνης μόνη της ή σε συνδυασμό με άλλους ανοσοκατασταλτικούς παράγοντες
Λόγω της ανοσοκατασταλτικής δράσης της ενέσιμης κυταραβίνης, ιογενείς, βακτηριακές, μυκητιακές, παρασιτικές ή σαπροφυτικές λοιμώξεις οπουδήποτε στο σώμα μπορεί να σχετίζονται με τη χρήση της κυταραμπίνης μόνη της ή σε συνδυασμό με άλλους ανοσοκατασταλτικούς παράγοντες μετά από ανοσοκατασταλτικές δόσεις που επηρεάζουν την κυτταρική ή χυμική ανοσία. Αυτές οι λοιμώξεις μπορεί να είναι ήπιες, αλλά μπορεί να είναι σοβαρές και μερικές φορές θανατηφόρες.
04.6 Κύηση και γαλουχία
Εγκυμοσύνη
Η κυταραβίνη είναι γνωστό ότι έχει τερατογόνο δράση σε ορισμένα είδη ζώων. Η χρήση του citara bine σε γυναίκες που είναι έγκυες ή μπορεί να μείνουν έγκυες πρέπει να γίνεται μόνο αφού ληφθούν υπόψη τα πιθανά οφέλη και κίνδυνοι.Οι γυναίκες πρέπει να χρησιμοποιούν αποτελεσματικές μεθόδους ελέγχου των γεννήσεων κατά τη διάρκεια της θεραπείας και για έως και 6 μήνες μετά τη θεραπεία.
Ωρα ταίσματος
Αυτό το φάρμακο κανονικά δεν πρέπει να χορηγείται σε ασθενείς που είναι έγκυες ή σε μητέρες που θηλάζουν.
Γονιμότητα
Δεν έχουν διεξαχθεί μελέτες γονιμότητας για την αξιολόγηση της τοξικότητας της κυταραβίνης στην αναπαραγωγή. Αναστολή των γονάδων, με αποτέλεσμα αμηνόρροια ή αζωοσπερμία, μπορεί να συμβεί σε ασθενείς που λαμβάνουν κυταραβίνη, ειδικά σε συνδυασμό με παράγοντες αλκυλίωσης. Γενικά, αυτές οι επιδράσεις φαίνεται να σχετίζονται με τη δόση και τη διάρκεια της θεραπείας και μπορεί να είναι μη αναστρέψιμες (βλ. Παράγραφο 4.8. Η κυταραβίνη έχει μεταλλαξιογόνο δυναμικό που μπορεί να προκαλέσει χρωμοσωμική βλάβη στα σπερματοζωάρια του ανθρώπου, τα αρσενικά που υποβάλλονται σε θεραπεία με κυτταραμπίνη και οι σύντροφοί τους θα πρέπει να συμβουλεύονται να χρησιμοποιούν αξιόπιστη αντισύλληψη κατά τη διάρκεια της θεραπείας και έως και έξι μήνες μετά τη θεραπεία.
04.7 Επιδράσεις στην ικανότητα οδήγησης και χειρισμού μηχανών
Η κυταραβίνη δεν επηρεάζει την ικανότητα οδήγησης και χειρισμού μηχανών. Ωστόσο, η ικανότητα οδήγησης ή χειρισμού μηχανών μπορεί να επηρεαστεί σε ασθενείς που λαμβάνουν χημειοθεραπεία, επομένως οι ασθενείς θα πρέπει να προειδοποιούνται και να συμβουλεύονται να αποφεύγουν τέτοιες δραστηριότητες εάν συμβεί αυτό.
04.8 Ανεπιθύμητες ενέργειες
Οι ακόλουθες ανεπιθύμητες ενέργειες έχουν αναφερθεί σε σχέση με τη θεραπεία με κυταραμπίνη:
Οι συχνότητες καθορίζονται χρησιμοποιώντας την ακόλουθη σύμβαση:
Πολύ συνηθισμένο (/1 / 10)
Κοινή (/1 / 100,
Όχι συχνές (≥1 / 1.000 έως
Σπάνια (/1 / 10.000,
Πολύ σπάνιο (
Άγνωστο (η συχνότητα δεν μπορεί να εκτιμηθεί από τα διαθέσιμα δεδομένα)
Οι ανεπιθύμητες ενέργειες που προκαλούνται από την κυταραβίνη είναι δοσοεξαρτώμενες. Οι πιο συχνές είναι οι γαστρεντερικές παρενέργειες. Η κυταραβίνη είναι τοξική για τον μυελό των οστών και προκαλεί αιματολογικές παρενέργειες.
Λοιμώξεις και προσβολές:
Ασυνήθης: Σήψη (ανοσοκαταστολή), κυτταρίτιδα στο σημείο της ένεσης
Αγνωστο: Πνευμονία, απόστημα ήπατος
Νεοπλάσματα καλοήθη, κακοήθη και απροσδιόριστα (συμπεριλαμβανομένων των κύστεων και των πολύποδων):
Ασυνήθης: Lentigo
Διαταραχές του αίματος και του λεμφικού συστήματος:
κοινός: Αναιμία, μεγαλοβλάστωση, λευκοπενία, θρομβοπενία.
Αγνωστο: Δικτυοκυτταροπενία.
Η σοβαρότητα αυτών των αντιδράσεων εξαρτάται από τη δοσολογία και το δοσολογικό σχήμα. Μπορεί να εμφανιστούν αλλαγές στη μορφολογία των κυττάρων του μυελού των οστών και των περιφερικών επιχρισμάτων.
Διαταραχές του ανοσοποιητικού συστήματος:
Ασυνήθης: Αναφυλαξία.
Αγνωστο: Αλλεργικό οίδημα.
Διαταραχές μεταβολισμού και διατροφής:
κοινός: Ανορεξία, υπερουριχαιμία.
Διαταραχές του νευρικού συστήματος:
κοινός: Σε υψηλές δόσεις, παρεγκεφαλιδική ή εγκεφαλική επίδραση με επιδείνωση του επιπέδου συνείδησης, δυσαρθρία, νυσταγμός.
Ασυνήθης: Πονοκέφαλος, περιφερική νευροπάθεια
Αγνωστο: Νευροτοξικότητα, νευρίτιδα, ζάλη
Διαταραχές των ματιών:
κοινός: Αναστρέψιμη αιμορραγική επιπεφυκίτιδα (φωτοφοβία, κάψιμο, διαταραχή της όρασης, αυξημένη δακρύρροια), κερατίτιδα.
Αγνωστο: Επιπεφυκίτιδα (μπορεί να σχετίζεται με εξάνθημα).
Καρδιακές διαταραχές:
Ασυνήθης: Περικαρδίτιδα.
Πολύ σπάνιο: Αρρυθμία.
Διαταραχές του αναπνευστικού, του θώρακα και του μεσοθωρακίου:
Ασυνήθης: Πνευμονία, δύσπνοια, πονόλαιμος.
Γαστρεντερικές διαταραχές:
κοινός: Δυσφαγία, κοιλιακό άλγος, ναυτία, έμετος, διάρροια, στοματική / πρωκτική φλεγμονή ή έλκος.
Ασυνήθης: Οισοφαγίτιδα, έλκος οισοφάγου, πνευμονία εντερικής κυστοειδούς, νεκρωτική κολίτιδα, περιτονίτιδα.
Αγνωστο: Παγκρεατίτιδα.
Ηπατοχολικές διαταραχές:
κοινός: Αναστρέψιμες επιδράσεις στο ήπαρ με αυξημένα επίπεδα ενζύμων.
Ασυνήθης: Undκτερος.
Αγνωστο: Ηπατική δυσλειτουργία.
Διαταραχές του δέρματος και του υποδόριου ιστού:
κοινός: Αναστρέψιμες ανεπιθύμητες ενέργειες στο δέρμα, όπως ερύθημα, φλεγμονώδης δερματίτιδα, κνίδωση, αγγειίτιδα, αλωπεκία.
Ασυνήθης: Δέρμα εξέλκωση, κνησμός, καύση πόνου στις παλάμες και τα πέλματα των ποδιών.
Πολύ σπάνιο: Ουδετερόφιλος εκκλητικός υδραδενίτης.
Αγνωστο: Εφελίδες, δερματικό εξάνθημα.
Διαταραχές του μυοσκελετικού και του συνδετικού ιστού:
Ασυνήθης: Μυαλγία, αρθραλγία.
Διαταραχές των νεφρών και των ούρων:
κοινός: Νεφρική δυσλειτουργία, κατακράτηση ούρων.
Γενικές διαταραχές και καταστάσεις στο σημείο χορήγησης:
κοινός: Πυρετός, θρομβοφλεβίτιδα στο σημείο της ένεσης.
Ασυνήθης: Πόνος στο στήθος.
Σύνδρομο Cytarabine (Ara-C) (Ανοσοαλλεργικό αποτέλεσμα):
Πυρετός, μυαλγία, οστικός πόνος, περιστασιακά πόνος στο στήθος, εξάνθημα, επιπεφυκίτιδα και ναυτία μπορεί να εμφανιστούν 6 έως 12 ώρες μετά την έναρξη της θεραπείας. Η χορήγηση κορτικοστεροειδών μπορεί να θεωρηθεί ως προφύλαξη και θεραπεία. Εάν τα κορτικοστεροειδή είναι αποτελεσματικά, μπορεί να συνεχιστεί η χορήγηση. Κυταραβίνη θεραπεία.
Οι ανεπιθύμητες ενέργειες λόγω θεραπείας με υψηλές δόσεις κυταραβίνης, εκτός από αυτές που παρατηρούνται με συμβατικές δόσεις περιλαμβάνουν:
Αιματολογική τοξικότητα:
Θεωρείται ως βαθιά πανκυτταροπενία που μπορεί να διαρκέσει 15-25 ημέρες με πιο σοβαρή απλασία μυελού των οστών από ό, τι παρατηρείται σε συμβατικές δόσεις.
Λοιμώξεις και προσβολές: Σήψη, απόστημα ήπατος.
Διαταραχές του νευρικού συστήματος:
Μετά από θεραπεία σε υψηλές δόσεις κυταραμπίνης, συμπτώματα εγκεφαλικής ή παρεγκεφαλικής δυσλειτουργίας, όπως αλλαγές προσωπικότητας, διαταραχή διαύγειας, δυσαρθρία, αταξία, τρόμος, νυσταγμός, πονοκέφαλος, σύγχυση, υπνηλία, εμφανίζονται στο 8-37% των θεραπευόμενων ασθενών, ζάλη, κώμα, σπασμοί κλπ. Περιφερικές κινητικές και αισθητηριακές νευροπάθειες έχουν επίσης αναφερθεί μετά από θεραπεία σε υψηλές δόσεις Η συχνότητα στους ηλικιωμένους (> 55 ετών) μπορεί να είναι υψηλότερη. Άλλοι προδιαθεσικοί παράγοντες είναι η διαταραχή της ηπατικής και νεφρικής λειτουργίας, η προηγούμενη θεραπεία του ΚΝΣ (π.χ. ακτινοθεραπεία) και η κατάχρηση αλκοόλ.Στις περισσότερες περιπτώσεις, οι αλλαγές στο ΚΝΣ είναι αναστρέψιμες.
Ο κίνδυνος τοξικότητας από το ΚΝΣ αυξάνεται εάν η θεραπεία με κυταραβίνη - που χορηγείται σε υψηλές δόσεις μέσω της ενδοφλέβιας οδού - σχετίζεται με άλλη τοξική θεραπεία από το ΚΝΣ, όπως ακτινοθεραπεία ή υψηλές δόσεις.
Τοξικότητα κερατοειδούς και επιπεφυκότα:
Έχουν περιγραφεί βλάβες του κερατοειδούς και αιμορραγική επιπεφυκίτιδα. Αυτά τα φαινόμενα μπορούν να προληφθούν ή να μειωθούν με την ενστάλαξη κορτικοστεροειδών σε κολλύρια.
Διαταραχές του δέρματος και του υποδόριου ιστού: δερματικό εξάνθημα που προκαλεί ξεφλούδισμα, αλωπεκία.
Ιογενείς, βακτηριακές, μυκητιακές, παρασιτικές ή σαπροφυτικές λοιμώξεις, σε οποιοδήποτε σημείο του σώματος, μπορεί να σχετίζονται με τη χρήση της κυταραβίνης μόνη της ή σε συνδυασμό με άλλους ανοσοκατασταλτικούς παράγοντες, μετά από χορήγηση δόσεων που επηρεάζουν την κυτταρική ή χυμική ανοσία. Αυτές οι λοιμώξεις μπορεί να είναι ήπιες, αλλά μπορεί να είναι και σοβαρές.
Έχει περιγραφεί ένα σύνδρομο κυταραβίνης. Χαρακτηρίζεται από πυρετό, μυαλγία, πόνο στα οστά, περιστασιακά πόνο στο στήθος, εξάνθημα της ωχράς κηλίδας, επιπεφυκίτιδα και αδιαθεσία. Εμφανίζεται συνήθως 6-12 ώρες μετά τη χορήγηση φαρμάκου. Η χορήγηση κορτικοστεροειδών έχει βρεθεί ότι είναι αποτελεσματική στη θεραπεία ή την πρόληψη αυτού του συνδρόμου. του συνδρόμου είναι αρκετά σοβαρά ώστε να απαιτούν θεραπεία, θα πρέπει να προβλεφθεί τόσο η χρήση κορτικοστεροειδών όσο και η συνέχιση της θεραπείας με κυταραβίνη.
Γαστρεντερικές διαταραχές:
Ιδιαίτερα στη θεραπεία με υψηλές δόσεις κυταραβίνης, εκτός από τα κοινά συμπτώματα, μπορεί να εμφανιστούν πιο σοβαρές αντιδράσεις. Έχουν αναφερθεί εντερική διάτρηση ή νέκρωση με ειλεό και περιτονίτιδα.
Μετά από θεραπεία σε υψηλές δόσεις έχουν παρατηρηθεί ηπατικά αποστήματα, ηπατομεγαλία, σύνδρομο Budd-Chiari (θρόμβωση ηπατικής φλέβας) και παγκρεατίτιδα.
Διαταραχές του αναπνευστικού, του θώρακα και του μεσοθωρακίου:
Κλινικά συμπτώματα παρόμοια με αυτά που υπάρχουν στο πνευμονικό οίδημα / ARDS μπορεί να αναπτυχθούν, ειδικά σε θεραπεία υψηλής δόσης. Η αντίδραση πιθανώς προκαλείται από κυψελιδική τριχοειδή βλάβη. Είναι δύσκολο να εκτιμηθεί η συχνότητα (αναφέρεται σε 10-26% σε πολλές δημοσιεύσεις), επειδή οι ασθενείς συνήθως έχουν υποτροπή, όπου άλλοι παράγοντες μπορούν να συμβάλουν σε αυτήν την αντίδραση.
Οι υπολοιποι:
Μετά τη θεραπεία με κυτταραμπίνη, έχουν αναφερθεί καρδιομυοπάθεια και ραβδομυόλυση. Αναφέρθηκε ένα περιστατικό αναφυλαξίας που οδήγησε σε καρδιοπνευμονική ανακοπή που απαιτούσε ανάνηψη. Αυτό το συμβάν εμφανίστηκε αμέσως μετά την ενδοφλέβια χορήγηση κυταραμπίνης.
Οι γαστρεντερικές παρενέργειες μειώνονται εάν η κυταραβίνη χορηγηθεί ως έγχυση. Συνιστάται η χρήση τοπικών γλυκοκορτικοειδών ως προφύλαξη από αιμορραγική επιπεφυκίτιδα.
Αμηνόρροια και αζωοσπερμία (βλ. Παράγραφο 4.6)
Δεν συνιστάται ενδορραχιαία χρήση της κυταραβίνης. Ωστόσο, έχουν αναφερθεί οι ακόλουθες ανεπιθύμητες ενέργειες με αυτόν τον τύπο χρήσης. Αναμενόμενες συστηματικές αντιδράσεις: μυελοκαταστολή, ναυτία, έμετος. Περιστασιακά, έχει αναφερθεί σοβαρή μυελοτοξικότητα ακόμη και με τετραπληγία και παράλυση, νεκρωτική εγκεφαλοπάθεια, τύφλωση και άλλες μεμονωμένες νευροτοξικότητες.
Αναφορά υποψίας ανεπιθύμητων ενεργειών
Η αναφορά ύποπτων ανεπιθύμητων ενεργειών που εμφανίζονται μετά την έγκριση του φαρμακευτικού προϊόντος είναι σημαντική, καθώς επιτρέπει τη συνεχή παρακολούθηση της σχέσης οφέλους / κινδύνου του φαρμακευτικού προϊόντος.
Οι επαγγελματίες υγείας καλούνται να αναφέρουν τυχόν υποψίες ανεπιθύμητων ενεργειών μέσω του συστήματος αναφοράς στη διεύθυνση: http://www.agenziafarmaco.gov.it/it/ υπεύθυνοι.
04,9 Υπερδοσολογία
Χωρίς συγκεκριμένο αντίδοτο. Οι συμβουλές για τη διαχείριση σε περίπτωση υπερδοσολογίας περιλαμβάνουν: διακοπή της θεραπείας, στη συνέχεια θεραπεία της προκύπτουσας μυελοκαταστολής που περιλαμβάνει μεταγγίσεις ολικού αίματος ή αιμοπεταλίων και, εάν απαιτείται, αντιβιοτικά. Μια δόση 4,5 g / m2 με ενδοφλέβια έγχυση χορηγούμενη πάνω από μία ώρα κάθε 12 ώρες για 12 φορές προκαλεί μη αναστρέψιμη και θανατηφόρα τοξικότητα από το κεντρικό νευρικό σύστημα.
Η κυταραβίνη μπορεί να αποβληθεί με αιμοκάθαρση.
05.0 ΦΑΡΜΑΚΟΛΟΓΙΚΕΣ ΙΔΙΟΤΗΤΕΣ
05.1 Φαρμακοδυναμικές ιδιότητες
Φαρμακοθεραπευτική ομάδα: Ανάλογο πυριμιδίνης
Κωδικός ATC: L01BC01
Η κυταραβίνη, ένα νουκλεοτιδικό ανάλογο της πυριμιδίνης, είναι ένας αντινεοπλαστικός παράγοντας, ο οποίος αναστέλλει τη σύνθεση δεοξυριβονουκλεϊκού οξέος, ιδιαίτερα στη φάση S του κυτταρικού κύκλου. Διαθέτει επίσης αντιιικές και ανοσοκατασταλτικές ιδιότητες. Λεπτομερείς μελέτες για τον μηχανισμό της κυτταροτοξικότητας. in vitro υποδηλώνουν ότι η πρωταρχική δράση της κυταραβίνης είναι η αναστολή της σύνθεσης της δεοξυκυτιδίνης μέσω του ενεργού μεταβολίτη τριφωσφορικού της, της αραβινοφουρανοζυλοτριφωσφορικής κυτταροσίνης ARA-CTP, αν και πιθανώς η αναστολή των κυτιδυλοκινασών και η ενσωμάτωση της ένωσης σε νουκλεϊκά οξέα παίζει επίσης ρόλο. τις κυτταροστατικές και κυτοκτόνες δράσεις του.
Τα σχήματα υψηλής δόσης κυταραβίνης μπορούν να ξεπεράσουν την αντίσταση των κυττάρων λευχαιμίας που δεν ανταποκρίνονται πλέον στις συμβατικές δόσεις. Διάφοροι μηχανισμοί φαίνεται να εμπλέκονται σε αυτήν την αντίσταση:
Αύξηση της ποσότητας του υποστρώματος
Αύξηση στην ενδοκυτταρική ομάδα του ARA-CTP, αφού το c "είναι ένας θετικός συσχετισμός μεταξύ της κυτταρικής κατακράτησης του ARA-CTP και του ποσοστού των κυττάρων της φάσης S.
05.2 Φαρμακοκινητικές ιδιότητες
Η κυταραβίνη αποαμινώνεται σε αραβινοφουρανοσιλουρακίλη στο ήπαρ και στα νεφρά. Μετά από ενδοφλέβια χορήγηση σε ανθρώπους, μόνο το 5,8% των χορηγούμενων δόσεων απεκκρίνεται αναλλοίωτη στα ούρα εντός 12-24 ωρών, ενώ το 90% της δόσης απεκκρίνεται ως το αποαμινωμένο ανενεργό προϊόν, ουρακίλη αραβινοφουρανοσίλη (ARA-U). Η κυταραβίνη μεταβολίζεται, κυρίως από το ήπαρ και πιθανώς το νεφρό. Μετά από χορήγηση εφάπαξ υψηλών δόσεων ενδοφλεβίως, τα επίπεδα στο πλάσμα μειώνονται σε μη ανιχνεύσιμα επίπεδα εντός 15 λεπτών στους περισσότερους ασθενείς. Σε μερικούς ασθενείς υπάρχει αποδεδειγμένο κυκλοφορούν φάρμακο ήδη 5 λεπτά μετά την ένεση. Ο χρόνος ημίσειας ζωής του φαρμάκου είναι 10 λεπτά.
Η υψηλή δόση κυταραμπίνης επιτυγχάνει τα ανώτατα επίπεδα πλάσματος 200 φορές υψηλότερα από αυτά που παρατηρούνται με το συμβατικό δοσολογικό σχήμα. Η κορυφή του ανενεργού μεταβολίτη ARA-U, με το σχήμα υψηλής δόσης, παρατηρήθηκε μετά από μόλις 15 λεπτά. Η νεφρική κάθαρση είναι πιο αργή με υψηλή δόση κυταραμπίνης από ό, τι με συμβατική δόση κυταραμπίνης. Τα επίπεδα που επιτυγχάνονται στο εγκεφαλονωτιαίο υγρό (ΕΝΥ) μετά από ενδοφλέβια έγχυση υψηλών δόσεων 1-3 g / m2 κυταραβίνης είναι περίπου 100-300 νανογραμμάρια / ml.
Τα κορυφαία επίπεδα πλάσματος που επιτυγχάνονται είναι περίπου 20-60 λεπτά μετά την υποδόρια εφαρμογή και σε συγκρίσιμες δόσεις, είναι σημαντικά χαμηλότερα από τα επίπεδα στο πλάσμα που επιτυγχάνονται μετά από ενδοφλέβια χορήγηση.
05.3 Προκλινικά δεδομένα ασφάλειας
Δεν υπάρχουν προκλινικά δεδομένα σχετικά με τον συνταγογράφο που να είναι επιπρόσθετα σε αυτά που ήδη περιλαμβάνονται στις άλλες ενότητες της Περίληψης των Χαρακτηριστικών του Προϊόντος.
06.0 ΦΑΡΜΑΚΕΥΤΙΚΕΣ ΠΛΗΡΟΦΟΡΙΕΣ
06.1 Έκδοχα
Macrogol 400
Τρομεταμόλη (για ρύθμιση του pH)
Νερό για ενέσεις
06.2 Ασυμβατότητα
Ασυμβατότητα με: νάτριο καρβενικιλλίνη, νάτριο κεφαλοθίνη, θειική γενταμικίνη, ηπαρίνη νατρίου, ηλεκτρική νάτριο υδροκορτιζόνη, κανονική ινσουλίνη, μεθοτρεξάτη, 5-φθοροουρακίλη, ναφικιλίνη νάτριο, οξακιλλίνη νάτριο, ηλεκτρική ηλεκτρική πενικιλίνη νατρίου (βενζυλοπενικιλλίνη πρεδνιζολόνη)
Ωστόσο, η ασυμβατότητα εξαρτάται από διάφορους παράγοντες (π.χ. συγκεντρώσεις φαρμάκων, συγκεκριμένα διαλυτικά που χρησιμοποιούνται, pH που προκύπτει, θερμοκρασία).
Αυτό το φαρμακευτικό προϊόν δεν πρέπει να αναμειγνύεται με άλλα φαρμακευτικά προϊόντα εκτός από αυτά που αναφέρονται στην παράγραφο 6.6.
06.3 Περίοδος ισχύος
2 χρόνια
Σταθερότητα κατά τη χρήση:
Φυσικοχημική σταθερότητα κατά τη χρήση έχει αποδειχθεί σε ενέσιμο διάλυμα χλωριούχου νατρίου (0,9% β / ο) και δεξτρόζης (5% β / ο) για έως και 24 ώρες σε θερμοκρασίες κάτω των 25 ° C και έως 72 ώρες σε θερμοκρασία από 2 έως 8 ° C
Από μικροβιολογική άποψη, το προϊόν πρέπει να χρησιμοποιείται αμέσως. Εάν δεν χρησιμοποιηθεί αμέσως, οι χρόνοι και οι συνθήκες αποθήκευσης πριν από τη χρήση είναι ευθύνη του χρήστη και κανονικά δεν θα υπερβαίνουν τις 24 ώρες στους 2 έως 8 ° C, εκτός εάν έχει γίνει αραίωση σε συνθήκες άσηπτης ελεγχόμενης και επικυρωμένης.
06.4 Ειδικές προφυλάξεις κατά την αποθήκευση
Μην φυλάσσετε σε θερμοκρασία μεγαλύτερη των 25 ° C.
Μην ψύχετε ή παγώνετε.
Για τις συνθήκες αποθήκευσης του αραιωμένου φαρμακευτικού προϊόντος, βλέπε παράγραφο 6.3.
06.5 Φύση της άμεσης συσκευασίας και περιεχόμενο της συσκευασίας
Για 1 ml,
Το ενέσιμο διάλυμα περιέχεται σε ένα διαφανές γυάλινο φιαλίδιο τύπου 2 των 2 ml, κλειστό με γκρι ελαστικό πώμα 13 mm και αποσπώμενη στεγανοποίηση αλουμινίου από διαφανές μπλε ή γαλάζιο μπλε χρώμα.
Για 5 ml,
Το ενέσιμο διάλυμα περιέχεται σε ένα διαυγές σωληνωτό γυάλινο φιαλίδιο των 5 ml, κλειστό με γκρι ελαστικό πώμα 20 mm και διαφανή μπλε ή μπλε ή γαλάζιο απόχρωση αλουμινίου.
Για 10 ml,
Το ενέσιμο διάλυμα περιέχεται σε σωληνοειδές γυάλινο φιαλίδιο τύπου 10 των 10 ml, κλειστό με γκρι ελαστικό πώμα 20 mm και 20 mm διαφανές μπλε ή μπλε-γαλάζιο σφραγιστικό αλουμινίου.
Για 20 ml,
Το ενέσιμο διάλυμα περιέχεται σε φιαλίδιο διαυγούς γυαλιού τύπου I των 20 ml κλειστό με γκρι ελαστικό πώμα 20 mm και μπλε-μπλε απόχρωση αλουμινίου 20 mm.
Για 40 ml,
Το ενέσιμο διάλυμα περιέχεται σε διαφανές γυάλινο φιαλίδιο τύπου 50 των 50 ml κλειστό με γκρι ελαστικό πώμα 20 mm και μπλε-μπλε απόχρωση αλουμινίου 20 mm.
Για 50 ml,
Το ενέσιμο διάλυμα περιέχεται σε ένα διαφανές γυάλινο φιαλίδιο Τύπου Ι των 50 ml, κλειστό με γκρι ελαστικό πώμα 20 mm και αποσπώμενη σφραγίδα ιώδους αλουμινίου 20 mm.
Μεγέθη συσκευασίας
1 φιαλίδιο του 1 ml, 5 φιαλίδια του 1 ml
1 φιαλίδιο των 5 ml, 5 φιαλίδια των 5 ml
1 φιαλίδιο των 10 ml
1 φιαλίδιο των 20 ml
1 φιαλίδιο των 40 ml
1 φιαλίδιο των 50 ml
Μπορεί να μην κυκλοφορούν όλες οι συσκευασίες.
06.6 Οδηγίες χρήσης και χειρισμού
Μόνο για μία χρήση.
Εάν το διάλυμα φαίνεται αποχρωματισμένο ή περιέχει ορατά σωματίδια, θα πρέπει να απορριφθεί.
Μόλις ανοίξει, το περιεχόμενο κάθε φιαλιδίου πρέπει να χρησιμοποιηθεί αμέσως. Πετάξτε το αχρησιμοποίητο προϊόν.
Τα συχνά χρησιμοποιούμενα υγρά έγχυσης για την κυταραβίνη (βλ. Παράγραφο 6.3) είναι ενέσιμο νερό, 0,9% β / ο φυσιολογικό ορό ή 5% β / ο δεξτρόζη. Η ενέσιμη κυταραβίνη δεν πρέπει να αναμειγνύεται με άλλα φαρμακευτικά προϊόντα εκτός από αυτά που αναφέρονται στην παράγραφο 6.6.
Οδηγίες για τον χειρισμό των κυτταροτοξικών
Διαχείριση:
Θα πρέπει να χορηγείται από ή υπό την άμεση επίβλεψη ειδικευμένου ιατρού με εμπειρία στη χρήση χημειοθεραπευτικών παραγόντων για τον καρκίνο.
Παρασκευή:
• Οι χημειοθεραπευτικοί παράγοντες θα πρέπει να προετοιμάζονται για χορήγηση μόνο από επαγγελματίες εκπαιδευμένους στην ασφαλή χρήση του σκευάσματος.
• Λειτουργίες όπως αραίωση και μεταφορά στη σύριγγα πρέπει να γίνονται μόνο στην κατάλληλη περιοχή.
• Το προσωπικό που εκτελεί αυτές τις διαδικασίες πρέπει να προστατεύεται επαρκώς με ρόμπες, γάντια και γυαλιά.
• Συνιστάται στο έγκυο προσωπικό να μην χειρίζεται φάρμακα χημειοθεραπείας.
Απόρριψη και μόλυνση:
Το προϊόν ή τυχόν αχρησιμοποίητα απόβλητα πρέπει να απορρίπτονται σύμφωνα με τους τοπικούς κανονισμούς.
Για καταστροφή, τοποθετήστε σε σακούλα / δοχείο διάθεσης απορριμμάτων υψηλού κινδύνου (για κυτταροτοξικά) και αποτέφρωση στους 1100oC.
Σε περίπτωση διασποράς, περιορίστε την πρόσβαση στην πληγείσα περιοχή και φορέστε κατάλληλο προστατευτικό εξοπλισμό, συμπεριλαμβανομένων γαντιών και γυαλιών ασφαλείας. Περιορίστε την εξάπλωση και καθαρίστε την περιοχή με χαρτί / απορροφητικό υλικό. Οι διασπορές μπορούν επίσης να αντιμετωπιστούν με 5% υποχλωριώδες νάτριο. Η περιοχή διασποράς θα πρέπει να καθαριστεί με άφθονο νερό. Τοποθετήστε το μολυσμένο υλικό σε μια σακούλα. / Στεγανό δοχείο για την απόρριψη των κυτοτοξικών και την αποτέφρωση στους 1100 ° C
07.0 ΚΑΤΟΧΟΣ ΑΔΕΙΑΣ ΜΑΡΚΕΤΙΝΓΚ
Accord Healthcare Limited,
Sage House, 319 Pinner Road,
North Harrow,
Middlesex, HA1 4HF,
Ηνωμένο Βασίλειο
08.0 ΑΡΙΘΜΟΣ ΑΔΕΙΑΣ ΜΑΡΚΕΤΙΝΓΚ
"100 mg / ml ενέσιμο διάλυμα ή έγχυση", 1 γυάλινο φιαλίδιο 1 ml - Αριθμός AIC: 042356016
"100 mg / ml ενέσιμο διάλυμα ή έγχυση", 5 γυάλινα φιαλίδια του 1 ml - Αριθμός AIC: 042356028
"100 mg / ml ενέσιμο διάλυμα ή έγχυση", 1 γυάλινο φιαλίδιο των 5 ml - αρ. AIC: 042356030
"100 mg / ml ενέσιμο διάλυμα ή έγχυση", 5 γυάλινα φιαλίδια των 5 ml - Αριθμός AIC: 042356042
"100 mg / ml ενέσιμο διάλυμα ή έγχυση", 1 γυάλινο φιαλίδιο των 10 ml - Αριθμός AIC: 042356055
"100 mg / ml ενέσιμο διάλυμα ή έγχυση", 1 γυάλινο φιαλίδιο των 20 ml - Αριθμός AIC: 042356067
"100 mg / ml ενέσιμο διάλυμα ή έγχυση", 1 γυάλινο φιαλίδιο των 40 ml - Αριθμός AIC: 042356079
"100 mg / ml ενέσιμο διάλυμα ή έγχυση", 1 γυάλινο φιαλίδιο των 50 ml - Αριθμός AIC: 042356081
09.0 ΗΜΕΡΟΜΗΝΙΑ ΠΡΩΤΗΣ ΕΓΚΡΙΣΗΣ ΑΝΑΝΕΩΣΗΣ ΤΗΣ ΑΔΕΙΑΣ
Ημερομηνία πρώτης έγκρισης: 24 Ιουλίου 2013
10.0 ΗΜΕΡΟΜΗΝΙΑ ΑΝΑΘΕΩΡΗΣΗΣ ΤΟΥ ΚΕΙΜΕΝΟΥ
Φεβρουάριος 2016