Ορισμένα χαρακτηριστικά του Huntington μπορούν να διαχειριστούν με:
- Η λογοθεραπεία, η ψυχοθεραπεία και η γνωστική αποκατάσταση μπορούν να βελτιώσουν τόσο τα σωματικά όσο και τα ψυχολογικά συμπτώματα της νόσου. Συγκεκριμένα, αυτές οι θεραπείες είναι χρήσιμες για την επικοινωνία και την αυτόνομη εκτέλεση καθημερινών δραστηριοτήτων. Η καλύτερη κατανόηση των συμπεριφορικών και γνωστικών διαταραχών μπορεί επίσης να βοηθήσει στην ανάπτυξη στρατηγικών προσαρμογής στις αλλαγές που προκαλούνται από την πρόοδο της νόσου του Χάντινγκτον.
- Φυσικοθεραπεία και τακτική άσκηση: συμβάλλουν στη διατήρηση του συντονισμού της κίνησης. Στα αρχικά στάδια της νόσου συνιστάται ήπια σωματική δραστηριότητα (κολύμπι, περπάτημα κ.λπ.).
- Χρήση ειδικών βοηθημάτων για να βοηθήσουν τους ασθενείς με νόσο του Huntington, που αντιμετωπίζουν δυσκολίες συντονισμού, να περπατήσουν ανεξάρτητα.
- Φάρμακα: Ενδείκνυνται όταν εμφανίζονται σημαντικά συμπτώματα. Για παράδειγμα, η χορεία και η διέγερση μπορούν να κατασταλούν μερικώς με φάρμακα που εμποδίζουν ή καταστρέφουν τους υποδοχείς ντοπαμίνης. Ωστόσο, πολλά φάρμακα μπορούν να προκαλέσουν παρενέργειες, καθώς και να έχουν διαφορετικές επιδράσεις σε διαφορετικούς ασθενείς. Επομένως, θα πρέπει να δημιουργηθεί η ιδανική ισορροπία. κατά περίπτωση από τον ειδικό γιατρό, με βάση τα συμπτώματα και την ατομική ανταπόκριση στις θεραπείες.
, στη θεραπεία της νόσου του Χάντινγκτον. Η κλινική φάση είναι πολύ απαιτητική, κυρίως επειδή η ασθένεια έχει αργή εξέλιξη και "μεγάλη κλινική ετερογένεια. Υπάρχουν κλίμακες αξιολόγησης της νόσου του Huntington και είναι σχεδόν ίδιες σε όλες τις κλινικές. Η πλήρης διείσδυση της νόσου και η διαθεσιμότητα προγνωστική γενετική, προσφέρει την ευκαιρία να επιχειρηθεί θεραπεία κατά τα αρχικά στάδια της νόσου. Επί του παρόντος, οι μελέτες στοχεύουν στην αναζήτηση ευαίσθητων και σταθερών βιοδεικτών αλλαγής, προκειμένου να παρέμβουν στις πρώτες εκδηλώσεις της νόσου.
Επί του παρόντος, οι τεχνικές νευροαπεικόνισης έχουν προσφέρει τους καλύτερους βιοδείκτες κατά την προδρομική φάση (που προηγείται των κλινικών συμπτωμάτων της νόσου). Επιπλέον, παρέχουν συσχέτιση μεταξύ των θεραπειών που διεξάγονται σε ζωικά μοντέλα και σε ανθρώπους.
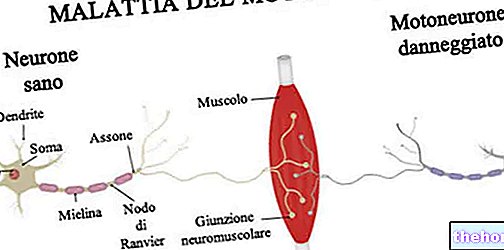
Όπως αναφέρθηκε, η ατροφία του ραβδωτού σώματος είναι πρώιμη και εξελίσσεται κατά τη διάρκεια της νόσου. Άλλες περιοχές του εγκεφάλου όπως οι υποφλοιώδεις και φλοιώδεις δομές λευκής ύλης έχουν επίσης αποδειχθεί ότι επηρεάζονται στην προδρομική περίοδο.
Μέσω της λειτουργικής απεικόνισης μπορεί επίσης να εντοπίσει ορισμένες ανωμαλίες σε άτομα κατά την προδρομική περίοδο. Αυτή η τεχνική μπορεί επίσης να είναι αρκετά ευαίσθητη για να εντοπίσει ανιχνεύσιμες ανωμαλίες δομής ή αλλαγές στη συμπεριφορά.
Τέλος, η ταυτοποίηση μοριακών βιοδεικτών, όπως γαλακτικό ή άλλα προϊόντα κυτταρικού στρες, θα μπορούσε να καταστεί δυνατή χάρη στις τεχνικές φασματοσκοπίας μαγνητικού συντονισμού.
ο εκλεκτικός εκφυλισμός των νευρώνων στη νόσο του Huntington δεν έχει ακόμη διευκρινιστεί πλήρως. Συνεπώς, υπάρχει ανάγκη διερεύνησης πιθανών νέων θεραπευτικών στρατηγικών. Συγκεκριμένα, έχει διαπιστωθεί ότι στη νόσο του Huntington υπάρχει εκλεκτική απώλεια υποδοχέων κανναβινοειδών τύπου CB1 στα βασικά γάγγλια, η οποία αντιπροσωπεύει μία από τις πρώτες νευροχημικές αλλοιώσεις. Για το λόγο αυτό, ερευνητικές μελέτες ερευνούν αυτήν τη στιγμή τον νευροπροστατευτικό ρόλο των κανναβινοειδών στη νόσο του Χάντινγκτον.
Για περισσότερες πληροφορίες: Κανναβινοειδείς υποδοχείςΝόσος του Huntington: υποδοχείς CB1
Η εμπλοκή του ενδοκανναβινοειδούς συστήματος, ιδιαίτερα των υποδοχέων CB1, στη νόσο του Huntington έχει υποβληθεί εδώ και καιρό. Πράγματι, έχει αποδειχθεί ότι μία από τις πρώτες εμφανείς αλλαγές σε άτομα που επηρεάζονται από τη νόσο είναι η εκλεκτική απώλεια υποδοχέων CB1 στους βασικούς πυρήνες. Αυτή η απώλεια υποδοχέα προηγείται της έναρξης της νευροπαθολογίας του ραβδωτού σώματος. Σε διαγονιδιακά ζωικά μοντέλα για τη νόσο του Huntington είναι Παρατηρήθηκε αλλαγή τόσο στην έκφραση του υποδοχέα CB1 όσο και στα επίπεδα των ενδοκανναβινοειδών. Αυτά τα στοιχεία οδήγησαν στην υπόθεση ότι μια δυσρύθμιση του ενδοκανναβινοειδούς συστήματος θα μπορούσε να αντιπροσωπεύει έναν στόχο για την ανάπτυξη νέων θεραπευτικών στρατηγικών.
Σε πολύ πρόσφατες μελέτες έχει αποδειχθεί ότι η διαγραφή των υποδοχέων CB1 σε διαγονιδιακά μοντέλα για τη νόσο του Huntington οδήγησε σε επιδείνωση του κινητικού φαινοτύπου, σε "ατροφία του ραβδωτού σώματος και συσσώρευση της πρωτεΐνης huntingtin, ενώ έγινε χρόνια θεραπεία με αγωνιστή κάνναβης". , τετραϋδροκαννιμπόλη (Δ9-THC), ήταν ευεργετική.
Τέλος, οι υποδοχείς CB1 εκφράζονται ιδιαίτερα στους GABAergic νευρώνες, οι οποίοι αποτελούν το 90-95% των νευρώνων στο ραβδωτό σώμα, την περιοχή του εγκεφάλου που επηρεάζεται από τη νόσο του Huntington, όπως εξηγείται στις προηγούμενες παραγράφους.
Η διέγερση των υποδοχέων CB1 οδηγεί σε μείωση της απελευθέρωσης του ανασταλτικού νευροδιαβιβαστή GABA. Αυτή η μείωση θα μπορούσε να είναι επιβλαβής για τους ασθενείς που επηρεάζονται από τη νόσο του Huntington, δεδομένου ότι με τη μείωση του ανασταλτικού τόνου που ασκείται από το GABA, θα υπάρξει υπερβολική αύξηση του τόνου διέγερσης, που καθορίζεται από το γλουταμινικό, και κατά συνέπεια στο φαινόμενο της διεγερτοτοξικότητας. Η διεγερτοτοξικότητα πιστεύεται ότι συμβάλλει στον θάνατο των νευρώνων προβολής στο ραβδωτό σώμα. Ωστόσο, οι υποδοχείς CB1 βρίσκονται επίσης σε νευρώνες γλουταμινικού, αν και σε μικρότερο βαθμό. Έχει υποτεθεί ότι η διέγερση αυτών των υποδοχέων θα οδηγούσε επίσης σε χαμηλότερη απελευθέρωση γλουταμικού Το γεγονός ότι η χρόνια θεραπεία με Δ9-THC ήταν ευεργετική υποδηλώνει ότι η συμβολή των υποδοχέων CB1 στη διαμεσολάβηση της απόκρισης στους αγωνιστές κανναβινοειδών σε συγκεκριμένους νευρώνες μπορεί να αλλάξει στην εξέλιξη της νόσου.
Μελλοντικές προοπτικές
Προς το παρόν, η αναζήτηση θεραπείας για τη νόσο του Huntington είναι ενεργή και πολλές κλινικές δοκιμές βρίσκονται σε εξέλιξη για την αξιολόγηση της αποτελεσματικότητας διαφόρων φαρμακολογικών παραγόντων και / ή μη φαρμακολογικών προσεγγίσεων (π.χ. γονιδιακή θεραπεία, μεταμόσχευση βλαστικών κυττάρων) ικανές να μειώσουν την παραγωγή κυνηγιού ή να βελτιώσει την επιβίωση των νευρώνων, να αποτρέψει ή να επιβραδύνει την εξέλιξη της νόσου.
Για παράδειγμα, σίγαση γονιδίων χρησιμοποιώντας παρεμβολή RNA (RNAi) ή αντιπληροφοριακά ολιγονουκλεοτίδια (ASO). Οι ASO δεσμεύονται, ειδικότερα, με το "αγγελιοφόρο RNA που μεταφέρει πληροφορίες" από το μεταλλαγμένο γονίδιο, εμποδίζει τη μετάφρασή του και διεγείρει την υποβάθμισή του, έτσι ώστε να μην παράγεται η πρωτεΐνη κυνηγιντίνης. Η θεραπεία με βλαστοκύτταρα, από την άλλη πλευρά, συνίσταται στην αντικατάσταση κατεστραμμένων νευρώνων, χάρη στη μεταμόσχευση βλαστικών κυττάρων, στις πληγείσες περιοχές του εγκεφάλου. Δοκιμές σε ζωικά μοντέλα και σε προκαταρκτικές κλινικές δοκιμές έδωσαν αντικρουόμενα αποτελέσματα με αυτήν την τεχνική, επομένως χρειάζονται περαιτέρω στοιχεία για να διαπιστωθεί η αποτελεσματικότητά της.
Βιβλιογραφία
- Caron, N.S., Wright, G.E.B. & Hayden, M.R. Ασθένεια Huntington. GeneReviews ((R)) ασθένεια Huntington. Σιάτλ (WA), 2018.
- Neurobiol Dis. 2012 Μαρ. 45: 983-91. doi: 10.1016 / j.nbd.2011.12.017. Epub 2011 Δεκεμβρίου 23. Ανισορροπία των υποδοχέων CB1 που εκφράζεται σε GABAergic και γλουταμετρικούς νευρώνες σε ένα διαγονιδιακό μοντέλο ποντικού της νόσου του Huntington. Chiodi V, Uchigashima M, Beggiato S, Ferrante A, Armida M, Martire A, Potenza RL, Ferraro L, Tanganelli S, Watanabe M, Domenici MR, Popoli P.