Ενεργά συστατικά: παλιπεριδόνη
XEPLION 25 mg ενέσιμο εναιώρημα παρατεταμένης αποδέσμευσης
XEPLION 50 mg ενέσιμο εναιώρημα παρατεταμένης αποδέσμευσης
XEPLION 75 mg ενέσιμο εναιώρημα παρατεταμένης αποδέσμευσης
XEPLION 100 mg ενέσιμο εναιώρημα παρατεταμένης αποδέσμευσης
XEPLION 150 mg ενέσιμο εναιώρημα παρατεταμένης αποδέσμευσης
Ενδείξεις Γιατί χρησιμοποιείται το Xeplion; Σε τι χρησιμεύει;
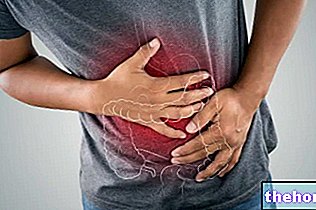
Το Xeplion περιέχει τη δραστική ουσία παλιπεριδόνη, η οποία ανήκει στην κατηγορία των αντιψυχωσικών φαρμάκων και χρησιμοποιείται ως θεραπεία συντήρησης για τα συμπτώματα της σχιζοφρένειας σε ενήλικες ασθενείς που έχουν σταθεροποιηθεί σε παλιπεριδόνη ή ρισπεριδόνη.
Εάν έχετε δείξει ότι ανταποκρίνεστε παλιπεριδόνη ή ρισπεριδόνη στο παρελθόν και έχετε ήπια έως μέτρια συμπτώματα, ο γιατρός σας μπορεί να ξεκινήσει θεραπεία με Xeplion χωρίς προηγούμενη σταθεροποίηση με παλιπεριδόνη ή ρισπεριδόνη.
Η σχιζοφρένεια είναι μια ασθένεια που χαρακτηρίζεται από «θετικά» και «αρνητικά» συμπτώματα. Θετικό σημαίνει περίσσεια συμπτωμάτων που δεν υπάρχουν κανονικά. Για παράδειγμα, ένα άτομο με σχιζοφρένεια μπορεί να ακούει φωνές ή να βλέπει πράγματα που δεν υπάρχουν στην πραγματικότητα (που ονομάζονται παραισθήσεις), να πιστεύει πράγματα που δεν είναι αληθινά (που ονομάζονται αυταπάτες) ή να είναι ασυνήθιστα καχύποπτα για τους άλλους. Τα αρνητικά συμπτώματα σημαίνουν έλλειψη συμπεριφορών ή συναισθημάτων που είναι φυσιολογικά παρόντα. Για παράδειγμα, ένα άτομο με σχιζοφρένεια μπορεί να έχει την τάση να απομονώνεται και να μην αντιδρά συναισθηματικά ή να δυσκολεύεται να μιλήσει καθαρά και λογικά. Τα άτομα με αυτή τη διαταραχή μπορεί επίσης να αισθάνονται κατάθλιψη, άγχος, ενοχή ή ένταση.
Το Xeplion μπορεί να βοηθήσει στην ανακούφιση των συμπτωμάτων της ασθένειάς σας και να αποτρέψει την επανεμφάνισή τους.
Αντενδείξεις Όταν το Xeplion δεν πρέπει να χρησιμοποιείται
Μην χρησιμοποιείτε το Xeplion
- εάν είστε αλλεργικοί στην παλιπεριδόνη ή σε οποιοδήποτε άλλο συστατικό αυτού του φαρμάκου (αναφέρονται στην παράγραφο 6).
- εάν είστε αλλεργικοί σε άλλο αντιψυχωσικό φάρμακο, συμπεριλαμβανομένης της ρισπεριδόνης.
Προφυλάξεις κατά τη χρήση Τι πρέπει να γνωρίζετε πριν πάρετε το Xeplion
Μιλήστε με τον γιατρό, τον φαρμακοποιό ή τον νοσοκόμο σας πριν χρησιμοποιήσετε το Xeplion. Αυτό το φάρμακο δεν έχει μελετηθεί σε ηλικιωμένους ασθενείς με άνοια. Ωστόσο, οι ηλικιωμένοι ασθενείς με άνοια που λαμβάνουν άλλα φάρμακα παρόμοιου τύπου μπορεί να έχουν αυξημένο κίνδυνο εγκεφαλικού επεισοδίου ή θανάτου (βλ. Παράγραφο 4, πιθανές παρενέργειες).
Όλα τα φάρμακα έχουν παρενέργειες και μερικές από τις παρενέργειες αυτού του φαρμάκου μπορεί να επιδεινώσουν τα συμπτώματα άλλων ιατρικών καταστάσεων. Για το λόγο αυτό, είναι σημαντικό να συζητήσετε με το γιατρό σας οποιαδήποτε από τις ακόλουθες καταστάσεις, οι οποίες ενδέχεται να επιδεινωθούν κατά τη διάρκεια της θεραπείας με αυτό το φάρμακο.
- Εάν έχετε νόσο Πάρκινσον.
- Εάν έχετε διαγνωστεί ποτέ με μια ασθένεια της οποίας τα συμπτώματα περιλαμβάνουν υψηλή θερμοκρασία και μυϊκή δυσκαμψία (γνωστό και ως νευροληπτικό κακόηθες σύνδρομο).
- Εάν είχατε ποτέ ανώμαλες κινήσεις της γλώσσας ή του προσώπου (Όψιμη Δυσκινησία).
- Εάν γνωρίζετε ότι είχατε χαμηλά επίπεδα λευκών αιμοσφαιρίων στο παρελθόν (τα οποία μπορεί να οφείλονται ή όχι σε άλλα φάρμακα).
- Εάν είστε διαβητικός ή έχετε προδιάθεση για διαβήτη.
- Εάν έχετε διαγνωστεί με καρκίνο του μαστού ή όγκο της υπόφυσης στον εγκέφαλο.
- Εάν έχετε καρδιακή νόσο ή λαμβάνετε θεραπεία για καρδιακή νόσο που τείνει να μειώσει την αρτηριακή σας πίεση.
- Εάν έχετε χαμηλή αρτηριακή πίεση όταν σηκώνεστε όρθιοι ή ξαφνικά μεταβείτε από το ψέμα στο καθιστό.
- Εάν πάσχετε από επιληψία.
- Εάν έχετε νεφρικά προβλήματα.
- Εάν έχετε ηπατικά προβλήματα.
- Εάν έχετε παρατεταμένη και / ή επώδυνη στύση.
- Εάν δυσκολεύεστε να ελέγξετε τη βασική θερμοκρασία του σώματος ή τις υπερβολικές συνθήκες θερμότητας.
- Εάν έχετε ασυνήθιστα υψηλό επίπεδο ορμόνης προλακτίνης στο αίμα σας ή εάν έχετε πιθανό όγκο εξαρτώμενο από την προλακτίνη.
- Εάν εσείς ή κάποιος άλλος στην οικογένειά σας έχετε ιστορικό θρόμβων αίματος (θρόμβοι), καθώς τα αντιψυχωσικά έχουν συσχετιστεί με το σχηματισμό θρόμβων αίματος.
Εάν έχετε οποιαδήποτε από αυτές τις καταστάσεις, μιλήστε με το γιατρό σας ώστε να μπορεί να εκτιμήσει εάν πρέπει να προσαρμόσετε τη δόση σας ή να την ακολουθήσετε προσεκτικά για λίγο.
Δεδομένου ότι επικίνδυνα χαμηλοί αριθμοί συγκεκριμένου τύπου λευκών αιμοσφαιρίων που απαιτούνται για τη διακοπή λοιμώξεων στο αίμα έχουν παρατηρηθεί πολύ σπάνια σε ασθενείς που λαμβάνουν αυτό το φάρμακο, ο γιατρός σας μπορεί να ελέγξει τον αριθμό των λευκών αιμοσφαιρίων σας.
Παρόλο που ανεχτήκατε προηγουμένως από του στόματος παλιπεριδόνη ή από του στόματος ρισπεριδόνη, σπάνια εμφανίζονται αλλεργικές αντιδράσεις μετά τη λήψη ενέσεων Xeplion. Επισκεφθείτε το γιατρό σας αμέσως εάν εμφανίσετε εξάνθημα, πρήξιμο στο λαιμό, κνησμό ή προβλήματα αναπνοής, καθώς αυτά μπορεί να είναι σημάδια σοβαρής αλλεργικής αντίδρασης.
Αυτό το φάρμακο μπορεί να προκαλέσει αύξηση βάρους. Η σημαντική αύξηση βάρους μπορεί να επηρεάσει αρνητικά την υγεία. Ο γιατρός σας πρέπει να σας ζυγίζει τακτικά.
Δεδομένου ότι έχει παρατηρηθεί σακχαρώδης διαβήτης ή επιδείνωση προϋπάρχοντος σακχαρώδους διαβήτη σε ασθενείς που λαμβάνουν αυτό το φάρμακο, ο γιατρός σας θα πρέπει να ελέγξει για υψηλά επίπεδα σακχάρου στο αίμα. Σε ασθενείς με προϋπάρχον σακχαρώδη διαβήτη, το επίπεδο γλυκόζης στο αίμα πρέπει να παρακολουθείται τακτικά.
Δεδομένου ότι αυτό το φάρμακο μπορεί να μειώσει την επιθυμία για εμετό, υπάρχει πιθανότητα να καλύψει τη φυσιολογική απάντηση του σώματος στην κατάποση τοξικών ουσιών ή άλλες ιατρικές καταστάσεις.
Κατά τη διάρκεια μιας «χειρουργικής επέμβασης στα μάτια» λόγω θόλωσης του φακού (καταρράκτης), η κόρη (ο μαύρος κύκλος στο κέντρο του ματιού σας) ενδέχεται να μην αυξηθεί σε μέγεθος, όπως απαιτείται. Επίσης, η ίριδα (το έγχρωμο τμήμα του ματιού) μπορεί να γίνει ξεφτίλα κατά τη διάρκεια της χειρουργικής επέμβασης, το οποίο μπορεί να προκαλέσει βλάβη στο μάτι. Εάν σχεδιάζετε να κάνετε χειρουργική επέμβαση στα μάτια, φροντίστε να ενημερώσετε τον οφθαλμίατρό σας ότι παίρνετε αυτό το φάρμακο.
Παιδιά και έφηβοι
Αυτό το φάρμακο δεν πρέπει να χρησιμοποιείται σε παιδιά και εφήβους κάτω των 18 ετών.
Αλληλεπιδράσεις Ποια φάρμακα ή τρόφιμα μπορεί να αλλάξουν την επίδραση του Xeplion
Ενημερώστε το γιατρό σας εάν παίρνετε, έχετε πάρει πρόσφατα ή μπορεί να πάρετε άλλα φάρμακα.
Η λήψη αυτού του φαρμάκου με καρβαμαζεπίνη (αντιεπιληπτικό και σταθεροποιητικό διάθεσης) μπορεί να καταστήσει αναγκαία την προσαρμογή της δόσης αυτού του φαρμάκου.
Καθώς αυτό το φάρμακο δρα κυρίως στον εγκέφαλο, η παρεμβολή σε άλλα φάρμακα (ή αλκοόλ) που δρουν στον εγκέφαλο, όπως άλλα ψυχιατρικά φάρμακα, οπιούχα, αντιισταμινικά και φάρμακα για διαταραχές του ύπνου, μπορεί να προκαλέσει «υπερβολή παρενεργειών όπως υπνηλία ή άλλες επιδράσεις στον εγκέφαλο.
Καθώς αυτό το φάρμακο μπορεί να μειώσει την αρτηριακή πίεση, να είστε προσεκτικοί όταν αυτό το φάρμακο χρησιμοποιείται με άλλα φάρμακα που μειώνουν την αρτηριακή πίεση.
Αυτό το φάρμακο μπορεί να μειώσει την επίδραση των φαρμάκων που χρησιμοποιούνται για τη θεραπεία της νόσου του Πάρκινσον και του συνδρόμου ανήσυχων ποδιών (π.χ. λεβοντόπα).
Αυτό το φάρμακο μπορεί να προκαλέσει μια «ανωμαλία ηλεκτροκαρδιογραφήματος (ΗΚΓ)», η οποία χαρακτηρίζεται από μεγαλύτερη περίοδο για την εξέλιξη μιας ηλεκτρικής ώθησης σε ένα συγκεκριμένο τμήμα της καρδιάς (γνωστή ως «παράταση του διαστήματος QT»). έχουν αυτά τα αποτελέσματα περιλαμβάνουν ορισμένα φάρμακα που χρησιμοποιούνται για τη θεραπεία του καρδιακού ρυθμού ή για τη θεραπεία λοιμώξεων και άλλων αντιψυχωσικών Είναι σημαντικό να ενημερώσετε το γιατρό σας για τυχόν φάρμακα που παίρνετε για τη θεραπεία αυτών των καταστάσεων.
Εάν έχετε προδιάθεση να αναπτύξετε επιληπτικές κρίσεις, αυτό το φάρμακο μπορεί να αυξήσει την πιθανότητα εμφάνισής τους. Άλλα φάρμακα που έχουν αυτό το αποτέλεσμα περιλαμβάνουν ορισμένα φάρμακα που χρησιμοποιούνται για τη θεραπεία της κατάθλιψης ή των λοιμώξεων και άλλα αντιψυχωσικά. Είναι σημαντικό να ενημερώσετε το γιατρό σας για τυχόν φάρμακα που παίρνετε για τη θεραπεία αυτών των καταστάσεων.
Προειδοποιήσεις Είναι σημαντικό να γνωρίζετε ότι:
Εγκυμοσύνη και θηλασμός
Εάν είστε έγκυος ή θηλάζετε, νομίζετε ότι μπορεί να είστε έγκυος ή σχεδιάζετε να αποκτήσετε παιδί, ζητήστε τη συμβουλή του γιατρού ή του φαρμακοποιού σας πριν πάρετε αυτό το φάρμακο. Δεν πρέπει να χρησιμοποιείτε αυτό το φάρμακο κατά τη διάρκεια της εγκυμοσύνης, εκτός εάν το έχετε ήδη συζητήσει με το γιατρό σας. Τα ακόλουθα συμπτώματα μπορεί να εμφανιστούν σε νεογέννητα μωρά, σε μητέρες που έχουν χρησιμοποιήσει παλιπεριδόνη το τελευταίο τρίμηνο (τους τελευταίους τρεις μήνες της εγκυμοσύνης τους): τρόμο, μυϊκή δυσκαμψία και / ή αδυναμία, υπνηλία, διέγερση, αναπνευστικά προβλήματα και δυσκολία στη σίτιση. το παιδί σας έχει οποιοδήποτε από αυτά τα συμπτώματα, ίσως χρειαστεί να επικοινωνήσετε με το γιατρό σας.
Αυτό το φάρμακο μπορεί να περάσει από τη μητέρα στο μωρό μέσω του μητρικού γάλακτος και μπορεί να βλάψει το μωρό. Επομένως, μην θηλάζετε εάν χρησιμοποιείτε αυτό το φάρμακο.
Οδήγηση και χειρισμός μηχανών
Μπορεί να εμφανιστεί ζάλη, υπερβολική κόπωση και προβλήματα όρασης κατά τη διάρκεια της θεραπείας με αυτό το φάρμακο (βλ. Παράγραφο 4). Αυτό πρέπει να λαμβάνεται υπόψη σε περιπτώσεις όπου απαιτείται πλήρης επαγρύπνηση, π.χ. όταν οδηγείτε αυτοκίνητο ή χειρίζεστε μηχανήματα.
Σημαντικές πληροφορίες σχετικά με ορισμένα συστατικά του Xeplion
Το κανονικό εύρος δοσολογίας για αυτό το φαρμακευτικό προϊόν περιέχει λιγότερο από 1 mmol (23 mg) νατρίου ανά δόση. στην πράξη είναι ουσιαστικά "χωρίς νάτριο".
Δόση, μέθοδος και χρόνος χορήγησης Πώς να χρησιμοποιήσετε το Xeplion: Δοσολογία
Αυτό το φάρμακο χορηγείται από το γιατρό σας ή άλλο επαγγελματία υγείας σε ιατρείο ή κλινική. Ο γιατρός σας θα αποφασίσει πότε πρέπει να επιστρέψετε στο ιατρείο ή την κλινική για την ένεση. Είναι σημαντικό να μην παραλείψετε την προγραμματισμένη δόση σας. Εάν νομίζετε ότι δεν θα μπορείτε να παρευρεθείτε στο ραντεβού του γιατρού σας, επικοινωνήστε αμέσως μαζί του για να σας ενημερώσει για νέο ραντεβού το συντομότερο δυνατό. Θα σας χορηγηθεί μια πρώτη ένεση (150 mg) και μια δεύτερη ένεση (100 mg) αυτού του φαρμάκου στον άνω βραχίονα με απόσταση περίπου μιας εβδομάδας. Στη συνέχεια, θα λάβετε μια ένεση (η οποία μπορεί να κυμαίνεται από 25 mg έως 150 mg) ή στον άνω βραχίονα ή στον γλουτό μία φορά το μήνα.
Εάν ο γιατρός σας σας μεταφέρει από ρισπεριδόνη παρατεταμένης αποδέσμευσης σε αυτό το φάρμακο, θα λάβετε την πρώτη σας ένεση αυτού του φαρμάκου (η οποία μπορεί να κυμαίνεται από 25 mg έως 150 mg) είτε στον άνω βραχίονα είτε στον γλουτό την ημερομηνία που έχει ήδη προγραμματιστεί για την επόμενη ένεσή σας Το Στη συνέχεια, θα λάβετε μια ένεση (η οποία μπορεί να κυμαίνεται από 25 mg έως 150 mg) είτε στον άνω βραχίονα είτε στον γλουτό μία φορά το μήνα.
Ανάλογα με τα συμπτώματά σας, ο γιατρός σας μπορεί να αυξήσει ή να μειώσει την ποσότητα του φαρμάκου που λαμβάνετε τη στιγμή της προγραμματισμένης μηνιαίας ένεσης κατά ένα επίπεδο δόσης.
Ασθενείς με νεφρικά προβλήματα
Ο γιατρός σας μπορεί να προσαρμόσει τη δόση του φαρμάκου με βάση τη νεφρική σας λειτουργία. Εάν έχετε ήπια νεφρικά προβλήματα, ο γιατρός σας μπορεί να συνταγογραφήσει χαμηλότερη δόση. Εάν έχετε μέτρια έως σοβαρά νεφρικά προβλήματα, αυτό το φάρμακο δεν πρέπει να χρησιμοποιείται.
Ατομα της τρίτης ηλικίας
Ο γιατρός σας μπορεί να μειώσει τη δόση αυτού του φαρμάκου εάν μειωθεί η νεφρική σας λειτουργία.
Υπερδοσολογία Τι πρέπει να κάνετε εάν έχετε πάρει πάρα πολύ Xeplion
Εάν πάρετε μεγαλύτερη δόση Xeplion από την κανονική
Αυτό το φάρμακο θα σας χορηγηθεί υπό ιατρική επίβλεψη. επομένως είναι απίθανο να σας δοθεί πάρα πολύ.
Ασθενείς που έχουν λάβει υπερδοσολογία παλιπεριδόνης μπορεί να εμφανίσουν τα ακόλουθα συμπτώματα: υπνηλία ή νάρκωση, γρήγορους καρδιακούς παλμούς, χαμηλή αρτηριακή πίεση, μη φυσιολογικό ηλεκτροκαρδιογράφημα (ανίχνευση της ηλεκτρικής δραστηριότητας της καρδιάς) ή αργές ή ανώμαλες κινήσεις του προσώπου, του σώματος, των βραχιόνων ή πόδια.
Εάν σταματήσετε να χρησιμοποιείτε το Xeplion
Εάν σταματήσετε να παίρνετε τις ενέσεις σας, θα χάσετε τις επιδράσεις του φαρμάκου. Δεν πρέπει να σταματήσετε να χρησιμοποιείτε αυτό το φάρμακο εκτός εάν σας το πει ο γιατρός σας, καθώς τα συμπτώματά σας μπορεί να επανέλθουν.
Εάν έχετε περαιτέρω απορίες σχετικά με τη λήψη αυτού του φαρμάκου, ρωτήστε το γιατρό ή το φαρμακοποιό σας
Παρενέργειες Ποιες είναι οι παρενέργειες του Xeplion
Όπως όλα τα φάρμακα, έτσι και αυτό το φάρμακο μπορεί να προκαλέσει ανεπιθύμητες ενέργειες, αν και δεν παρουσιάζονται σε όλους τους ανθρώπους.
Ενημερώστε αμέσως το γιατρό σας εάν:
- Νομίζετε ότι έχετε θρόμβους αίματος στις φλέβες σας, ιδιαίτερα στα πόδια (τα συμπτώματα περιλαμβάνουν πρήξιμο, πόνο και ερυθρότητα στα πόδια), τα οποία μπορούν να ταξιδέψουν κατά μήκος των αιμοφόρων αγγείων στους πνεύμονες, προκαλώντας πόνο στο στήθος και δυσκολία στην αναπνοή. Εάν παρατηρήσετε κάποιο από αυτά τα συμπτώματα, συμβουλευτείτε αμέσως το γιατρό σας.
- Έχετε άνοια και παρατηρείτε μια ξαφνική αλλαγή στην ψυχική σας κατάσταση ή μια "ξαφνική αδυναμία ή μούδιασμα του προσώπου, των χεριών ή των ποδιών, ειδικά στη μία πλευρά, ή εάν η γλώσσα σας είναι ακατανόητη, έστω και για μικρό χρονικό διάστημα. Μπορεί". είναι τα σημάδια ενός εγκεφαλικού επεισοδίου.
- Έχετε πυρετό, μυϊκή δυσκαμψία, εφίδρωση ή μειωμένο επίπεδο συνείδησης (διαταραχή που ονομάζεται «νευροληπτικό κακοήθη σύνδρομο»). Μπορεί να χρειαστεί άμεση ιατρική θεραπεία.
- Είναι άνδρας και έχει παρατεταμένη ή επώδυνη στύση. Αυτή η κατάσταση ονομάζεται πριαπισμός. Μπορεί να χρειαστεί άμεση ιατρική θεραπεία.
- Έχει ακούσιες ρυθμικές κινήσεις της γλώσσας, του στόματος και του προσώπου. Μπορεί να χρειαστεί να διακόψετε την παλιπεριδόνη.
- Έχετε σοβαρή αλλεργική αντίδραση που χαρακτηρίζεται από πυρετό, πρήξιμο του στόματος, του προσώπου, των χειλιών ή της γλώσσας, δύσπνοια, κνησμό, δερματικό εξάνθημα και μερικές φορές πτώση της αρτηριακής πίεσης (που αντιστοιχεί σε αναφυλακτική αντίδραση "). Ανεκτή από του στόματος ρισπεριδόνη ή από του στόματος παλιπεριδόνη, σπάνια εμφανίζονται αλλεργικές αντιδράσεις μετά τη λήψη ενέσεων Xeplion.
Ενδέχεται να εμφανιστούν οι ακόλουθες ανεπιθύμητες ενέργειες:
Πολύ συχνές: μπορεί να επηρεάσουν περισσότερα από 1 στα 10 άτομα
- δυσκολία να κοιμηθεί ή να κοιμηθεί
- πονοκέφαλο
Συχνές: μπορεί να επηρεάσουν έως 1 στα 10 άτομα
- κοινά συμπτώματα κρυολογήματος, λοίμωξη του ουροποιητικού συστήματος, αίσθηση ότι έχετε γρίπη
- Το Xeplion μπορεί να αυξήσει τα επίπεδα μιας ορμόνης που ονομάζεται «προλακτίνη» που βρίσκεται σε μια εξέταση αίματος (η οποία μπορεί να προκαλέσει συμπτώματα ή όχι). Όταν εμφανίζονται συμπτώματα υψηλού επιπέδου προλακτίνης, αυτά μπορεί να περιλαμβάνουν (στους άνδρες) πρήξιμο του μαστού, δυσκολία στη στύση ή διατήρηση σεξουαλικής δυσλειτουργίας. (Στις γυναίκες) δυσφορία στο στήθος, απώλεια γάλακτος από τους μαστούς, έμμηνο κύκλο ή άλλα προβλήματα με την περιοδο σου
- υψηλό σάκχαρο στο αίμα, αύξηση βάρους, απώλεια βάρους, αύξηση τριγλυκεριδίων (ένα λίπος) στο αίμα
- διέγερση, κατάθλιψη, άγχος
- παρκινσονισμός: Αυτή η κατάσταση μπορεί να περιλαμβάνει αργές ή μη φυσιολογικές κινήσεις, αίσθημα δυσκαμψίας ή έντασης των μυών (καθιστώντας τις κινήσεις σπασμωδικές) και μερικές φορές ακόμη και μια αίσθηση κίνησης που παγώνει και στη συνέχεια επανεκκινείται. Άλλα σημεία του Παρκινσονισμού περιλαμβάνουν αργό ανακάτεμα στο περπάτημα, τρόμο στην ηρεμία, αυξημένο σάλιο ή / και στάξιμο και απώλεια έκφρασης του προσώπου.
- ανησυχία, αίσθημα υπνηλίας ή απώλεια εγρήγορσης
- δυστονία: αυτή είναι μια κατάσταση που περιλαμβάνει αργή ή παρατεταμένη ακούσια συστολή μυών. Ενώ μπορεί να περιλαμβάνει οποιοδήποτε μέρος του σώματος (με αποτέλεσμα μη φυσιολογική στάση), η δυστονία συχνά περιλαμβάνει τους μυς του προσώπου, συμπεριλαμβανομένων των ανώμαλων κινήσεων των ματιών, του στόματος, της γλώσσας ή του σαγονιού
- ζάλη
- δυσκινησία: Αυτή είναι μια κατάσταση που περιλαμβάνει ακούσιες κινήσεις των μυών και μπορεί να περιλαμβάνει επαναλαμβανόμενες, σπαστικές ή στριμμένες κινήσεις ή συσπάσεις.
- τρόμος
- χαμηλό καρδιακό ρυθμό, γρήγορο καρδιακό ρυθμό
- υψηλή πίεση του αίματος
- βήχας, βουλωμένη μύτη
- κοιλιακό άλγος, έμετος, ναυτία, δυσκοιλιότητα, διάρροια, δυσπεψία, πονόδοντος
- αύξηση των ηπατικών τρανσαμινασών στο αίμα
- εξάνθημα
- πόνος στα οστά ή στους μύες, πόνος στην πλάτη
- πυρετός, αδυναμία, κόπωση (κούραση)
- αντίδραση στο σημείο της ένεσης, συμπεριλαμβανομένης της φαγούρας, του πόνου ή του οιδήματος
Όχι συχνές: μπορεί να επηρεάσουν έως 1 στα 100 άτομα
- πνευμονία, λοίμωξη στο στήθος (βρογχίτιδα), λοίμωξη του αναπνευστικού συστήματος, ιγμορίτιδα, λοίμωξη της ουροδόχου κύστης, λοίμωξη του αυτιού, λοίμωξη των ματιών, αμυγδαλίτιδα, λοίμωξη του δέρματος, φλεγμονή του δέρματος που προκαλείται από ακάρεα, απόστημα κάτω από το δέρμα
- μείωση του αριθμού των λευκών αιμοσφαιρίων, αναιμία, μείωση των ερυθρών αιμοσφαιρίων, αύξηση των ηωσινοφίλων του αίματος (ένας τύπος λευκών αιμοσφαιρίων)
- αλλεργική αντίδραση
- διαβήτης ή επιδείνωση του διαβήτη, αύξηση της ινσουλίνης στο αίμα (ορμόνη που ελέγχει τα επίπεδα σακχάρου στο αίμα)
- αυξημένη όρεξη, απώλεια όρεξης με αποτέλεσμα υποσιτισμό και χαμηλό σωματικό βάρος
- αυξημένη χοληστερόλη στο αίμα
- διαταραχές ύπνου, αυξημένη διάθεση (μανία), σύγχυση, μειωμένη σεξουαλική επιθυμία, νευρικότητα, εφιάλτες
- όψιμη δυσκινησία (συσπάσεις ή σπασμωδικές κινήσεις που δεν μπορείτε να ελέγξετε στο πρόσωπο, τη γλώσσα ή άλλα μέρη του σώματος). Επικοινωνήστε αμέσως με το γιατρό σας εάν εμφανίσετε ακούσιες ρυθμικές κινήσεις της γλώσσας, του στόματος και του προσώπου. Μπορεί να χρειαστεί να διακόψετε αυτό το φάρμακο
- επιληπτικές κρίσεις (λιποθυμίες), λιποθυμία, επείγουσα ανάγκη κίνησης ενός μέρους του σώματος, ζάλη όταν στέκεστε όρθιοι, διαταραχές της προσοχής, προβλήματα ομιλίας, απώλεια ή ανώμαλη αίσθηση της γεύσης, μειωμένη ευαισθησία του δέρματος στον πόνο και στην αφή, α μυρμήγκιασμα, τσίμπημα ή μούδιασμα του δέρματος
- θολή όραση, μόλυνση του «ματιού» ή «ελαφρώς κόκκινο», ξηροφθαλμία
- αίσθηση περιστροφής (ίλιγγος), κουδούνισμα στα αυτιά, πόνος στο αυτί
- κολπική μαρμαρυγή (ανώμαλος καρδιακός ρυθμός), διακοπή της αγωγιμότητας μεταξύ του άνω και κάτω τμήματος της καρδιάς, μη φυσιολογική ηλεκτρική αγωγή της καρδιάς, παράταση του διαστήματος QT της καρδιάς, γρήγορος καρδιακός παλμός όταν στέκεται όρθιος, ανώμαλη ηλεκτρική ανίχνευση της καρδιάς ( ηλεκτροκαρδιογράφημα ή ΗΚΓ), αίσθημα αγώνων ή παλμών στο στήθος (αίσθημα παλμών)
- χαμηλή αρτηριακή πίεση, μείωση της αρτηριακής πίεσης όταν στέκεστε όρθιοι (ως αποτέλεσμα, ορισμένοι άνθρωποι που παίρνουν αυτό το φάρμακο μπορεί να αισθάνονται λιποθυμία, ζάλη ή λιποθυμία όταν ξαφνικά σηκώνονται ή κάθονται)
- δύσπνοια, πνευμονική συμφόρηση, συριγμός, πονόλαιμος, ρινορραγία
- κοιλιακή δυσφορία, στομαχική ή εντερική λοίμωξη, ξηροστομία, υπερβολική διέλευση αερίου ή αέρα
- αύξηση της GGT στο αίμα (ένα ηπατικό ένζυμο που ονομάζεται γάμμα-γλουταμυλτρανσφεράση), αύξηση των ηπατικών ενζύμων στο αίμα
- εξάνθημα (ή κνίδωση), κνησμός, τριχόπτωση, έκζεμα, ξηροδερμία, κόκκινο δέρμα, ακμή
- μυϊκοί σπασμοί, δυσκαμψία των αρθρώσεων, πόνος στον αυχένα, πόνος στις αρθρώσεις
- ακράτεια (έλλειψη ελέγχου) ούρων, συχνή ούρηση, πόνος κατά την ούρηση
- στυτική δυσλειτουργία, διαταραχή εκσπερμάτωσης, απώλεια εμμήνου ρύσεως, καθυστέρηση της εμμήνου ρύσεως, απουσία εμμήνου ρύσεως ή άλλα προβλήματα με την έμμηνο ρύση (γυναίκες), ανάπτυξη στήθους στους άνδρες, απώλεια μητρικού γάλακτος, σεξουαλική δυσλειτουργία, κολπική έκκριση.
- πρήξιμο του προσώπου, του στόματος, των ματιών ή των χειλιών, πρήξιμο του σώματος, των χεριών ή των ποδιών
- μια αλλαγή στον τρόπο που περπατάτε
- θωρακικός πόνος, δυσφορία στο στήθος, αίσθημα αδιαθεσίας
- σκλήρυνση του δέρματος
- πτώση
Σπάνια: μπορεί να επηρεάσει έως 1 στα 1.000 άτομα
- μυκητιασική λοίμωξη των νυχιών
- επικίνδυνα χαμηλός αριθμός συγκεκριμένου τύπου λευκών αιμοσφαιρίων που απαιτείται για την καταπολέμηση λοιμώξεων
- μείωση σε ορισμένο τύπο λευκών αιμοσφαιρίων που χρησιμεύει για την προστασία του σώματος από τη μόλυνση, μείωση των αιμοπεταλίων (αιμοσφαίρια που βοηθούν στη διακοπή της αιμορραγίας)
- σοβαρή αλλεργική αντίδραση που χαρακτηρίζεται από πυρετό, πρήξιμο του στόματος, του προσώπου, των χειλιών ή της γλώσσας, δύσπνοια, κνησμό, εξάνθημα και μερικές φορές πτώση της αρτηριακής πίεσης,
- ακατάλληλη έκκριση ορμόνης που ελέγχει τον όγκο των ούρων
- επικίνδυνα υπερβολική πρόσληψη νερού, επιπλοκές απειλητικές για τη ζωή από τον ανεξέλεγκτο διαβήτη
- χαμηλό σάκχαρο αίματος, υπερβολική πρόσληψη νερού
- έλλειψη συναισθήματος
- αδυναμία επίτευξης οργασμού
- κακόηθες νευροληπτικό σύνδρομο (σύγχυση, μείωση ή απώλεια συνείδησης, υψηλός πυρετός και έντονη μυϊκή δυσκαμψία), ξαφνική απώλεια παροχής αίματος στον εγκέφαλο (εγκεφαλικό επεισόδιο ή «μίνι» εγκεφαλικό επεισόδιο), έλλειψη ανταπόκρισης σε ερεθίσματα, απώλεια συνείδησης, χαμηλό επίπεδο συνείδηση, διαταραχές της ισορροπίας
- αγγειακά προβλήματα στον εγκέφαλο, κώμα που προκαλείται από ανεξέλεγκτο διαβήτη, ανώμαλος συντονισμός, τρόμος στο κεφάλι
- γλαύκωμα (αυξημένη πίεση στο εσωτερικό του βολβού του ματιού), προβλήματα με την κίνηση των ματιών, κύλιση των ματιών προς το πίσω μέρος του κεφαλιού, υπερευαισθησία των ματιών στο φως, αυξημένα δάκρυα, κόκκινα μάτια
- ακανόνιστος καρδιακός παλμός της καρδιάς
- θρόμβοι αίματος στις φλέβες, ιδιαίτερα στα πόδια (τα συμπτώματα περιλαμβάνουν πρήξιμο, πόνο και ερυθρότητα στα πόδια), τα οποία μπορούν να ταξιδέψουν κατά μήκος των αιμοφόρων αγγείων στους πνεύμονες, προκαλώντας πόνο στο στήθος και δυσκολία στην αναπνοή. Εάν παρατηρήσετε κάποιο από αυτά τα συμπτώματα, συμβουλευτείτε αμέσως το γιατρό σας.
- μειωμένο οξυγόνο σε μέρη του σώματος (επειδή μειώνεται η ροή του αίματος), έξαψη
- αναπνευστικά προβλήματα κατά τη διάρκεια του ύπνου (άπνοια ύπνου), γρήγορη και ρηχή αναπνοή, πνευμονία που προκαλείται από εισπνοή τροφής, συμφόρηση των αεραγωγών, διαταραχή της φωνής.
- φλεγμονή του παγκρέατος, απόφραξη του εντέρου, πρησμένη γλώσσα, ακράτεια κοπράνων, πολύ σκληρά κόπρανα, δυσκολία στην κατάποση, σκασμένα χείλη, έλλειψη κίνησης του εντέρου που προκαλεί απόφραξη
- κιτρίνισμα του δέρματος και των ματιών (ίκτερος)
- σοβαρή αλλεργική αντίδραση με οίδημα που μπορεί να επηρεάσει το λαιμό προκαλώντας δυσκολία στην αναπνοή,
- εξάνθημα που σχετίζεται με τα ναρκωτικά, αποχρωματισμός του δέρματος, πάχυνση του δέρματος, απολέπιση και φαγούρα του τριχωτού της κεφαλής ή του δέρματος, πιτυρίδα
- διάσπαση των μυϊκών ινών και μυϊκός πόνος (ραβδομυόλυση), μη φυσιολογική στάση του σώματος
- αύξηση της CPK (φωσφοκινάση κρεατίνης) στο αίμα, ένα ένζυμο που μερικές φορές απελευθερώνεται όταν υπάρχει μυϊκή βλάβη, πρήξιμο των αρθρώσεων, μυϊκή αδυναμία
- αδυναμία ούρησης
- πριαπισμός (παρατεταμένη στύση του πέους που μπορεί να απαιτήσει χειρουργική θεραπεία)
- πόνος στο στήθος, δυσφορία στο στήθος, διεύρυνση στήθους, διεύρυνση στήθους, διαρροή υγρού στήθους από τους μαστούς
- πολύ χαμηλή θερμοκρασία σώματος, μείωση της θερμοκρασίας του σώματος, ρίγη, αύξηση της θερμοκρασίας του σώματος, αίσθημα δίψας, συμπτώματα απόσυρσης φαρμάκων
- συσσώρευση πύου που προκαλείται από μόλυνση στο σημείο της ένεσης, βαθιά λοίμωξη του δέρματος, κύστη στο σημείο της ένεσης, μώλωπες στο σημείο της ένεσης
Άγνωστο: η συχνότητα δεν μπορεί να εκτιμηθεί από τα διαθέσιμα δεδομένα
- ζάχαρη στα ούρα Οι ακόλουθες ανεπιθύμητες ενέργειες έχουν παρατηρηθεί με τη χρήση ενός άλλου φαρμάκου που ονομάζεται ρισπεριδόνη, το οποίο είναι πολύ παρόμοιο με την παλιπεριδόνη, επομένως αυτές οι επιδράσεις μπορεί να αναμένονται και με αυτό το φάρμακο: άλλοι τύποι προβλημάτων των αιμοφόρων αγγείων του εγκεφάλου, ήχοι κρεπτίων του πνεύμονα, θάνατος των κυττάρων του δέρματος στο σημείο της ένεσης και του έλκους στο σημείο της ένεσης.Ματιώδη προβλήματα μπορεί επίσης να εμφανιστούν κατά τη διάρκεια χειρουργικής επέμβασης καταρράκτη. Κατά τη διάρκεια χειρουργικής επέμβασης καταρράκτη, μπορεί να εμφανιστεί μια κατάσταση που ονομάζεται σύνδρομο ενδοεγχειρητικής δισκέτας (IFIS) εάν παίρνετε ή έχετε πάρει Xeplion. Εάν πρόκειται να υποβληθείτε σε χειρουργική επέμβαση καταρράκτη, φροντίστε να ενημερώσετε το γιατρό σας εάν παίρνετε ή έχετε πάρει αυτό το φάρμακο.
Αναφορά παρενεργειών
Εάν παρατηρήσετε κάποια ανεπιθύμητη ενέργεια, μιλήστε με τον γιατρό, τον φαρμακοποιό ή τον νοσοκόμο σας. Αυτό περιλαμβάνει τυχόν ανεπιθύμητες ενέργειες που δεν αναφέρονται στο παρόν φύλλο οδηγιών χρήσης. Μπορείτε επίσης να αναφέρετε ανεπιθύμητες ενέργειες απευθείας μέσω του εθνικού συστήματος αναφοράς που παρατίθεται στο Παράρτημα V. Παρενέργειες που μπορείτε να βοηθήσετε παρέχουν περισσότερες πληροφορίες σχετικά με την ασφάλεια αυτού του φαρμάκου
Λήξη και διατήρηση
Κρατήστε αυτό το φάρμακο μακριά από τα μάτια και την πρόσβαση των παιδιών.
Μη χρησιμοποιείτε αυτό το φάρμακο μετά την ημερομηνία λήξης που αναφέρεται στο κουτί. Η ημερομηνία λήξης αναφέρεται στην τελευταία ημέρα του μήνα.
Μην φυλάσσετε σε θερμοκρασία μεγαλύτερη των 30 ° C.
Μην πετάτε φάρμακα μέσω λυμάτων ή οικιακών απορριμμάτων. Ρωτήστε τον φαρμακοποιό σας πώς να πετάξετε φάρμακα που δεν χρησιμοποιείτε πια. Αυτό θα βοηθήσει στην προστασία του περιβάλλοντος.
Σύνθεση και φαρμακευτική μορφή
Τι περιέχει το Xeplion
Το δραστικό συστατικό είναι η παλιπεριδόνη.
Κάθε προγεμισμένη σύριγγα Xeplion 25 mg περιέχει 39 mg παλμιτικής παλιπεριδόνης.
Κάθε προγεμισμένη σύριγγα Xeplion 50 mg περιέχει 78 mg παλμιτικής παλιπεριδόνης.
Κάθε προγεμισμένη σύριγγα Xeplion 75 mg περιέχει 117 mg παλμιτικής παλιπεριδόνης.
Κάθε προγεμισμένη σύριγγα Xeplion 100 mg περιέχει 156 mg παλμιτικής παλιπεριδόνης.
Κάθε προγεμισμένη σύριγγα Xeplion 150 mg περιέχει 234 mg παλμιτικής παλιπεριδόνης.
Τα άλλα συστατικά είναι: Πολυσορβικό 20 Πολυαιθυλενογλυκόλη 4000 Μονοϋδρικό κιτρικό οξύ Διένυδρο όξινο φωσφορικό νάτριο άνυδρο Νάτριο διυδρογόνο φωσφορικό μονοένυδρο Υδροξείδιο του νατρίου (για ρύθμιση του pH) Νερό για ενέσεις
Περιγραφή της εμφάνισης του Xeplion και περιεχόμενο της συσκευασίας
Το Xeplion είναι ένα λευκό έως υπόλευκο ενέσιμο εναιώρημα παρατεταμένης αποδέσμευσης σε μια προγεμισμένη σύριγγα.
Κάθε συσκευασία περιέχει 1 προγεμισμένη σύριγγα και 2 βελόνες.
Πακέτο έναρξης θεραπείας: Κάθε συσκευασία περιέχει 1 συσκευασία Xeplion 150 mg και 1 συσκευασία Xeplion 100 mg.
Φύλλο οδηγιών χρήσης: AIFA (Ιταλικός Οργανισμός Φαρμάκων). Περιεχόμενο που δημοσιεύτηκε τον Ιανουάριο 2016. Οι πληροφορίες που υπάρχουν δεν μπορεί να είναι ενημερωμένες.
Για να έχετε πρόσβαση στην πιο ενημερωμένη έκδοση, είναι σκόπιμο να αποκτήσετε πρόσβαση στον ιστότοπο AIFA (Ιταλικός Οργανισμός Φαρμάκων). Αποποίηση ευθυνών και χρήσιμες πληροφορίες.
01.0 ΟΝΟΜΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟDΟΝΤΟΣ
XEPLION 100 MG ΑΠΕΝΕΡΓΟΠΟΙΗΜΕΝΗ ΑΠΟΣΤΟΛΗ ΑΠΟΣΤΟΛΗΣ ΑΠΟΣΤΟΛΗΣ
02.0 ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ
Κάθε προγεμισμένη σύριγγα περιέχει 156 mg παλμιτικής παλιπεριδόνης ισοδύναμη με 100 mg παλιπεριδόνης.
Για τον πλήρη κατάλογο των εκδόχων, ανατρέξτε στην ενότητα 6.1.
03.0 ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ ΜΟΡΦΗ
Ενέσιμο εναιώρημα παρατεταμένης αποδέσμευσης.
Το χρώμα της ανάρτησης είναι λευκό έως υπόλευκο. Το εναιώρημα βρίσκεται σε ουδέτερο ρΗ (περίπου 7,0).
04.0 ΚΛΙΝΙΚΕΣ ΠΛΗΡΟΦΟΡΙΕΣ
04.1 Θεραπευτικές ενδείξεις
Το XEPLION ενδείκνυται για τη θεραπεία συντήρησης της σχιζοφρένειας σε ενήλικες ασθενείς που έχουν σταθεροποιηθεί σε παλιπεριδόνη ή ρισπεριδόνη.
Σε επιλεγμένους ενήλικες ασθενείς με σχιζοφρένεια και οι οποίοι έχουν ανταποκριθεί προηγουμένως σε στοματική παλιπεριδόνη ή ρισπεριδόνη, το XEPLION μπορεί να χρησιμοποιηθεί χωρίς προηγούμενη στοματική σταθεροποίηση εάν τα ψυχωσικά συμπτώματα είναι ήπια έως μέτρια και απαιτείται μακράς δράσης ενέσιμη θεραπεία.
04.2 Δοσολογία και τρόπος χορήγησης
Δοσολογία
Συνιστάται η έναρξη του XEPLION με δόση 150 mg την 1η ημέρα της θεραπείας και δόση 100 mg μία εβδομάδα αργότερα (ημέρα 8), και στις δύο περιπτώσεις που χορηγείται στον δελτοειδή μυ για να επιτευχθούν γρήγορα θεραπευτικές συγκεντρώσεις (βλ. Παράγραφο 5.2 ). Η τρίτη δόση πρέπει να χορηγείται ένα μήνα μετά τη δεύτερη δόση. Η συνιστώμενη μηνιαία δόση συντήρησης είναι 75 mg. ορισμένοι ασθενείς μπορεί να επωφεληθούν από χαμηλότερες ή υψηλότερες δόσεις εντός του συνιστώμενου εύρους 25-150 mg με βάση την υποκειμενική ανεκτικότητα και / ή αποτελεσματικότητα. Οι υπέρβαροι ή παχύσαρκοι ασθενείς μπορεί να απαιτούν δόσεις κοντά στο ανώτερο εύρος (βλέπε παράγραφο 5.2). Μετά τη δεύτερη δόση, μπορούν να χορηγηθούν μηνιαίες δόσεις συντήρησης τόσο στον δελτοειδή μυ όσο και στον γλουτό.
"Η προσαρμογή της δόσης συντήρησης μπορεί να γίνει μηνιαία. Κατά την προσαρμογή της δόσης, θα πρέπει να ληφθούν υπόψη τα χαρακτηριστικά παρατεταμένης αποδέσμευσης του XEPLION (βλ. Παράγραφο 5.2), καθώς το πλήρες αποτέλεσμα των δόσεων συντήρησης μπορεί να μην είναι εμφανές για αρκετούς μήνες.
Μετάβαση από την από του στόματος παλιπεριδόνη ή από του στόματος ρισπεριδόνη
Στην αρχική φάση της θεραπείας με XEPLION, η προηγούμενη από του στόματος παλιπεριδόνη ή από του στόματος ρισπεριδόνη μπορεί να αποσυρθεί. Το XEPLION πρέπει να ξεκινήσει όπως περιγράφηκε προηγουμένως στην αρχή της ενότητας 4.2.
Μετάβαση από ενέσιμη ρισπεριδόνη σε παρατεταμένη αποδέσμευση
Όταν οι ασθενείς μεταβαίνουν από ενέσιμη ρισπεριδόνη σε παρατεταμένη αποδέσμευση, ξεκινήστε θεραπεία με XEPLION στη θέση της επόμενης προγραμματισμένης ένεσης. Το XEPLION πρέπει στη συνέχεια να συνεχίζεται σε μηνιαία διαστήματα. Το αρχικό πρόγραμμα δοσολογίας της εβδομάδας 1, το οποίο περιλαμβάνει ενδομυϊκές ενέσεις (την ημέρα 1 και την ημέρα, αντίστοιχα), όπως περιγράφεται στην παράγραφο 4.2, δεν απαιτείται.
Οι ασθενείς που είχαν προηγουμένως σταθεροποιηθεί σε διαφορετικές δόσεις ενέσιμης ρισπεριδόνης παρατεταμένης αποδέσμευσης μπορεί να επιτύχουν παρόμοια έκθεση σε παλιπεριδόνη σε σταθερή κατάσταση κατά τη διάρκεια της θεραπείας συντήρησης με μηνιαίες δόσεις XEPLION σύμφωνα με το ακόλουθο πρόγραμμα:
Δόσεις ενέσιμης ρισπεριδόνης παρατεταμένης αποδέσμευσης και XEPLION που απαιτούνται για την επίτευξη παρόμοιας έκθεσης σε παλιπεριδόνη σταθερής κατάστασης
Η διακοπή της αντιψυχωσικής φαρμακευτικής αγωγής πρέπει να γίνεται σύμφωνα με τις κατάλληλες συνταγογραφικές πληροφορίες. Εάν διακοπεί το XEPLION, θα πρέπει να ληφθούν υπόψη τα χαρακτηριστικά παρατεταμένης αποδέσμευσής του. Όπως συνιστάται επίσης για άλλα αντιψυχωσικά φάρμακα, η ανάγκη συνέχισης οποιουδήποτε προϋπάρχοντος αντιψυχωσικού φαρμάκου. Εξωπυραμιδικά συμπτώματα (EPS , ExtraPyramidal Symptoms) θα πρέπει να επαναξιολογούνται περιοδικά.
Χαμένη δόση
Πώς να αποφύγετε να χάσετε μια δόση
Συνιστάται η δεύτερη δόση της αρχικής φάσης της θεραπείας με XEPLION να χορηγείται μία εβδομάδα μετά την πρώτη δόση. Για να αποφύγετε να χάσετε μια δόση, η δεύτερη δόση μπορεί να δοθεί σε ασθενείς 4 ημέρες πριν ή 4 ημέρες μετά την προθεσμία μιας εβδομάδας (ημέρα 8). Ομοίως, μετά την αρχική φάση, συνιστάται να κάνετε την τρίτη ένεση και τις επόμενες ενέσεις μία φορά το μήνα. Για να αποφευχθεί η απώλεια μιας μηνιαίας δόσης, οι ασθενείς μπορούν να εγχυθούν έως και 7 ημέρες πριν ή 7 ημέρες μετά τη μηνιαία προθεσμία.
Εάν έχει παρέλθει η προγραμματισμένη ημερομηνία για τη δεύτερη ένεση του XEPLION (ημέρα 8 ± 4 ημέρες), ο προτεινόμενος τρόπος συνέχισης της θεραπείας εξαρτάται από τον χρόνο που έχει παρέλθει από την πρώτη ένεση στον ασθενή.
Χαμένη δεύτερη δόση της αρχικής φάσης (
Εάν έχουν περάσει λιγότερο από 4 εβδομάδες από την πρώτη ένεση, τότε θα πρέπει να δοθεί στον ασθενή η δεύτερη ένεση των 100 mg στον δελτοειδή μυ, το συντομότερο δυνατό. Μια τρίτη ένεση 75 mg XEPLION στον δελτοειδή ή γλουτιαίο μυ πρέπει να γίνει 5 εβδομάδες μετά την πρώτη ένεση (ανεξάρτητα από το πότε έγινε η δεύτερη ένεση). Η κανονική μηνιαία πορεία των ενέσεων στον δελτοειδή ή γλουτιαίο μυ 25-150 mg, με βάση την ατομική ανεκτικότητα και / ή αποτελεσματικότητα του ασθενούς, θα πρέπει να ακολουθείται στη συνέχεια.
Χαμένη δεύτερη δόση της αρχικής φάσης (4-7 εβδομάδες μετά την πρώτη ένεση)
Εάν έχουν περάσει 4 έως 7 εβδομάδες από την πρώτη ένεση του XEPLION, επαναφέρετε τη δοσολογία με δύο ενέσεις των 100 mg ως εξής:
1. ένεση στο δελτοειδές το συντομότερο δυνατό
2. άλλη ένεση στο δελτοειδές μία εβδομάδα αργότερα
3. επανέναρξη του κανονικού μηνιαίου κύκλου ενέσεων στον δελτοειδή ή γλουτιαίο μυ 25-150 mg, με βάση την ατομική ανεκτικότητα και / ή αποτελεσματικότητα του ασθενούς.
Χαμένη δεύτερη δόση της αρχικής φάσης (> 7 εβδομάδες μετά την πρώτη ένεση)
Εάν έχουν περάσει πάνω από 7 εβδομάδες από την πρώτη ένεση του XEPLION, ξεκινήστε τη χορήγηση όπως περιγράφεται στις συστάσεις για την αρχική φάση του XEPLION που αναφέρονται παραπάνω.
Χαμένη μηνιαία δόση συντήρησης (από 1 μήνα έως 6 εβδομάδες)
Μετά την αρχική φάση, η συνιστώμενη πορεία ενέσεων του XEPLION είναι μηνιαία. Εάν έχουν περάσει λιγότερο από 6 εβδομάδες από την τελευταία ένεση, τότε η προηγουμένως καθορισμένη δόση θα πρέπει να χορηγηθεί το συντομότερο δυνατό, ακολουθούμενη από ενέσεις σε μηνιαία διαστήματα.
Χαμένη μηνιαία δόση συντήρησης (> 6 εβδομάδες έως 6 μήνες)
Εάν έχουν περάσει πάνω από 6 εβδομάδες από την τελευταία ένεση του XEPLION, οι συστάσεις έχουν ως εξής:
Για ασθενείς σταθεροποιημένους με δόσεις 25 έως 100 mg:
1. ένεση δελτοειδούς το συντομότερο δυνατό στην ίδια δόση με την οποία ο ασθενής είχε προηγουμένως σταθεροποιηθεί
2. άλλη ένεση δελτοειδούς (ίδια δόση) μία εβδομάδα αργότερα (ημέρα 8)
3. επανέναρξη του κανονικού μηνιαίου κύκλου ενέσεων στον δελτοειδή ή γλουτιαίο μυ 25-150 mg, με βάση την ατομική ανεκτικότητα και / ή αποτελεσματικότητα του ασθενούς.
Για ασθενείς σταθεροποιημένους με 150 mg:
1. ένεση στο δελτοειδές το συντομότερο δυνατό σε δόση 100 mg
2. άλλη ένεση δελτοειδούς μία εβδομάδα αργότερα (ημέρα 8) σε δόση 100 mg
3. επανέναρξη του κανονικού μηνιαίου κύκλου ενέσεων στον δελτοειδή ή γλουτιαίο μυ 25-150 mg, με βάση την ατομική ανεκτικότητα και / ή αποτελεσματικότητα του ασθενούς.
Χαμένη μηνιαία δόση συντήρησης (> 6 μήνες). Εάν έχουν περάσει περισσότεροι από 6 μήνες από την τελευταία ένεση του XEPLION, ξεκινήστε τη δοσολογία όπως περιγράφεται στις συστάσεις για την αρχική φάση του XEPLION που αναφέρονται παραπάνω.
Ειδικοί πληθυσμοί
Ηλικιωμένος πληθυσμός
Η αποτελεσματικότητα και η ασφάλεια σε άτομα ηλικίας> 65 ετών δεν έχουν τεκμηριωθεί.
Γενικά, η συνιστώμενη δοσολογία του XEPLION για ηλικιωμένους ασθενείς με φυσιολογική νεφρική λειτουργία είναι η ίδια με αυτή των νεότερων ενηλίκων ασθενών με φυσιολογική νεφρική λειτουργία. Ωστόσο, καθώς οι ηλικιωμένοι ασθενείς μπορεί να έχουν διαταραγμένη νεφρική λειτουργία, μπορεί να απαιτείται προσαρμογή της δόσης (βλ. Παράγραφο Νεφρική ανεπάρκεια παρακάτω για συστάσεις δοσολογίας σε ασθενείς με νεφρική ανεπάρκεια).
Νεφρική ανεπάρκεια
Το XEPLION δεν έχει μελετηθεί συστηματικά σε ασθενείς με νεφρική ανεπάρκεια (βλ. Παράγραφο 5.2). Για ασθενείς με ήπια νεφρική δυσλειτουργία (κάθαρση κρεατινίνης ≥ 50 έως
Το XEPLION δεν συνιστάται σε ασθενείς με μέτρια ή σοβαρή νεφρική δυσλειτουργία (κάθαρση κρεατινίνης
Ηπατική ανεπάρκεια
Με βάση την εμπειρία με από του στόματος παλιπεριδόνη, δεν απαιτείται προσαρμογή της δόσης σε ασθενείς με ήπια έως μέτρια ηπατική δυσλειτουργία. Δεδομένου ότι η παλιπεριδόνη δεν έχει μελετηθεί σε ασθενείς με σοβαρή ηπατική δυσλειτουργία, συνιστάται προσοχή σε αυτούς τους ασθενείς.
Άλλοι ειδικοί πληθυσμοί
Δεν συνιστάται προσαρμογή της δόσης για το XEPLION με βάση το φύλο, τη φυλή ή την κατάσταση του καπνιστή.
Παιδιατρικός πληθυσμός
Η ασφάλεια και η αποτελεσματικότητα του XEPLION σε παιδιά ηλικίας κάτω των 18 ετών δεν έχουν τεκμηριωθεί. Δεν υπάρχουν διαθέσιμα δεδομένα.
Τρόπος χορήγησης
Το XEPLION προορίζεται μόνο για ενδομυϊκή χρήση. Πρέπει να εγχυθεί αργά και βαθιά στον μυ. Κάθε ένεση πρέπει να γίνεται από επαγγελματία υγείας. Η χορήγηση πρέπει να πραγματοποιείται σε μία μόνο ένεση. Η δόση δεν πρέπει να χορηγείται ως ξεχωριστές ενέσεις. Η δόση δεν πρέπει να χορηγείται ενδοφλεβίως ή υποδορίως.
Οι δόσεις τις ημέρες 1 και 8 της αρχικής φάσης θα πρέπει και οι δύο να χορηγηθούν στον δελτοειδή μυ για να επιτευχθούν γρήγορα θεραπευτικές συγκεντρώσεις (βλ. Παράγραφο 5.2). Μετά τη δεύτερη δόση, μπορούν να χορηγηθούν μηνιαίες δόσεις συντήρησης στον δελτοειδή μυ ή στο γλουτιαίο μέγιστο. Η μετάβαση από τον γλουτό στο δελτοειδή (και αντίστροφα) θα πρέπει να λαμβάνεται υπόψη για τον πόνο στο σημείο της ένεσης εάν αυτή η ταλαιπωρία δεν είναι καλά ανεκτή (βλ. Παράγραφο 4.8). Συνιστάται επίσης εναλλαγή μεταξύ αριστερής και δεξιάς πλευράς (δείτε παρακάτω).
Για οδηγίες χρήσης και χειρισμού του XEPLION, ανατρέξτε στην ενότητα του φύλλου οδηγιών (πληροφορίες που προορίζονται για ιατρούς ή επαγγελματίες υγείας).
Χορήγηση στον δελτοειδή μυ
Το συνιστώμενο μέγεθος βελόνας για την αρχική και συντηρητική χορήγηση του XEPLION στον δελτοειδή μυ καθορίζεται από το βάρος του ασθενούς. Για βάρος ≥ 90 kg, 1½-ίντσας, 22 G (38,1 mm x 0,72 mm) Για βάρος δελτοειδείς μύες.
Χορήγηση στον γλουτιαίο μυ
Το συνιστώμενο μέγεθος βελόνας για χορήγηση συντήρησης του XEPLION στον γλουτιαίο μυ είναι 1 ίντσα, 22 G (38,1 mm x 0,72 mm). Η χορήγηση πρέπει να πραγματοποιείται στο εξωτερικό άνω τεταρτημόριο της περιοχής του γλουτού. Οι ενέσεις στον γλουτό πρέπει να εναλλάσσονται μεταξύ των δύο γλουτιαίων μυών.
04.3 Αντενδείξεις
Υπερευαισθησία στη δραστική ουσία, στη ρισπεριδόνη ή σε κάποιο από τα έκδοχα που αναφέρονται στην παράγραφο 6.1.
04.4 Ειδικές προειδοποιήσεις και κατάλληλες προφυλάξεις κατά τη χρήση
Χρήση σε ασθενείς σε οξεία διέγερση ή σε σοβαρή ψυχωτική κατάσταση
Το XEPLION δεν πρέπει να χρησιμοποιείται για τη διαχείριση οξείας διέγερσης ή σοβαρών ψυχωτικών καταστάσεων όταν απαιτείται άμεσος έλεγχος των συμπτωμάτων.
Διάστημα QT
Πρέπει να δίνεται προσοχή όταν συνταγογραφείται παλιπεριδόνη σε ασθενείς με γνωστές καρδιαγγειακές διαταραχές ή με οικογενειακό ιστορικό παράτασης του QT και με ταυτόχρονη χρήση άλλων φαρμάκων που πιστεύεται ότι παρατείνουν το διάστημα QT.
Κακόηθες νευροληπτικό σύνδρομο
Κακόηθες νευροληπτικό σύνδρομο (ΝΜΣ), που χαρακτηρίζεται από υπερθερμία, μυϊκή δυσκαμψία, αστάθεια του αυτόνομου νευρικού συστήματος, αλλαγές στη συνείδηση και αυξημένη φωσφοκινάση κρεατίνης στον ορό, έχει αναφερθεί με παλιπεριδόνη Επιπρόσθετες κλινικές εκδηλώσεις μπορεί να περιλαμβάνουν μυοσφαιρινουρία (ραβδομυόλυση) και οξεία νεφρική ανεπάρκεια. Εάν ένας ασθενής παρουσιάζει σημεία ή συμπτώματα που υποδηλώνουν NMS, η θεραπεία με οποιοδήποτε αντιψυχωσικό, συμπεριλαμβανομένης της παλιπεριδόνης, θα πρέπει να διακόπτεται.
Όψιμη δυσκινησία
Φάρμακα με ανταγωνιστική δράση σε ντοπαμινεργικούς υποδοχείς έχουν συσχετιστεί με την πρόκληση όψιμης δυσκινησίας που χαρακτηρίζεται από ρυθμικές και ακούσιες κινήσεις, ιδιαίτερα της γλώσσας και / ή του προσώπου. Διακόψτε οποιαδήποτε αντιψυχωσικά, συμπεριλαμβανομένης της παλιπεριδόνης.
Λευκοπενία, ουδετεροπενία και ακοκκιοκυτταραιμία
Έχουν αναφερθεί γεγονότα λευκοπενίας, ουδετεροπενίας και ακοκκιοκυττάρωσης με τη χρήση αντιψυχωσικών, συμπεριλαμβανομένου του XEPLION. Η ακοκκιοκυτταραιμία έχει αναφερθεί πολύ σπάνια (τα λευκά αιμοσφαίρια (WBC) ή η επαγόμενη από φάρμακα λευκοπενία / ουδετεροπενία θα πρέπει να παρακολουθούνται κατά τη διάρκεια της παρακολούθησης μετά την κυκλοφορία). οι πρώτοι μήνες θεραπείας και η διακοπή του XEPLION θα πρέπει να εξεταστούν στο πρώτο σημάδι κλινικά σημαντικής μείωσης του WBC απουσία άλλων αιτιολογικών παραγόντων. Οι ασθενείς με κλινικά σημαντική ουδετεροπενία πρέπει να παρακολουθούνται στενά για πυρετό ή άλλα συμπτώματα ή σημεία μόλυνσης και να αντιμετωπίζονται άμεσα εάν εμφανιστούν τέτοια συμπτώματα ή σημεία. Ασθενείς με σοβαρή ουδετεροπενία (απόλυτος αριθμός ουδετερόφιλων
Υπεργλυκαιμία και σακχαρώδης διαβήτης
Κατά τη διάρκεια της θεραπείας με παλιπεριδόνη έχουν αναφερθεί υπεργλυκαιμία, σακχαρώδης διαβήτης και επιδείνωση προϋπάρχοντος διαβήτη. Σε ορισμένες περιπτώσεις, έχει αναφερθεί προηγούμενη αύξηση βάρους που θα μπορούσε να είναι ένας προδιαθεσικός παράγοντας. Η συσχέτιση με την κετοξέωση έχει αναφερθεί πολύ σπάνια και σπάνια με διαβητικό κώμα. Συνιστάται η κατάλληλη κλινική παρακολούθηση σύμφωνα με τις οδηγίες που χρησιμοποιούνται για τα αντιψυχωσικά. Οι ασθενείς που λαμβάνουν θεραπεία με οποιοδήποτε άτυπο αντιψυχωσικό, συμπεριλαμβανομένου του XEPLION, θα πρέπει να παρακολουθούνται για συμπτώματα υπεργλυκαιμίας. (Όπως πολυδιψία, πολυουρία, πολυφαγία και αδυναμία) και οι ασθενείς με σακχαρώδη διαβήτη πρέπει να παρακολουθούνται τακτικά για επιδείνωση του γλυκαιμικού ελέγχου.
Αύξηση βάρους
Έχει αναφερθεί σημαντική αύξηση βάρους κατά τη χρήση του XEPLION. Το βάρος πρέπει να αξιολογείται τακτικά.
Υπερπρολακτιναιμία
Μελέτες κυτταρικής καλλιέργειας υποδεικνύουν ότι η κυτταρική ανάπτυξη στους ανθρώπινους όγκους του μαστού μπορεί να διεγερθεί από την προλακτίνη. Αν και δεν έχει αποδειχθεί μέχρι στιγμής σαφής συσχέτιση με τη χορήγηση αντιψυχωσικών σε κλινικές και επιδημιολογικές μελέτες, συνιστάται προσοχή σε ασθενείς με σχετικό ιατρικό ιστορικό. Η παλιπεριδόνη πρέπει να χρησιμοποιείται με προσοχή σε ασθενείς με πιθανούς όγκους εξαρτώμενους από την προλακτίνη.
Ορθοστατική υπόταση
Η παλιπεριδόνη μπορεί να προκαλέσει ορθοστατική υπόταση σε μερικούς ασθενείς λόγω της άλφα-αποκλειστικής της δράσης.
Βάσει συγκεντρωτικών δεδομένων από τρεις δοκιμές ελεγχόμενου με εικονικό φάρμακο, 6 εβδομάδων, σταθερών δόσεων με δισκία παλιπεριδόνης από του στόματος παρατεταμένης αποδέσμευσης (3, 6, 9 και 12 mg), αναφέρθηκε ορθοστατική υπόταση από το 2,5% των ατόμων που έλαβαν από του στόματος παλιπεριδόνη έναντι 0,8% των ατόμων που έλαβαν εικονικό φάρμακο. Το XEPLION πρέπει να χρησιμοποιείται με προσοχή σε ασθενείς με γνωστή καρδιαγγειακή νόσο (π.χ. καρδιακή ανεπάρκεια, έμφραγμα του μυοκαρδίου ή ισχαιμία, ελαττώματα αγωγιμότητας), εγκεφαλοαγγειακή νόσο ή καταστάσεις που προδιαθέτουν τον ασθενή σε υπόταση (όπως αφυδάτωση και υποογκαιμία).
Σπασμοί
Το XEPLION πρέπει να χρησιμοποιείται με προσοχή σε ασθενείς με ιστορικό επιληπτικών κρίσεων ή άλλων καταστάσεων που μπορεί να μειώσουν το όριο επιληπτικών κρίσεων.
Νεφρική ανεπάρκεια
Οι συγκεντρώσεις της παλιπεριδόνης στο πλάσμα αυξάνονται σε ασθενείς με νεφρική ανεπάρκεια και, ως εκ τούτου, συνιστάται προσαρμογή της δόσης σε ασθενείς με ήπια νεφρική ανεπάρκεια. Το XEPLION δεν συνιστάται σε ασθενείς με μέτρια ή σοβαρή νεφρική δυσλειτουργία (κάθαρση κρεατινίνης
Ηπατική ανεπάρκεια
Δεν υπάρχουν διαθέσιμα δεδομένα σε ασθενείς με σοβαρή ηπατική δυσλειτουργία (Child-Pugh Class C). Συνιστάται προσοχή όταν χρησιμοποιείτε παλιπεριδόνη σε τέτοιους ασθενείς.
Ηλικιωμένοι ασθενείς με άνοια
Δεν έχουν διεξαχθεί μελέτες με το XEPLION σε ηλικιωμένους ασθενείς με άνοια. Το XEPLION πρέπει να χρησιμοποιείται με προσοχή σε ηλικιωμένους ασθενείς με άνοια με παράγοντες κινδύνου εγκεφαλικού επεισοδίου. Η εμπειρία με τη ρισπεριδόνη που αναφέρεται παρακάτω θεωρείται επίσης έγκυρη για την παλιπεριδόνη.
Παγκόσμια θνησιμότητα
Σε μετα-ανάλυση 17 ελεγχόμενων κλινικών δοκιμών, ηλικιωμένοι ασθενείς με άνοια που έλαβαν θεραπεία με άλλα άτυπα αντιψυχωσικά, συμπεριλαμβανομένης της ρισπεριδόνης, της αριπιπραζόλης, της ολανζαπίνης και της κουετιαπίνης, είχαν υψηλότερο κίνδυνο θνησιμότητας από το εικονικό φάρμακο. Μεταξύ εκείνων που έλαβαν ρισπεριδόνη, η θνησιμότητα ήταν 4% σε σύγκριση με το 3,1% για το εικονικό φάρμακο.
Ανεπιθύμητες ενέργειες εγκεφαλοαγγειακών αγγείων
Σε τυχαιοποιημένες ελεγχόμενες με εικονικό φάρμακο κλινικές δοκιμές σε ασθενείς με άνοια που έλαβαν θεραπεία με κάποια άτυπα αντιψυχωσικά, συμπεριλαμβανομένης της ρισπεριδόνης, της αριπιπραζόλης και της ολανζαπίνης, παρατηρήθηκε περίπου τριπλάσιος κίνδυνος ανεπιθύμητων ενεργειών των εγκεφαλοαγγειακών αγγείων. Ο μηχανισμός πίσω από τον αυξημένο κίνδυνο είναι άγνωστος.
Νόσος Πάρκινσον και άνοια με σώματα Lewy
Οι γιατροί θα πρέπει να σταθμίσουν τους κινδύνους και τα οφέλη από τη συνταγογράφηση του XEPLION σε ασθενείς με νόσο του Πάρκινσον ή άνοια με σώματα Lewy (DLB) καθώς και οι δύο ομάδες ασθενών μπορεί να διατρέχουν μεγαλύτερο κίνδυνο ανάπτυξης νευροληπτικού κακοήθους συνδρόμου, καθώς και αυξημένη ευαισθησία στα αντιψυχωσικά. Οι εκδηλώσεις αυτής της αυξημένης ευαισθησίας μπορεί να περιλαμβάνουν σύγχυση, θαμπάδα, αστάθεια στη στάση του σώματος με συχνές πτώσεις, καθώς και εξωπυραμιδικά συμπτώματα.
Πριαπισμός
Αντιψυχωσικά φαρμακευτικά προϊόντα (συμπεριλαμβανομένης της ρισπεριδόνης) με αλφα-αδρενεργικά αποτελέσματα αποκλεισμού έχουν αναφερθεί ότι προκαλούν πριαπισμό. Κατά τη διάρκεια της εποπτείας μετά την κυκλοφορία, έχει αναφερθεί πριαπισμός με την από του στόματος παλιπεριδόνη, η οποία είναι ο ενεργός μεταβολίτης της ρισπεριδόνης. Οι ασθενείς θα πρέπει να ενημερώνονται ότι εάν ο πριαπισμός δεν υποχωρήσει μέσα σε 3-4 ώρες, θα πρέπει να αναζητήσουν επείγουσα ιατρική βοήθεια.
Ρύθμιση θερμοκρασίας σώματος
Η μειωμένη ικανότητα του σώματος να μειώσει τη θερμοκρασία του σώματος έχει αποδοθεί σε αντιψυχωσικά φάρμακα. Συνιστάται ιδιαίτερη προσοχή όταν συνταγογραφείτε το XEPLION σε ασθενείς που μπορεί να εκτεθούν σε καταστάσεις που μπορεί να συμβάλουν στην αύξηση της θερμοκρασίας του πυρήνα του σώματος, όπως έντονη άσκηση, έκθεση σε ακραία ζέστη, ταυτόχρονη θεραπεία αντιχολινεργικών φαρμάκων ή επιρρεπείς σε αφυδάτωση.
Φλεβική θρομβοεμβολή
Έχουν αναφερθεί περιπτώσεις φλεβικής θρομβοεμβολής (VTE) με αντιψυχωσικά φάρμακα.
Οι ασθενείς που λαμβάνουν αντιψυχωσικά έχουν συχνά αποκτήσει παράγοντες κινδύνου για VTE, επομένως όλοι οι πιθανοί παράγοντες κινδύνου για VTE πρέπει να προσδιοριστούν πριν και κατά τη διάρκεια της θεραπείας με XEPLION και να ληφθούν προληπτικά μέτρα.
Αντιεμετικό αποτέλεσμα
Ένα αντιεμετικό αποτέλεσμα παρατηρήθηκε σε προκλινικές μελέτες με παλιπεριδόνη. Αυτή η επίδραση, εάν εμφανιστεί σε ανθρώπους, θα μπορούσε να καλύψει τα σημεία και τα συμπτώματα υπερδοσολογίας ορισμένων φαρμάκων ή καταστάσεων όπως η εντερική απόφραξη, το σύνδρομο Reye και ο όγκος του εγκεφάλου.
Διαχείριση
Πρέπει να ληφθεί μέριμνα ώστε να αποφευχθεί η ακούσια ένεση του XEPLION σε ένα αιμοφόρο αγγείο.
Διεγχειρητικό σύνδρομο Floppy Iris
Ενδοεγχειρητικό σύνδρομο δισκέτας (IFIS) έχει παρατηρηθεί κατά τη διάρκεια χειρουργικής επέμβασης καταρράκτη σε ασθενείς που έλαβαν φαρμακευτικά προϊόντα με άλφα1α-αδρενεργικό ανταγωνιστικό αποτέλεσμα, όπως το XEPLION (βλ. Παράγραφο 4.8).
Το IFIS μπορεί να αυξήσει τον κίνδυνο οφθαλμικών επιπλοκών κατά τη διάρκεια και μετά την επέμβαση. Η τρέχουσα ή η προηγούμενη χρήση φαρμακευτικών προϊόντων με δράση άλφα1α-αδρενεργικών ανταγωνιστών πρέπει να γνωστοποιείται στον οφθαλμίατρο πριν από τη χειρουργική επέμβαση. Το πιθανό όφελος από τη διακοπή της θεραπείας με αποκλειστές alpha1 πριν από τη χειρουργική επέμβαση καταρράκτη δεν έχει τεκμηριωθεί και πρέπει να σταθμιστεί έναντι του κινδύνου διακοπής της αντιψυχωσικής θεραπείας.
04.5 Αλληλεπιδράσεις με άλλα φαρμακευτικά προϊόντα και άλλες μορφές αλληλεπίδρασης
Συνιστάται προσοχή όταν συνταγογραφείτε το XEPLION σε συνδυασμό με φαρμακευτικά προϊόντα που είναι γνωστό ότι παρατείνουν το διάστημα QT, όπως αντιαρρυθμικά κατηγορίας ΙΑ (π.χ. κινιδίνη, δισοπυραμίδη) και αντιαρρυθμικά κατηγορίας ΙΙΙ (π.χ. αμιοδαρόνη, σοταλόλη), ορισμένα αντιισταμινικά, κάποια άλλα αντιψυχωσικά και μερικά ανθελονοσιακά (π.χ. μεφλοκίνη). Ο κατάλογος είναι ενδεικτικός και όχι εξαντλητικός.
Πιθανή επίδραση του XEPLION σε άλλα φάρμακα
Η παλιπεριδόνη δεν αναμένεται να προκαλέσει κλινικά σημαντικές φαρμακοκινητικές αλληλεπιδράσεις με φαρμακευτικά προϊόντα που μεταβολίζονται από τα ισοένζυμα του κυτοχρώματος P-450.
Δεδομένων των πρωτογενών επιδράσεων της παλιπεριδόνης στο κεντρικό νευρικό σύστημα (ΚΝΣ) (βλ. Παράγραφο 4.8), το XEPLION θα πρέπει να χρησιμοποιείται με προσοχή σε συνδυασμό με άλλα φαρμακευτικά προϊόντα κεντρικής δράσης, π.χ. αγχολυτικά, τα περισσότερα αντιψυχωσικά, υπνωτικά, οπιούχα κ.λπ. ή με αλκοόλ.
Η παλιπεριδόνη μπορεί να ανταγωνιστεί τη δράση της λεβοντόπα και άλλων αγωνιστών ντοπαμίνης. Εάν αυτός ο συνδυασμός κριθεί απαραίτητος, ειδικά στην τελική φάση της νόσου του Πάρκινσον, θα πρέπει να συνταγογραφείται η χαμηλότερη αποτελεσματική δόση για κάθε θεραπεία.
Λόγω της δυνατότητάς του να προκαλέσει ορθοστατική υπόταση (βλ. Παράγραφο 4.4), μπορεί να παρατηρηθεί πρόσθετο αποτέλεσμα όταν το XEPLION χορηγείται με άλλους θεραπευτικούς παράγοντες που έχουν αυτό το δυναμικό, π.χ. άλλα αντιψυχωσικά ή τρικυκλικά.
Συνιστάται προσοχή εάν η παλιπεριδόνη χορηγείται σε συνδυασμό με άλλα φαρμακευτικά προϊόντα που πιστεύεται ότι μειώνουν το όριο επιληπτικών κρίσεων (π.χ. φαινοθειαζίνες ή βουτυροφαινόνες, τρικυκλικά ή SSRIs, τραμαδόλη, μεφλοκίνη κ.λπ.).
Η συγχορήγηση δισκίων από του στόματος παρατεταμένης αποδέσμευσης παλιπεριδόνης σε σταθερή κατάσταση (12 mg μία φορά ημερησίως) με δισκία παρατεταμένης αποδέσμευσης βαλπροϊκού οξέος + βαλπροϊκό νάτριο (500 έως 2000 mg άπαξ ημερησίως) δεν επηρέασε τη φαρμακοκινητική του βαλπροϊκού σε σταθερή κατάσταση.
Δεν έχουν διεξαχθεί μελέτες αλληλεπίδρασης μεταξύ του XEPLION και του λιθίου, ωστόσο η φαρμακοκινητική αλληλεπίδραση είναι απίθανη.
Δυνατότητα άλλων φαρμάκων να επηρεάσουν το XEPLION
Εκπαίδευση in vitro υποδεικνύουν ότι το CYP2D6 και το CYP3A4 μπορεί να εμπλέκονται ελάχιστα στο μεταβολισμό της παλιπεριδόνης, ωστόσο δεν υπάρχουν ενδείξεις ή in vitro κανενα απο τα δυο in vivo ότι αυτά τα ισοένζυμα παίζουν σημαντικό ρόλο στο μεταβολισμό της παλιπεριδόνης. Η συγχορήγηση από του στόματος παλιπεριδόνης με παροξετίνη, ένας ισχυρός αναστολέας του CYP2D6, δεν έδειξε κλινικά σημαντικές επιδράσεις στη φαρμακοκινητική της παλιπεριδόνης.
Η συγχορήγηση παλιπεριδόνης από του στόματος παρατεταμένης αποδέσμευσης μίας ημέρας με καρβαμαζεπίνη 200 mg δύο φορές ημερησίως προκάλεσε μείωση περίπου 37% της μέσης Cmax και AUC σε σταθερή κατάσταση της παλιπεριδόνης. Αυτή η μείωση προκαλείται ουσιαστικά από μια αύξηση κατά 35% της νεφρικής κάθαρσης της παλιπεριδόνης πιθανώς ως αποτέλεσμα της επαγωγής της καρβαμαζεπίνης των νεφρών P-gp. Μια μικρή μείωση της ποσότητας της δραστικής ουσίας που απεκκρίνεται αμετάβλητη στα ούρα υποδηλώνει μια ελάχιστη επίδραση στο μεταβολισμό της CYP ή τη βιοδιαθεσιμότητα της παλιπεριδόνης κατά τη συγχορήγηση με καρβαμαζεπίνη. Με υψηλότερες δόσεις καρβαμαζεπίνης, μπορεί να εμφανιστούν μεγαλύτερες μειώσεις στις συγκεντρώσεις της παλιπεριδόνης στο πλάσμα. Κατά την έναρξη της θεραπείας με καρβαμαζεπίνη, η δόση του XEPLION θα πρέπει να επανεκτιμηθεί και να αυξηθεί εάν είναι απαραίτητο. Αντίθετα, σε περίπτωση διακοπής της θεραπείας με καρβαμαζεπίνη, η δόση του XEPLION θα πρέπει να επανεκτιμηθεί και να μειωθεί εάν είναι απαραίτητο.
Η συγχορήγηση μιας εφάπαξ δόσης 12 mg από του στόματος δισκίου παλιπεριδόνης παρατεταμένης αποδέσμευσης με δισκία βαλπροϊκού οξέος παρατεταμένης αποδέσμευσης + βαλπροϊκό νάτριο (δύο δισκία των 500 mg μία φορά ημερησίως) είχε ως αποτέλεσμα αύξηση περίπου 50% Cmax και AUC παλιπεριδόνης, πιθανώς ως αποτέλεσμα της αυξημένης στοματικής απορρόφησης. Δεδομένου ότι δεν παρατηρήθηκε επίδραση στη συστηματική κάθαρση, δεν θα ήταν αναμενόμενη κλινικά σημαντική αλληλεπίδραση μεταξύ δισκίων παρατεταμένης αποδέσμευσης βαλπροϊκού οξέος + βαλπροϊκού νατρίου και ενδομυϊκής ένεσης XEPLION. Αυτή η αλληλεπίδραση δεν έχει μελετηθεί με το XEPLION.
Ταυτόχρονη χρήση του XEPLION με ρισπεριδόνη
Η ρισπεριδόνη που χορηγείται από το στόμα ή ενδομυϊκά μεταβολίζεται σε παλιπεριδόνη σε διάφορους βαθμούς. Να είστε προσεκτικοί εάν η ρισπεριδόνη από το στόμα ή η παλιπεριδόνη συγχορηγούνται με το XEPLION.
04.6 Κύηση και γαλουχία
Εγκυμοσύνη
Δεν υπάρχουν επαρκή δεδομένα για τη χρήση της παλιπεριδόνης κατά τη διάρκεια της εγκυμοσύνης. Η παλμιτική παλιπεριδόνη που χορηγείται ενδομυϊκά και η παλιπεριδόνη που χορηγείται από το στόμα δεν έχει αποδειχθεί τερατογόνος σε μελέτες σε ζώα, αλλά έχουν παρατηρηθεί και άλλοι τύποι τοξικότητας στην αναπαραγωγή (βλ. Παράγραφο 5.3). τα αντιψυχωσικά (συμπεριλαμβανομένης της παλιπεριδόνης) κατά το τρίτο τρίμηνο της εγκυμοσύνης διατρέχουν κίνδυνο ανεπιθύμητων ενεργειών, συμπεριλαμβανομένων εξωπυραμιδικών ή / και συμπτωμάτων στέρησης που μπορεί να διαφέρουν σε σοβαρότητα και διάρκεια μετά τον τοκετό. ανησυχία, υπερτονία, υποτονία, τρόμος, υπνηλία, δυσκολία στην αναπνοή ή διατροφικές διαταραχές Το Κατά συνέπεια, τα βρέφη πρέπει να παρακολουθούνται στενά. Το XEPLION δεν πρέπει να λαμβάνεται κατά τη διάρκεια της εγκυμοσύνης, εκτός εάν είναι απολύτως απαραίτητο.
Ωρα ταίσματος
Η παλιπεριδόνη απεκκρίνεται στο μητρικό γάλα σε τέτοιο βαθμό ώστε πιθανές επιδράσεις στο βρέφος που θηλάζει όταν χορηγούνται θεραπευτικές δόσεις σε θηλάζουσες γυναίκες. Το XEPLION δεν πρέπει να χρησιμοποιείται κατά τη διάρκεια του θηλασμού.
Γονιμότητα
Δεν παρατηρήθηκαν σχετικές επιδράσεις σε μη κλινικές μελέτες.
04.7 Επιδράσεις στην ικανότητα οδήγησης και χειρισμού μηχανών
Η παλιπεριδόνη μπορεί να επηρεάσει ελαφρά ή μέτρια την ικανότητα οδήγησης ή χειρισμού μηχανών λόγω πιθανών νευρικών συστημάτων και οπτικών επιδράσεων όπως καταστολή, υπνηλία, συγκοπή και θολή όραση (βλ. Παράγραφο 4.8). Επομένως, οι ασθενείς θα πρέπει να συμβουλεύονται να μην οδηγούν ή να χειρίζονται μηχανήματα έως ότου είναι γνωστή η ατομική ευαισθησία στο XEPLION.
04.8 Ανεπιθύμητες ενέργειες
Περίληψη του προφίλ ασφαλείας
Οι πιο συχνά αναφερόμενες ανεπιθύμητες ενέργειες σε κλινικές δοκιμές ήταν αϋπνία, πονοκέφαλος, άγχος, λοίμωξη του ανώτερου αναπνευστικού συστήματος, αντίδραση στο σημείο της ένεσης, παρκινσονισμός, αύξηση βάρους, ακαθισία, διέγερση, καταστολή / υπνηλία., Ναυτία, δυσκοιλιότητα, ζάλη, μυοσκελετική πόνος, ταχυκαρδία, τρόμος, κοιλιακός πόνος, έμετος, διάρροια, κόπωση και δυστονία. Από αυτά, η ακαθησία και η καταστολή / υπνηλία φαίνεται να σχετίζονται με τη δόση.
Πίνακας ανεπιθύμητων ενεργειών
Οι ακόλουθες ανεπιθύμητες ενέργειες αναφέρθηκαν όλες με παλιπεριδόνη κατά κατηγορία συχνότητας που εκτιμάται από κλινικές δοκιμές του XEPLION. Ισχύουν οι ακόλουθοι όροι και συχνότητες: πολύ κοινό (≥ 1/10), κοινός (≥ 1/100 έως σπάνια (≥ 1/1000 έως σπάνια (≥ 1/10.000 έως πολύ σπάνια (άγνωστα (δεν μπορούν να εκτιμηθούν από τα διαθέσιμα δεδομένα κλινικών δοκιμών)).
a Ανατρέξτε στην "υπερπρολακτιναιμία" παρακάτω.
β Ανατρέξτε στα "εξωπυραμιδικά συμπτώματα" παρακάτω.
γ Σε κλινικές δοκιμές ελεγχόμενες με εικονικό φάρμακο, ο σακχαρώδης διαβήτης αναφέρθηκε στο 0,32% των ασθενών που έλαβαν XEPLION έναντι 0,39% στην ομάδα του εικονικού φαρμάκου. Η συνολική επίπτωση όλων των κλινικών μελετών ήταν 0,47% σε όλους τους ασθενείς που έλαβαν θεραπεία με XEPLION.
d Η αϋπνία περιλαμβάνει: αρχική αϋπνία, κεντρική αϋπνία. Οι επιληπτικές κρίσεις περιλαμβάνουν: το οίδημα περιλαμβάνει: γενικευμένο οίδημα, περιφερικό οίδημα, πλαστικό οίδημα. Η διαταραχή της εμμήνου ρύσεως περιλαμβάνει: ακανόνιστη έμμηνο ρύση, ολιγομηνόρροια
ε Δεν παρατηρήθηκε σε κλινικές δοκιμές του XEPLION αλλά παρατηρήθηκε στην εμπειρία μετά την κυκλοφορία του φαρμάκου με παλιπεριδόνη.
Αναφέρθηκαν ανεπιθύμητες ενέργειες με σκευάσματα ρισπεριδόνης
Η παλιπεριδόνη είναι ο ενεργός μεταβολίτης της ρισπεριδόνης, επομένως, τα προφίλ ανεπιθύμητων ενεργειών αυτών των ενώσεων (συμπεριλαμβανομένων τόσο των στοματικών όσο και των ενέσιμων σκευασμάτων) σχετίζονται μεταξύ τους. Εκτός από τις ανεπιθύμητες ενέργειες που αναφέρθηκαν παραπάνω, οι ακόλουθες ανεπιθύμητες ενέργειες έχουν αναφερθεί με τη χρήση προϊόντων ρισπεριδόνης και μπορεί να αναμένονται με το XEPLION.
Διαταραχές του νευρικού συστήματος: εγκεφαλοαγγειακές διαταραχές
Διαταραχές των ματιών: sσύνδρομο ίριδας σημαίας (ενδοεγχειρητικά)
Αναπνευστικές, θωρακικές και μεσοθωρακικές διαταραχές: ραλίες
Γενικές διαταραχές και καταστάσεις στο σημείο χορήγησης (παρατηρούνται με το ενέσιμο σκεύασμα ρισπεριδόνης): νέκρωση στο σημείο της ένεσης, έλκος στο σημείο της ένεσης.
Περιγραφή επιλεγμένων ανεπιθύμητων ενεργειών
Αναφυλακτική αντίδραση
Σπάνια έχουν αναφερθεί περιπτώσεις αναφυλακτικής αντίδρασης μετά την ένεση με XEPLION σε εμπειρία μετά την κυκλοφορία σε ασθενείς που είχαν ανεχθεί προηγουμένως από του στόματος ρισπεριδόνη ή από του στόματος παλιπεριδόνη.
Αντιδράσεις στο σημείο της ένεσης
Η πιο συχνά αναφερόμενη ανεπιθύμητη αντίδραση στο σημείο της ένεσης ήταν ο πόνος. Η πλειοψηφία αυτών των αναφερόμενων αντιδράσεων ήταν ήπιας έως μέτριας σοβαρότητας. Οι βαθμολογίες των ατόμων για τον πόνο στο σημείο της ένεσης με βάση μια οπτική αναλογική κλίμακα τείνουν να μειώνονται με την πάροδο του χρόνου σε συχνότητα και ένταση σε όλες τις μελέτες της Φάσης 2 και της Φάσης 3. Οι ενέσεις Deltoid θεωρήθηκαν ως ήπια επώδυνες. Μεγαλύτερες από τις αντίστοιχες ενέσεις στον γλουτό. Άλλες αντιδράσεις στο σημείο της ένεσης ήταν κυρίως ήπιες σε ένταση και περιελάμβαναν επαγωγή (κοινή), κνησμό (σπάνιο) και οζίδια (σπάνια).
Εξωπυραμιδικά συμπτώματα (EPS)
Το EPS περιελάμβανε μια συγκεντρωτική ανάλυση των ακόλουθων όρων: παρκινσονισμός (περιλαμβάνει υπερέκκριση σιέλου, μυοσκελετική δυσκαμψία, παρκινσονισμό, απώλεια σάλιου, δυσκαμψία οδοντωτού τροχού, βραδυκινησία, υποκινησία, προσώπου μάσκας, μυϊκή ένταση, ακινησία, νουχαλική δυσκαμψία, μυϊκή δυσκαμψία, παρκινσονική δυσκαμψία, αντανακλαστικό, παρκινσονικός τρόμος σε ηρεμία), ακαθυσία (περιλαμβάνει ακαθησία, ανησυχία, υπερκινησία, σύνδρομο ανήσυχων ποδιών), δυσκινησία (περιλαμβάνει δυσκινησία, μυϊκές συσπάσεις, χοροαθέτωση, αθέτωση και μυοκλονία), δυστονία (περιλαμβάνει δυστονία, υπερτονία, τορτικολίτιδα, ακούσιες μυϊκές συσπάσεις, μυϊκή σύσπαση, βλεφαρόσπασμος, οφθαλμολογία, γλωσσική παράλυση, σπασμός προσώπου, λαρυγγόσπασμος, μυοτονία, οπίσθωνος, στοματοφαρυγγικός σπασμός, πλευροτόνιος, γλωσσικός σπασμός και τρισμός) και τρόμος. Πρέπει να σημειωθεί ότι περιλαμβάνεται ένα ευρύτερο φάσμα συμπτωμάτων που δεν έχουν απαραιτήτως πυραμιδική προέλευση
Αύξηση βάρους
Στη μελέτη 13 εβδομάδων που περιελάμβανε αρχική χορήγηση 150 mg, το ποσοστό των ατόμων με μη φυσιολογική αύξηση βάρους ≥ 7% παρουσίασε τάση που σχετίζεται με τη δόση, με ποσοστό επίπτωσης 5% στην ομάδα του εικονικού φαρμάκου σε σύγκριση με τα ποσοστά 6%, 8% και 13% στις ομάδες XEPLION 25 mg, 100 mg και 150 mg αντίστοιχα.
Κατά τη διάρκεια της ανοιχτής περιόδου μετάβασης / συντήρησης 33 εβδομάδων της δοκιμής μακροχρόνιας πρόληψης υποτροπής, το 12% των ατόμων που έλαβαν θεραπεία με XEPLION παρουσίασαν αυτό το αποτέλεσμα (gain 7% αύξηση βάρους από τη διπλή τυφλή φάση στο τελικό σημείο). Μέσος όρος (ΣΔ) η μεταβολή βάρους από την αρχική φάση στην ανοικτή φάση ήταν + 0,7 kg.
Υπερπρολακτιναιμία
Σε κλινικές δοκιμές, παρατηρήθηκε διάμεση αύξηση της προλακτίνης στον ορό και στα δύο φύλα που έλαβαν XEPLION. Ανεπιθύμητες ενέργειες που θα μπορούσαν να υποδηλώνουν αύξηση των επιπέδων προλακτίνης (π.χ. αμηνόρροια, γαλακτόρροια, διαταραχές της εμμήνου ρύσεως, γυναικομαστία) έχουν αναφερθεί συνολικά σε
Εφέ κατηγορίας
Παράταση του διαστήματος QT, κοιλιακές αρρυθμίες (κοιλιακή μαρμαρυγή, κοιλιακή ταχυκαρδία), αιφνίδιος ανεξήγητος θάνατος, καρδιακή ανακοπή και torsades de pointes μπορεί να εμφανιστούν με τη χορήγηση αντιψυχωσικών. Περιπτώσεις φλεβικής θρομβοεμβολής, συμπεριλαμβανομένων περιπτώσεων πνευμονικής εμβολής και περιπτώσεων βαθιάς φλεβικής θρόμβωσης (συχνότητα άγνωστο).
Αναφορά υποψίας ανεπιθύμητων ενεργειών
Η αναφορά ύποπτων ανεπιθύμητων ενεργειών που συνέβησαν μετά την έγκριση του φαρμακευτικού προϊόντος είναι σημαντική καθώς επιτρέπει τη συνεχή παρακολούθηση της ισορροπίας οφέλους / κινδύνου του φαρμακευτικού προϊόντος. Οι επαγγελματίες υγείας καλούνται να αναφέρουν τυχόν υποψίες ανεπιθύμητων ενεργειών μέσω του εθνικού συστήματος αναφοράς. Στο "Παράρτημα V Το
04,9 Υπερδοσολογία
Γενικά, τα αναμενόμενα σημεία και συμπτώματα οφείλονται σε μια ενίσχυση των γνωστών φαρμακολογικών επιδράσεων της παλιπεριδόνης, π.χ. υπνηλία και καταστολή, ταχυκαρδία και υπόταση, παράταση QT και εξωπυραμιδικά συμπτώματα. Torsade de pointes και κοιλιακή μαρμαρυγή έχουν αναφερθεί σε ασθενή σε κατάσταση υπερδοσολογίας με στοματική παλιπεριδόνη. Σε περίπτωση οξείας υπερδοσολογίας, θα πρέπει να λαμβάνεται υπόψη η πιθανότητα εμπλοκής πολλαπλών φαρμάκων.
Ο χαρακτήρας παρατεταμένης αποδέσμευσης του φαρμάκου και ο μεγάλος χρόνος ημίσειας ζωής αποβολής της παλιπεριδόνης πρέπει να λαμβάνονται υπόψη κατά την αξιολόγηση των αναγκών θεραπείας και της ανάρρωσης. Δεν υπάρχει ειδικό αντίδοτο στην παλιπεριδόνη. Θα πρέπει να θεσπιστούν τα κατάλληλα γενικά υποστηρικτικά μέτρα: Δημιουργία και διατήρηση καθαρού αεραγωγού και εξασφάλιση επαρκούς οξυγόνωσης και αερισμού.
Η καρδιαγγειακή παρακολούθηση πρέπει να ξεκινήσει αμέσως και πρέπει να περιλαμβάνει συνεχή ηλεκτροκαρδιογραφική παρακολούθηση για πιθανές αρρυθμίες. Η υπόταση και η κυκλοφοριακή κατάρρευση θα πρέπει να αντιμετωπίζονται με κατάλληλα μέτρα όπως ενδοφλέβια υγρά και / ή συμπαθομιμητικούς παράγοντες. Σε περίπτωση σοβαρών εξωπυραμιδικών συμπτωμάτων, θα πρέπει να χορηγούνται αντιχολινεργικοί παράγοντες. Συνεχίστε τη στενή παρακολούθηση και ιατρική παρακολούθηση έως ότου αναρρώσει ο ασθενής.
05.0 ΦΑΡΜΑΚΟΛΟΓΙΚΕΣ ΙΔΙΟΤΗΤΕΣ
05.1 Φαρμακοδυναμικές ιδιότητες
Φαρμακοθεραπευτική ομάδα: ψυχοληπτικά, άλλα αντιψυχωσικά.
Κωδικός ATC: N05AX13.
Το XEPLION περιέχει ένα ρακεμικό μίγμα (+) - και ( -) - παλιπεριδόνης.
Μηχανισμός δράσης
Η παλιπεριδόνη είναι ένας εκλεκτικός παράγοντας αποκλεισμού των μονοαμινικών επιδράσεων, των οποίων οι φαρμακολογικές ιδιότητες είναι διαφορετικές από αυτές των παραδοσιακών νευροληπτικών. Η παλιπεριδόνη συνδέεται ισχυρά με τους σεροτονεργικούς και ντοπαμινεργικούς υποδοχείς D2 5-HT2. Η παλιπεριδόνη αποκλείει επίσης τους αλφα1-αδρενεργικούς υποδοχείς και, σε μικρότερο βαθμό, τους ισταμινεργικούς Η1- και άλφα 2- αδρενεργικούς υποδοχείς. Η φαρμακολογική δράση των (+) και (-) εναντιομερών της παλιπεριδόνης είναι ποιοτικά και ποσοτικά παρόμοια.
Η παλιπεριδόνη δεν συνδέεται με χολινεργικούς υποδοχείς. Αν και η παλιπεριδόνη είναι ένας ισχυρός ανταγωνιστής D2, ο οποίος πιστεύεται ότι ανακουφίζει από τα θετικά συμπτώματα της σχιζοφρένειας, προκαλεί λιγότερη καταληψία και μειώνει την κινητική ικανότητα σε μικρότερο βαθμό από τα παραδοσιακά νευροληπτικά. Ο κεντρικός κυρίαρχος ανταγωνισμός σεροτονίνης μπορεί να μειώσει την τάση της παλιπεριδόνης να προκαλέσει εξωπυραμιδικές παρενέργειες.
Κλινική αποτελεσματικότητα
Οξεία θεραπεία της σχιζοφρένειας
Η αποτελεσματικότητα του XEPLION στην οξεία θεραπεία της σχιζοφρένειας διαπιστώθηκε σε τέσσερις βραχυπρόθεσμες (μία 9 εβδομάδων και τρεις 13 εβδομάδων) διπλά τυφλές, τυχαιοποιημένες, ελεγχόμενες με εικονικό φάρμακο, μελέτες σταθερής δόσης σε νοσηλευόμενους ενήλικες ασθενείς με οξεία οξεία ένταση Κριτήρια DSM-IV για σχιζοφρένεια. Σταθερές δόσεις του XEPLION σε αυτές τις μελέτες χορηγήθηκαν τις ημέρες 1, 8 και 36 στη μελέτη 9 εβδομάδων και επίσης την ημέρα 64 στις μελέτες των 13 εβδομάδων. Δεν απαιτείται περαιτέρω συμπλήρωση από του στόματος αντιψυχωσικά κατά τη διάρκεια οξείας θεραπείας της σχιζοφρένειας με XEPLION. Το κύριο τελικό σημείο αποτελεσματικότητας ορίστηκε ως μείωση των συνολικών βαθμολογιών της Κλίμακας Θετικού και Αρνητικού Συνδρόμου (PANSS) όπως φαίνεται στον παρακάτω πίνακα. Η κλίμακα PANSS είναι ένα επικυρωμένο εργαλείο πολλαπλών στοιχείων που αποτελείται από πέντε διαστάσεις για την αξιολόγηση θετικών συμπτωμάτων, αρνητικών συμπτωμάτων, εννοιολογικής αποδιοργάνωσης, εχθρότητας / διέγερσης ν σχετικά με το ελεγχόμενο και το άγχος / κατάθλιψη. Η λειτουργία αξιολογήθηκε χρησιμοποιώντας την κλίμακα Personal and Social Performance (PSP). Το PSP είναι μια κλινικά επικυρωμένη κλίμακα που μετρά την προσωπική και κοινωνική λειτουργία σε τέσσερις τομείς: κοινωνικά χρήσιμες δραστηριότητες (εργασία και μελέτη), προσωπικές και κοινωνικές σχέσεις, αυτο-φροντίδα και ενοχλητικές και επιθετικές συμπεριφορές.
Σε μια μελέτη 13 εβδομάδων (n = 636) που συνέκρινε τρεις σταθερές δόσεις XEPLION (αρχική ένεση δελτοειδούς 150 mg ακολουθούμενη από 3 γλουτούς ή δελτοειδείς δόσεις των 25 mg / 4 εβδομάδες, 100 mg / 4 εβδομάδες ή 150 mg / 4 εβδομάδες) με το εικονικό φάρμακο, και οι τρεις δόσεις του XEPLION ήταν ανώτερες από το εικονικό φάρμακο στη βελτίωση της συνολικής βαθμολογίας του PANSS. Σε αυτή τη μελέτη, τόσο οι ομάδες θεραπείας των 100 mg / 4 εβδομάδες όσο και οι 150 mg / 4 εβδομάδες, αλλά όχι οι 25 mg / 4 εβδομάδες, έδειξαν στατιστική υπεροχή έναντι του εικονικού φαρμάκου για τη βαθμολογία PSP. Αυτά τα αποτελέσματα υποστηρίζουν αποτελεσματικότητα και βελτίωση πλήρους διάρκειας στο PANSS και παρατηρήθηκαν νωρίς την ημέρα 4 με σημαντικό διαχωρισμό από το εικονικό φάρμακο στις ομάδες XEPLION 25 mg και 150 mg από την 8η ημέρα.
Τα αποτελέσματα των άλλων μελετών παρείχαν στατιστικά σημαντικά αποτελέσματα υπέρ του XEPLION, με εξαίρεση τη δόση των 50 mg σε μία μόνο μελέτη (βλ. Πίνακα παρακάτω).
* Για τη μελέτη R092670-PSY-3007, δόση έναρξης 150 mg χορηγήθηκε την 1η ημέρα σε όλα τα άτομα στις ομάδες θεραπείας XEPLION, ακολουθούμενη από την εκχωρημένη δόση στη συνέχεια.
Σημείωση: Η αρνητική αλλαγή στις βαθμολογίες δείχνει βελτίωση.
Διατήρηση του ελέγχου των συμπτωμάτων και καθυστέρηση στην υποτροπή της σχιζοφρένειας
Η αποτελεσματικότητα του XEPLION στη διατήρηση του ελέγχου των συμπτωμάτων και στην καθυστέρηση της υποτροπής της σχιζοφρένειας αποδείχθηκε σε μια μακροπρόθεσμη, διπλά τυφλή, ελεγχόμενη με εικονικό φάρμακο, ευέλικτη δόση, στην οποία συμμετείχαν 849 μη ηλικιωμένα άτομα που πληρούσαν τα κριτήρια DSM-IV για σχιζοφρένεια. Αυτή η μελέτη περιελάμβανε μια ανοιχτή φάση οξείας θεραπείας και σταθεροποίησης 33 εβδομάδων, μια ελεγχόμενη με εικονικό φάρμακο διπλή-τυφλή φάση τυχαιοποίησης για την παρακολούθηση της ενδεχόμενης υποτροπής και μια ανοικτή περίοδο επέκτασης 52 εβδομάδων. Σε αυτή τη μελέτη, οι δόσεις του XEPLION περιελάμβαναν 25, 50, 75 και 100 mg που χορηγούνταν μηνιαίως. η δόση των 75 mg επιτρέπεται μόνο κατά την περίοδο επέκτασης της ανοικτής ετικέτας 52 εβδομάδων. Τα άτομα έλαβαν αρχικά ευέλικτες δόσεις (25-100 mg) XEPLION κατά τη διάρκεια μιας μεταβατικής περιόδου 9 εβδομάδων, ακολουθούμενη από μια περίοδο συντήρησης 24 εβδομάδων, όπου τα άτομα έπρεπε να έχουν βαθμολογία PANSS ≤ 75. Η προσαρμογή της δόσης επιτρέπεται μόνο στην πρώτη 12 εβδομάδες της περιόδου συντήρησης. Συνολικά 410 σταθεροποιημένοι ασθενείς τυχαιοποιήθηκαν σε XEPLION (διάμεση διάρκεια 171 ημέρες [εύρος 1 ημέρα έως 407 ημέρες]) ή σε εικονικό φάρμακο (μέση διάρκεια 105 ημέρες [εύρος 8 ημέρες έως 441 ημέρες]) μέχρι να υποτροπιάσουν. Συμπτώματα σχιζοφρένειας στο διπλή-τυφλή φάση μεταβλητής διάρκειας. Η δοκιμή διακόπηκε νωρίς για λόγους αποτελεσματικότητας καθώς παρατηρήθηκε πολύ μεγαλύτερος χρόνος υποτροπής (σελ
Παιδιατρικός πληθυσμός
Ο Ευρωπαϊκός Οργανισμός Φαρμάκων έχει παραιτηθεί από την υποχρέωση υποβολής των αποτελεσμάτων των μελετών με το XEPLION σε όλα τα υποσύνολα του παιδιατρικού πληθυσμού σε σχιζοφρένεια. Βλέπε παράγραφο 4.2 για πληροφορίες σχετικά με την παιδιατρική χρήση.
05.2 "Φαρμακοκινητικές ιδιότητες
Απορρόφηση και κατανομή
Η παλμιτική παλιπεριδόνη είναι το προφάρμακο παλμιτικού εστέρα της παλιπεριδόνης. Λόγω της εξαιρετικά χαμηλής υδατοδιαλυτότητάς του, η παλμιτική παλιπεριδόνη διαλύεται αργά μετά από ενδομυϊκή ένεση πριν υδρολυθεί σε παλιπεριδόνη και απορροφηθεί στη συστηματική κυκλοφορία. Μετά από μία μόνο ενδομυϊκή δόση, οι συγκεντρώσεις της παλιπεριδόνης στο πλάσμα αυξάνονται σταδιακά για να φτάσουν τις μέγιστες συγκεντρώσεις στο πλάσμα σε διάμεσο Τ 13 ημερών. Η απελευθέρωση της δραστικής ουσίας ξεκινά ήδη από την 1η ημέρα και επιμένει για τουλάχιστον 4 μήνες.
Μετά από ενδομυϊκή ένεση εφάπαξ δόσεων (25-150 mg) στον δελτοειδή μυ, κατά μέσο όρο, παρατηρήθηκε υψηλότερη Cmax κατά 28% σε σύγκριση με την ένεση στον γλουτό.Οι δύο αρχικές ενδομυϊκές δελτοειδείς ενέσεις 150 mg την 1η ημέρα και 100 mg την 8η ημέρα βοηθούν στην γρήγορη επίτευξη θεραπευτικών συγκεντρώσεων. Το προφίλ απελευθέρωσης και το δοσολογικό σχήμα του XEPLION οδηγούν σε συνεχείς θεραπευτικές συγκεντρώσεις. Η συνολική έκθεση της παλιπεριδόνης μετά τη χορήγηση του XEPLION ήταν ανάλογη με τη δόση σε εύρος δόσης 25-150 mg, και μικρότερη από τη δόση ανάλογη για C για δόσεις άνω των 50 mg. mg ήταν 1,8 μετά από χορήγηση στον γλουτό και 2,2 μετά από χορήγηση στο δελτοειδές.Το εύρος δόσεων των 25-150 mg κυμαίνονταν από 25 έως 49 ημέρες.
Η απόλυτη βιοδιαθεσιμότητα της παλμιτικής παλιπεριδόνης μετά τη χορήγηση του XEPLION είναι 100%.
Μετά τη χορήγηση παλμιτικής παλιπεριδόνης, τα (+) και (-) εναντιομερή της παλιπεριδόνης αλληλομετατρέπονται, φθάνοντας σε αναλογία AUC (+) / (-) περίπου 1,6-1,8.
Η δέσμευση της πρωτεΐνης πλάσματος της ρακεμικής παλιπεριδόνης είναι 74%.
Βιομετασχηματισμός και εξάλειψη
Μετά από μία εβδομάδα μετά τη χορήγηση εφάπαξ από του στόματος δόσης 1 mg 14C-παλιπεριδόνης, το 59% της δόσης απεκκρίθηκε αμετάβλητη στα ούρα, αποδεικνύοντας ότι η παλιπεριδόνη δεν μεταβολίζεται εκτενώς από το ήπαρ. Περίπου το 80% της χορηγούμενης ραδιενέργειας ανακτήθηκε στα ούρα και 11% στα κόπρανα. In vivo Ταυτοποιήθηκαν τέσσερις μεταβολικές οδοί, καμία από τις οποίες δεν αντιπροσώπευε περισσότερο από το 6,5% της δόσης: αποαλκυλίωση, υδροξυλίωση, αφυδρογόνωση και διάσπαση βενζισοξαζόλης. Αν και οι μελέτες in vitro έχουν προτείνει ρόλο για το CYP2D6 και το CYP3A4 στο μεταβολισμό της παλιπεριδόνης, δεν υπάρχουν στοιχεία in vivo ότι αυτά τα ισοένζυμα παίζουν σημαντικό ρόλο στο μεταβολισμό της παλιπεριδόνης. Φαρμακοκινητικές αναλύσεις πληθυσμού υποδεικνύουν ότι δεν υπάρχει διακριτή διαφορά στην προφανή κάθαρση της παλιπεριδόνης μετά από χορήγηση από του στόματος παλιπεριδόνης μεταξύ εκτεταμένων μεταβολιστών και φτωχών μεταβολιστών υποστρωμάτων CYP2D6. Σπουδές in vitro σε μικροσώματα ανθρώπινου ήπατος έδειξαν ότι η παλιπεριδόνη δεν αναστέλλει σημαντικά τον μεταβολισμό φαρμακευτικών προϊόντων που μεταβολίζονται από ισοένζυμα κυτοχρώματος P450, συμπεριλαμβανομένων των CYP1A2, CYP2A6, CYP2C8 / 9/10, CYP2D6, CYP2E1, CYP3A4 και CYP3A5.
Σπουδές in vitro απέδειξε ότι η παλιπεριδόνη είναι υπόστρωμα P-gp και ασθενής αναστολέας της P-gp σε υψηλές συγκεντρώσεις. Δεν υπάρχουν διαθέσιμα δεδομένα in vivo και η κλινική συνάφεια είναι άγνωστη.
Έγχυση παλμιτικής παλιπεριδόνης παρατεταμένης αποδέσμευσης έναντι παλιπεριδόνης από του στόματος παρατεταμένος
Το XEPLION αναπτύχθηκε για την απελευθέρωση παλιπεριδόνης σε διάστημα ενός μήνα, ενώ η από του στόματος παρατεταμένη αποδέσμευση παλιπεριδόνη χορηγείται σε καθημερινή βάση. Το σχήμα αρχικής φάσης για το XEPLION (150 mg / 100 mg στον δελτοειδή μυ την ημέρα 1 / ημέρα 8) αναπτύχθηκε για να επιτευχθούν γρήγορα συγκεντρώσεις παλιπεριδόνης σε σταθερή κατάσταση στην αρχή της θεραπείας χωρίς τη χρήση συμπληρώματος από το στόμα.
Γενικά, τα συνολικά επίπεδα πλάσματος της αρχικής φάσης με το XEPLION ήταν εντός του εύρους έκθεσης που παρατηρήθηκε με 6-12 mg από του στόματος παλιπεριδόνη παρατεταμένης αποδέσμευσης. Η χρήση του καθεστώτος αρχικής φάσης XEPLION επέτρεψε στους ασθενείς να παραμείνουν εντός αυτού του παραθύρου έκθεσης παρατεταμένης αποδέσμευσης παλιπεριδόνης από το στόμα 6-12 mg ακόμη και σε ημέρες χαμηλής συγκέντρωσης πριν από τη χορήγηση (Ημέρα 8 και Ημέρα 36). Λόγω της διαφοράς στα μέσα φαρμακοκινητικά προφίλ μεταξύ τα δύο φάρμακα, πρέπει να δίνεται η δέουσα προσοχή όταν γίνεται άμεση σύγκριση των φαρμακοκινητικών ιδιοτήτων τους.
Ηπατική ανεπάρκεια
Η παλιπεριδόνη δεν μεταβολίζεται εκτενώς στο ήπαρ. Αν και το XEPLION δεν έχει μελετηθεί σε ασθενείς με ηπατική δυσλειτουργία, δεν απαιτείται προσαρμογή της δόσης σε ασθενείς με ήπια έως μέτρια ηπατική δυσλειτουργία. Σε μια μελέτη με από του στόματος παλιπεριδόνη σε άτομα με μέτρια ηπατική δυσλειτουργία (τάξη Child-Plugh Β), οι συγκεντρώσεις της ελεύθερης παλιπεριδόνης στο πλάσμα ήταν παρόμοιες με αυτές σε υγιή άτομα. Δεν έχουν διεξαχθεί μελέτες με παλιπεριδόνη σε ασθενείς με σοβαρή ηπατική δυσλειτουργία.
Νεφρική ανεπάρκεια
Η διάθεση μιας εφάπαξ από του στόματος δόσης παλιπεριδόνης 3 mg δισκίων παρατεταμένης αποδέσμευσης έχει μελετηθεί σε άτομα με ποικίλους βαθμούς νεφρικής λειτουργίας. Η αποβολή της παλιπεριδόνης μειώθηκε καθώς μειώθηκε η εκτιμώμενη κάθαρση κρεατινίνης. Η συνολική κάθαρση της παλιπεριδόνης μειώθηκε κατά μέσο όρο κατά 32% σε άτομα με ήπια μειωμένη νεφρική λειτουργία (CrCl = 50 έως
Ατομα της τρίτης ηλικίας
Δεν συνιστάται προσαρμογή της δόσης μόνο με βάση την ηλικία. Ωστόσο, μπορεί να απαιτείται προσαρμογή της δόσης λόγω μειώσεων της κάθαρσης κρεατινίνης που σχετίζονται με την ηλικία (βλέπε νεφρική δυσλειτουργία παραπάνω και παράγραφο 4.2).
Βάρος
Φαρμακοκινητικές μελέτες με παλμιτική παλιπεριδόνη έδειξαν μερικές φορές χαμηλότερες (10-20%) συγκεντρώσεις παλιπεριδόνης στο πλάσμα σε υπέρβαρους ή παχύσαρκους ασθενείς από ό, τι σε ασθενείς με φυσιολογικό βάρος (βλ. Παράγραφο 4.2).
Αγώνας
Οι πληθυσμιακές φαρμακοκινητικές αναλύσεις δεδομένων από μελέτες με στοματική παλιπεριδόνη δεν αποκάλυψαν διαφορές που σχετίζονται με τη φυλή στη φαρμακοκινητική της παλιπεριδόνης μετά τη χορήγηση του XEPLION.
Φύλο
Δεν παρατηρήθηκαν κλινικά σημαντικές διαφορές μεταξύ ανδρών και γυναικών ασθενών.
Καπνός
Με βάση μελέτες in vitro διεξάγεται με τη χρήση ανθρώπινων ηπατικών ενζύμων, η παλιπεριδόνη δεν είναι υπόστρωμα για το CYP1A2. Το κάπνισμα, επομένως, δεν αναμένεται να έχει καμία επίδραση στη φαρμακοκινητική της παλιπεριδόνης. Μια πληθυσμιακή φαρμακοκινητική ανάλυση δεδομένων με δισκία παρατεταμένης αποδέσμευσης παλιπεριδόνης έδειξε ελαφρώς χαμηλότερη έκθεση παλιπεριδόνης στους καπνιστές από ό, τι στους μη καπνιστές. Ωστόσο, η διαφορά είναι απίθανο να είναι κλινικά σχετική. Το κάπνισμα δεν έχει αξιολογηθεί για το XEPLION.
05.3 Προκλινικά δεδομένα ασφάλειας
Μελέτες τοξικότητας επαναλαμβανόμενης δόσης παλμιτικής παλιπεριδόνης με ενδομυϊκή ένεση και χορηγούμενης από του στόματος παλιπεριδόνης σε αρουραίους και σκύλους έδειξαν κυρίως φαρμακολογικές επιδράσεις, όπως καταστολή και μεσολαβούμενες από την προλακτίνη επιδράσεις στους μαστικούς και γεννητικούς αδένες. Μια φλεγμονώδης αντίδραση στο σημείο της ενδομυϊκής ένεσης παρατηρήθηκε σε ζώα που έλαβαν παλμιτική παλιπεριδόνη. Περιστασιακά σχηματίζεται απόστημα.
Σε μελέτες αναπαραγωγής αρουραίων με στοματική ρισπεριδόνη, η οποία μετατρέπεται εκτενώς σε παλιπεριδόνη σε αρουραίους και ανθρώπους, παρατηρήθηκαν αρνητικές επιδράσεις στο βάρος γέννησης και την επιβίωση των απογόνων. Δεν παρατηρήθηκε εμβρυοτοξικότητα ή δυσπλασίες μετά από ενδομυϊκή χορήγηση παλμιτικής παλιπεριδόνης σε έγκυους αρουραίους έως την υψηλότερη δόση (160 mg / kg / ημέρα) που αντιστοιχεί σε 4,1 φορές το επίπεδο έκθεσης στον άνθρωπο στη μέγιστη συνιστώμενη δόση των 150 mg. Άλλοι ανταγωνιστές ντοπαμίνης, όταν χορηγείται σε έγκυα ζώα, προκαλεί δυσμενείς επιπτώσεις στη μάθηση και την κινητική ανάπτυξη των απογόνων.
Η παλμιτική παλιπεριδόνη και η παλιπεριδόνη δεν ήταν γονοτοξικές. Σε μελέτες καρκινογένεσης από το στόμα ρισπεριδόνης σε αρουραίους και ποντικούς, βρέθηκαν αυξήσεις στα αδενώματα της υπόφυσης (σε ποντίκια), ενδοκρινικά παγκρεατικά αδενώματα (σε αρουραίους) και αδενώματα μαστικών αδένων (και στα δύο είδη). Το καρκινογόνο δυναμικό του παλμιτικού παλιπεριδόνης με ενδομυϊκή ένεση αξιολογήθηκε σε αρουραίους. Υπήρξε στατιστικά σημαντική αύξηση των αδενοκαρκινωμάτων των μαστικών αδένων σε θηλυκούς αρουραίους σε 10, 30 και 60 mg / kg / μήνα. Στατιστικά σημαντική αύξηση των αδενωμάτων και των καρκινωμάτων των μαστικών αδένων έχει αποδειχθεί σε άνδρες στα 30 και 60 mg / kg / μήνα που αντιπροσωπεύουν 1,2 και 2,2 φορές το επίπεδο έκθεσης στη μέγιστη συνιστώμενη ανθρώπινη δόση των 150 mg. Αυτοί οι όγκοι μπορεί να σχετίζονται με παρατεταμένη ντοπαμίνη Ο ανταγωνισμός των υποδοχέων D2 και η υπερπρολακτιναιμία. Η συνάφεια αυτών των ευρημάτων του όγκου στα τρωκτικά ως προς τον ανθρώπινο κίνδυνο είναι άγνωστη.
06.0 ΦΑΡΜΑΚΕΥΤΙΚΕΣ ΠΛΗΡΟΦΟΡΙΕΣ
06.1 Έκδοχα
Πολυσορβικό 20
Πολυαιθυλενογλυκόλη 4000
Μονοϋδρικό κιτρικό οξύ
Άνυδρο όξινο φωσφορικό δι-νάτριο
Μονοϋδρικό φωσφορικό διένυδρο νάτριο
Υδροξείδιο του νατρίου (για ρύθμιση του pH)
Νερό για ενέσεις
06.2 Ασυμβατότητα
Αυτό το φαρμακευτικό προϊόν δεν πρέπει να αναμειγνύεται με άλλα φαρμακευτικά προϊόντα.
06.3 Περίοδος ισχύος
2 χρόνια.
06.4 Ειδικές προφυλάξεις κατά την αποθήκευση
Φυλάσσεται σε θερμοκρασία που δεν υπερβαίνει τους 30 ° C.
06.5 Φύση της άμεσης συσκευασίας και περιεχόμενο της συσκευασίας
Προγεμισμένη σύριγγα (συμπολυμερές με κυκλική ολεφίνη) με στοπ εμβόλου, φτερά λαβής σύριγγας και καπάκι ασφάλισης (ελαστικό βρωμοβουτυλίου) με βελόνα ασφαλείας 22G, 1 ½ ίντσας (0,72mm x 38,1mm) και βελόνα ασφαλείας 23G, 1 ίντσα (0,64 mm x 25,4 mm).
Συσκευασία:
Η συσκευασία περιέχει 1 προγεμισμένη σύριγγα και 2 βελόνες
06.6 Οδηγίες χρήσης και χειρισμού
Τα αχρησιμοποίητα φάρμακα και τα απόβλητα που προέρχονται από αυτό το φάρμακο πρέπει να απορρίπτονται σύμφωνα με τους τοπικούς κανονισμούς
07.0 ΚΑΤΟΧΟΣ ΑΔΕΙΑΣ ΜΑΡΚΕΤΙΝΓΚ
Janssen-Cilag International NV, Turnhoutseweg 30,
B-2340 Beerse, Βέλγιο.
08.0 ΑΡΙΘΜΟΣ ΑΔΕΙΑΣ ΜΑΡΚΕΤΙΝΓΚ
ΕΕ/1/11/672/004
041004045
09.0 ΗΜΕΡΟΜΗΝΙΑ ΠΡΩΤΗΣ ΕΓΚΡΙΣΗΣ ΑΝΑΝΕΩΣΗΣ ΤΗΣ ΑΔΕΙΑΣ
04 Μαρτίου 2011
10.0 ΗΜΕΡΟΜΗΝΙΑ ΑΝΑΘΕΩΡΗΣΗΣ ΤΟΥ ΚΕΙΜΕΝΟΥ
D.CCE Μάρτιος 2015