Ορισμός
Τα ένζυμα είναι πρωτεΐνες που παράγονται σε φυτικά και ζωικά κύτταρα, οι οποίες λειτουργούν ως καταλύτες που επιταχύνουν τις βιολογικές αντιδράσεις χωρίς να τροποποιηθούν.
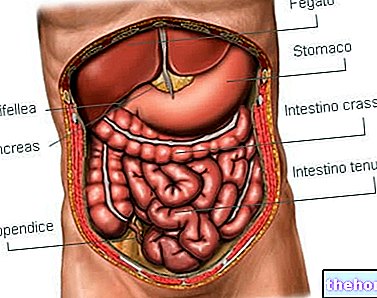
Τα ένζυμα λειτουργούν συνδυάζοντας με μια συγκεκριμένη ουσία για να τη μετατρέψουν σε διαφορετική ουσία. κλασικά παραδείγματα δίνονται από πεπτικά ένζυμα που υπάρχουν στο σάλιο, στο στομάχι, στο πάγκρεας και στο λεπτό έντερο, τα οποία εκτελούν μια ουσιαστική λειτουργία στην πέψη και βοηθούν στη διάσπαση των τροφών σε βασικά συστατικά, τα οποία στη συνέχεια μπορούν να απορροφηθούν και να χρησιμοποιηθούν από το σώμα, επεξεργασμένα από άλλα ένζυμα ή αποβάλλεται ως απόβλητο.
Κάθε ένζυμο έχει έναν συγκεκριμένο ρόλο: αυτό που διασπά τα λίπη, για παράδειγμα, δεν δρα σε πρωτεΐνες ή υδατάνθρακες. Τα ένζυμα είναι απαραίτητα για την ευημερία του οργανισμού.Η ανεπάρκεια, ακόμη και ενός μόνο ενζύμου, μπορεί να προκαλέσει σοβαρά προβλήματα.Ένα πολύ γνωστό παράδειγμα είναι η φαινυλκετονουρία (PKU), μια ασθένεια που χαρακτηρίζεται από την αδυναμία μεταβολισμού ενός απαραίτητου αμινοξέος, της φαινυλαλανίνης, του οποίου η συσσώρευση μπορεί να προκαλέσει σωματικές παραμορφώσεις και ψυχικές ασθένειες.
Βιοχημική μελέτη
Τα ένζυμα είναι συγκεκριμένες πρωτεΐνες που έχουν το χαρακτηριστικό ότι είναι βιολογικοί καταλύτες, έχουν δηλαδή την ικανότητα να διασπούν την ενέργεια ενεργοποίησης (Eatt) μιας αντίδρασης, τροποποιώντας την πορεία της έτσι ώστε μια κινητικά αργή διαδικασία να είναι ταχύτερη.
Τα ένζυμα αυξάνουν την κινητική των θερμοδυναμικά δυνατών αντιδράσεων και, σε αντίθεση με τους καταλύτες, είναι περισσότερο ή λιγότερο συγκεκριμένες: επομένως διαθέτουν ειδικότητα υποστρώματος.
Το ένζυμο δεν εμπλέκεται στη στοιχειομετρία της αντίδρασης: για να συμβεί αυτό, η τελική καταλυτική θέση πρέπει να είναι πανομοιότυπη με την αρχική.
Στην καταλυτική δράση υπάρχει σχεδόν πάντα μια αργή φάση που καθορίζει την ταχύτητα της διαδικασίας.
Όταν μιλάμε για ένζυμα δεν είναι σωστό να μιλάμε για αντιδράσεις ισορροπίας, μιλάμε, αντίθετα, για σταθερή κατάσταση (κατάσταση κατά την οποία ένας συγκεκριμένος μεταβολίτης σχηματίζεται και καταναλώνεται συνεχώς, διατηρώντας τη συγκέντρωσή του σχεδόν σταθερή με την πάροδο του χρόνου). Το προϊόν μιας αντίδρασης που καταλύεται από ένα ένζυμο είναι συνήθως το ίδιο ένα αντιδραστήριο για μια επακόλουθη αντίδραση, καταλύεται από ένα άλλο ένζυμο κ.ο.κ.
Οι διεργασίες που καταλύονται από ένζυμα αποτελούνται συνήθως από αλληλουχίες αντιδράσεων.
Μια γενική αντίδραση που καταλύεται από ένα ένζυμο (Ε) μπορεί να συνοψιστεί ως εξής:

Ε είναι το ένζυμο
S είναι το υπόστρωμα.
Το ES αντιπροσωπεύει το πρόσθετο μεταξύ ενζύμου και υποστρώματος.
Το P είναι το προϊόν.
Κ είναι η σταθερά ταχύτητας της αντίδρασης.
Ένα γενικό ένζυμο (Ε) συνδυάζεται με το υπόστρωμα (S) για να σχηματίσει το πρόσθετο (ES) με σταθερά ταχύτητας Κ1 · μπορεί να διαχωριστεί ξανά σε E + S, με σταθερή ταχύτητα Κ2, ή, (αν "ζει" αρκετά καιρό ) μπορεί να προχωρήσει στον σχηματισμό Ρ με σταθερά ταχύτητας Κ3.
Το προϊόν (Ρ) μπορεί, με τη σειρά του, να ανασυνδυασθεί με το ένζυμο και να μεταρρυθμίσει το πρόσθετο με σταθερά ρυθμού Κ4.
Όταν το ένζυμο και το υπόστρωμα αναμειγνύονται, υπάρχει ένα κλάσμα χρόνου στο οποίο η συνάντηση μεταξύ των δύο ειδών δεν έχει ακόμη συμβεί: δηλαδή, υπάρχει ένα εξαιρετικά μικρό χρονικό διάστημα (το οποίο εξαρτάται από την αντίδραση) στο οποίο το ένζυμο και το υπόστρωμα έχουν μετά από αυτήν την περίοδο, το ένζυμο και το υπόστρωμα έρχονται σε επαφή σε αυξανόμενες ποσότητες και σχηματίζεται το πρόσθετο ES. Στη συνέχεια, το ένζυμο δρα στο υπόστρωμα και το προϊόν απελευθερώνεται. Μπορεί τότε να ειπωθεί ότι το c "είναι ένα αρχικό χρονικό διάστημα στο οποίο η συγκέντρωση του πρόσθετου ES δεν μπορεί να προσδιοριστεί. Μετά από αυτήν την περίοδο, υποτίθεται ότι μια σταθερή κατάσταση καθορίζεται, δηλαδή, η ταχύτητα των διαδικασιών που οδηγούν στην απόκτηση του πρόσθετου είναι ίση με την ταχύτητα των διαδικασιών που οδηγούν στην καταστροφή του πρόσθετου.
Η σταθερά Michaelis-Menten (KM) είναι μια σταθερά ισορροπίας (αναφέρεται στην πρώτη ισορροπία που περιγράφεται παραπάνω). μπορεί να ειπωθεί, με καλή προσέγγιση (επειδή πρέπει να ληφθεί υπόψη και το K3), ότι το KM αντιπροσωπεύεται από την αναλογία μεταξύ των κινητικών σταθερών K2 και K1 (αναφέρεται στην καταστροφή και το σχηματισμό του προσαγωγού ES στην πρώτη ισορροπία που περιγράφηκε παραπάνω) Το
Μέσω της σταθεράς Michaelis-Menten έχουμε μια "ένδειξη της συγγένειας μεταξύ ενζύμου και υποστρώματος: εάν η ΚΜ είναι μικρή c" είναι "υψηλή συγγένεια μεταξύ ενζύμου και υποστρώματος, τότε η προσθήκη ES είναι σταθερή.
Τα ένζυμα υπόκεινται σε ρύθμιση (ή διαμόρφωση).
Στο παρελθόν γινόταν κυρίως λόγος για αρνητική διαμόρφωση, δηλαδή αναστολή των καταλυτικών δυνατοτήτων ενός ενζύμου, αλλά, μπορεί επίσης να υπάρξει θετική διαμόρφωση, δηλαδή, υπάρχουν είδη ικανά να ενισχύσουν τις καταλυτικές δυνατότητες ενός ενζύμου.
Υπάρχουν 4 τύποι αναστολών (που προκύπτουν από προσεγγίσεις που έγιναν σε ένα μοντέλο για να ταιριάζουν πειραματικά δεδομένα με μαθηματικές εξισώσεις):
- ανταγωνιστική αναστολή
- μη ανταγωνιστική αναστολή
- μη ανταγωνιστική αναστολή
- ανταγωνιστική αναστολή
Μιλάμε για ανταγωνιστική αναστολή όταν ένα μόριο (αναστολέας) είναι σε θέση να ανταγωνιστεί το υπόστρωμα. Για δομική ομοιότητα, ο αναστολέας μπορεί να αντιδράσει στη θέση του υποστρώματος, εξ ου και η ορολογία "ανταγωνιστική αναστολή". ο ρυθμός αντίδρασης συνεπώς εξαρτάται από αυτούς τους παράγοντες.
Για να επιτευχθεί ο ίδιος ρυθμός αντίδρασης όπως χωρίς την παρουσία του αναστολέα, είναι απαραίτητο να υπάρχει υψηλότερη συγκέντρωση υποστρώματος.
Πειραματικά αποδεικνύεται ότι, παρουσία ενός αναστολέα, η σταθερά Michaelis-Menten αυξάνεται.
Όσον αφορά, αντίθετα, η "μη ανταγωνιστική αναστολή, η αλληλεπίδραση μεταξύ του μορίου που πρέπει να λειτουργήσει ως διαμορφωτής (θετικός ή αρνητικός-αναστολέας) και του" ενζύμου "λαμβάνει χώρα σε μια τοποθεσία διαφορετική από εκείνη στην οποία η αλληλεπίδραση εμφανίζεται μεταξύ ενζύμου και υποστρώματος. μιλάμε λοιπόν για αλλοστερική διαμόρφωση (από τα ελληνικά αλλόστερος άλλος ιστότοπος).
Εάν ο αναστολέας συνδέεται με το ένζυμο, μπορεί να προκαλέσει μια αλλαγή στη δομή του ενζύμου και, κατά συνέπεια, μπορεί να μειώσει την αποτελεσματικότητα με την οποία το υπόστρωμα συνδέεται με το ένζυμο.
Σε αυτόν τον τύπο διαδικασίας, η σταθερά Michaelis-Menten παραμένει σταθερή αφού η τιμή αυτή εξαρτάται από τις ισορροπίες μεταξύ του ενζύμου και του υποστρώματος και, ακόμη και παρουσία αναστολέα, αυτές οι ισορροπίες δεν αλλάζουν.
Το φαινόμενο της μη ανταγωνιστικής αναστολής είναι σπάνιο. ένας τυπικός μη ανταγωνιστικός αναστολέας είναι μια ουσία που συνδέεται αναστρέψιμα με το παράγωγο ES προκαλώντας ESI:

Η παρεμπόδιση από την περίσσεια υποστρώματος μπορεί μερικές φορές να είναι μη ανταγωνιστική, καθώς αυτό συμβαίνει όταν ένα δεύτερο μόριο υποστρώματος συνδέεται με το σύμπλεγμα ES, προκαλώντας το σύμπλεγμα ESS.
Ένας ανασταλτικός παράγοντας ανταγωνισμού, από την άλλη πλευρά, μπορεί να συνδεθεί μόνο με το πρόσθετο ενζύμου υποστρώματος όπως στην προηγούμενη περίπτωση: η σύνδεση του υποστρώματος με το ελεύθερο ένζυμο προκαλεί μια διαμόρφωση διαμόρφωσης που καθιστά τη θέση προσβάσιμη για τον αναστολέα.
Η σταθερά Michaelis Menten μειώνεται καθώς αυξάνεται η συγκέντρωση του αναστολέα: προφανώς, επομένως, αυξάνεται η συγγένεια του ενζύμου με το υπόστρωμα.
Πρωτεάση σερίνης
Είναι μια οικογένεια ενζύμων στα οποία ανήκουν η χυμοτρυψίνη και η τρυψίνη.
Η χυμοτρυψίνη είναι ένα πρωτεολυτικό και υδρολυτικό ένζυμο που κόβει δεξιά υδρόφοβα και αρωματικά αμινοξέα.
Το προϊόν του γονιδίου που κωδικοποιεί τη χυμοτρυψίνη δεν είναι ενεργό (ενεργοποιείται με εντολή). η ανενεργή μορφή χυμοτρυψίνης αντιπροσωπεύεται από μια πολυπεπτιδική αλυσίδα 245 αμινοξέων. Η χυμοτρυψίνη έχει σφαιρικό σχήμα λόγω πέντε δισουλφιδικών γεφυρών και άλλων μικρών αλληλεπιδράσεων (ηλεκτροστατικές, δυνάμεις Van der Waals, δεσμοί υδρογόνου κ.λπ.).
Η χυμοτρυψίνη παράγεται από τα κύτταρα χυμόζης του παγκρέατος όπου περιέχεται σε ειδικές μεμβράνες και αποβάλλεται μέσω του παγκρεατικού πόρου στο έντερο, κατά τη στιγμή της πέψης της τροφής: η χυμοτρυψίνη είναι στην πραγματικότητα ένα πεπτικό ένζυμο. Οι πρωτεΐνες και τα θρεπτικά συστατικά που προσλαμβάνουμε μέσω της δίαιτας υποβάλλονται σε πέψη για να μειωθούν σε μικρότερες αλυσίδες και να απορροφηθούν και να μετατραπούν σε ενέργεια (π.χ. οι αμυλάσες και οι πρωτεάσες διασπούν τα θρεπτικά συστατικά σε γλυκόζη και αμινοξέα που φτάνουν στα κύτταρα, μέσω των αιμοφόρων αγγείων φτάνουν στην πυλαία φλέβα και από εκεί μεταφέρονται στο ήπαρ όπου υποβάλλονται σε περαιτέρω θεραπεία).
Τα ένζυμα παράγονται σε μη ενεργή μορφή και ενεργοποιούνται μόνο όταν φτάσουν στην "τοποθεσία όπου πρέπει να λειτουργήσουν". μόλις τελειώσει η δράση τους, απενεργοποιούνται. Ένα ένζυμο, μόλις απενεργοποιηθεί, δεν μπορεί να ενεργοποιηθεί εκ νέου: για να έχει "περαιτέρω καταλυτική δράση, πρέπει να αντικατασταθεί από" άλλο μόριο ενζύμου. Εάν η χιμιτρυψίνη παράγεται σε ενεργό μορφή ήδη στο πάγκρεας, θα επιτεθεί στο τελευταίο: η παγκρεατίτιδα είναι παθολογίες που οφείλονται σε πεπτικά ένζυμα που έχουν ήδη ενεργοποιηθεί στο πάγκρεας (και όχι στις απαιτούμενες θέσεις). Μερικές από αυτές αν δεν αντιμετωπιστούν εγκαίρως, οδηγούν στο θάνατο.
Στη χυμοτρυψίνη και σε όλες τις πρωτεάσες σερίνης, η καταλυτική δράση οφείλεται στην ύπαρξη ανιόντος αλκοόλης (-CH2O-) στην πλευρική αλυσίδα μιας σερίνης.
Οι πρωτεάσες σερίνης παίρνουν αυτό το όνομα ακριβώς επειδή η καταλυτική τους δράση οφείλεται σε σερίνη.
Μόλις όλο το ένζυμο έχει επιτελέσει τη δράση του, πριν μπορέσει να επαναλειτουργήσει στο υπόστρωμα, πρέπει να αποκατασταθεί με νερό · η «απελευθέρωση» σερίνης από το νερό είναι το πιο αργό στάδιο της διαδικασίας, και είναι αυτή η φάση που καθορίζει την ταχύτητα της κατάλυσης.
Η καταλυτική δράση πραγματοποιείται σε δύο φάσεις:
- σχηματισμός του ανιόντος με καταλυτικές ιδιότητες (αλιονικό ανιόν) και επακόλουθη πυρηνόφιλη επίθεση στον καρβονυλικό άνθρακα (C = O) με διάσπαση του πεπτιδικού δεσμού και σχηματισμό του εστέρα.
- επίθεση νερού με αποκατάσταση του καταλύτη (ικανός να ασκήσει ξανά την καταλυτική του δράση).
Τα διάφορα ένζυμα που ανήκουν στην οικογένεια πρωτεάσης σερίνης μπορούν να αποτελούνται από διαφορετικά αμινοξέα αλλά, για όλα αυτά, η καταλυτική θέση αντιπροσωπεύεται από το αλκοολικό ανιόν της πλευρικής αλυσίδας μιας σερίνης.
Μια υποοικογένεια πρωτεασών σερίνης είναι αυτή των ενζύμων που εμπλέκονται στην πήξη (η οποία συνίσταται στον μετασχηματισμό της πρωτεΐνης, από την ανενεργή μορφή τους σε "άλλη μορφή που είναι ενεργή"). Αυτά τα ένζυμα διασφαλίζουν ότι η πήξη είναι όσο το δυνατόν πιο αποτελεσματική και περιορίζεται ο χώρος και ο χρόνος (η πήξη πρέπει να συμβαίνει γρήγορα και πρέπει να συμβαίνει μόνο στην πληγείσα περιοχή). Τα ένζυμα που εμπλέκονται στην πήξη ενεργοποιούνται σε έναν καταρράκτη (από την ενεργοποίηση ενός ενζύμου, αποκτώνται δισεκατομμύρια ένζυμα: κάθε ενεργοποιημένο ένζυμο , με τη σειρά του ενεργοποιεί πολλά άλλα ένζυμα).
Η θρόμβωση είναι μια παθολογία λόγω δυσλειτουργίας των ενζύμων πήξης: προκαλείται από την ενεργοποίηση, χωρίς ανάγκη (επειδή δεν υπάρχει τραυματισμός), των ενζύμων που χρησιμοποιούνται στην πήξη.
Υπάρχουν ρυθμιστικά (ρυθμιστικά) ένζυμα και ανασταλτικά ένζυμα για άλλα ένζυμα: αλληλεπιδρώντας με τα τελευταία, ρυθμίζουν ή αναστέλλουν τη δραστηριότητά τους. ακόμη και το προϊόν ενός ενζύμου μπορεί να είναι αναστολέας του ενζύμου.Υπάρχουν επίσης ένζυμα που λειτουργούν όσο περισσότερο, τόσο μεγαλύτερο είναι το υπόστρωμα που υπάρχει.
Λυσοζύμη
Ο Luigi Pasteur ανακάλυψε, φτερνίζοντας σε ένα πιάτο petri, ότι στη βλέννα υπάρχει ένα ένζυμο ικανό να σκοτώνει βακτήρια: λυσοζύμη? από τα ελληνικά: liso = τι μέγεθος? zimo = ένζυμο.
Η λυσοζύμη είναι ικανή να διασπά το κυτταρικό τοίχωμα των βακτηρίων. Τα βακτήρια και γενικά οι μονοκύτταροι οργανισμοί χρειάζονται μηχανικά ανθεκτικές δομές που περιορίζουν το σχήμα τους. στο εσωτερικό των βακτηρίων υπάρχει πολύ υψηλή οσμωτική πίεση και έτσι προσελκύουν νερό. Η μεμβράνη πλάσματος θα εκραγεί αν δεν υπήρχε κυτταρικό τοίχωμα που αντιτίθεται στην είσοδο του νερού και περιορίζει τον όγκο του βακτηρίου.
Το κυτταρικό τοίχωμα αποτελείται από μια πολυσακχαριτική αλυσίδα στην οποία εναλλάσσονται μόρια Ν-ακετυλ-γλυκοζαμίνης (NAG) και μόρια Ν-ακετυλ-μουραμικού οξέος (NAM). ο δεσμός μεταξύ NAG και NAM διασπάται με υδρόλυση. Η καρβοξυλομάδα του ΝΑΜ, στο κυτταρικό τοίχωμα, εμπλέκεται σε έναν πεπτιδικό δεσμό με ένα αμινοξύ.
Μεταξύ των διαφόρων αλυσίδων, σχηματίζονται γέφυρες που αποτελούνται από ψευδοπεπτιδικούς δεσμούς: η διακλάδωση οφείλεται στο μόριο λυσίνης. η δομή στο σύνολό της είναι πολύ διακλαδισμένη και αυτό της δίνει υψηλή σταθερότητα.
Η λυσοζύμη είναι ένα αντιβιοτικό (σκοτώνει τα βακτήρια): λειτουργεί κάνοντας μια ρωγμή στο βακτηριακό τοίχωμα. όταν σπάσει αυτή η δομή (η οποία είναι μηχανικά ανθεκτική), το βακτήριο τραβάει νερό μέχρι να σκάσει. Η λυσοζύμη καταφέρνει να σπάσει τον β-1,4 γλυκοσιδικό δεσμό μεταξύ NAM και NAG.
Η καταλυτική θέση της λυσοζύμης αντιπροσωπεύεται από μια αυλάκωση που περνά κατά μήκος του ενζύμου στο οποίο εισάγεται η αλυσίδα πολυσακχαρίτη: έξι γλυκοσιδικοί δακτύλιοι της αλυσίδας τοποθετούνται στην αυλάκωση.
Στη θέση τρεις του αυλακιού c "είναι ένα τσοκ: σε αυτή τη θέση μπορεί να τοποθετηθεί μόνο ένα NAG, επειδή το NAM, το οποίο είναι υψηλότερων διαστάσεων, δεν μπορεί να εισέλθει. Η πραγματική καταλυτική θέση είναι μεταξύ των θέσεων τέσσερις και πέντε: αφού υπάρχει NAG στη θέση τρία, η τομή θα πραγματοποιηθεί μεταξύ NAM και NAG (και όχι αντίστροφα) · η κοπή, επομένως, είναι συγκεκριμένη.
Το βέλτιστο pH για να λειτουργήσει η λυσοζύμη είναι πέντε. Στην καταλυτική θέση του ενζύμου, δηλαδή μεταξύ των θέσεων τέσσερα και πέντε, υπάρχουν οι πλευρικές αλυσίδες ενός ασπαρτικού οξέος και ενός γλουταμινικού οξέος.
Βαθμός ομολογίας: μετρά τη συγγένεια (δηλαδή την ομοιότητα) μεταξύ πρωτεϊνικών δομών.
Υπάρχει ισχυρή σχέση μεταξύ λυσοζύμης και λακτόζης-συνθάσης.
Η συνθετάση λακτόζης συνθέτει λακτόζη (η οποία είναι η κύρια ζάχαρη γάλακτος): η λακτόζη είναι ένας γαλακτοζυλ γλυκοζίτης στον οποίο το c "είναι ένας β-1,4 γλυκοσιδικός δεσμός μεταξύ γαλακτόζης και γλυκόζης.
Επομένως, η συνθετάση λακτόζης καταλύει την αντίθετη αντίδραση με αυτήν που καταλύεται από τη λυσοζύμη (η οποία αντ 'αυτού διασπά τον β-1,4 γλυκοσιδικό δεσμό)
Η συνθετάση λακτόζης είναι ένα διμερές, δηλαδή αποτελείται από δύο πρωτεϊνικές αλυσίδες, η μία εκ των οποίων έχει καταλυτικές ιδιότητες και είναι συγκρίσιμη με τη λυσοζύμη και η άλλη είναι ρυθμιστική υπομονάδα.
Κατά τη διάρκεια της εγκυμοσύνης, οι γλυκοπρωτεΐνες συντίθενται από τα κύτταρα του μαστικού αδένα με τη δράση της γαλατοζυλοτρανφεράσης (έχει "ομολογία αλληλουχίας 40% με λυσοζύμη"): αυτό το ένζυμο είναι σε θέση να μεταφέρει μια γαλακτοζυλική ομάδα από μια δομή υψηλής ενέργειας σε κατά τη διάρκεια της εγκυμοσύνης, προκαλείται η έκφραση του γονιδίου που κωδικοποιεί τη γαλακτοζυλ-τρανσφεράση (υπάρχει επίσης η έκφραση άλλων γονιδίων που δίνουν επίσης άλλα προϊόντα): υπάρχει αύξηση του μεγέθους του μαστού επειδή ενεργοποιείται ο μαστικός αδένας (προηγουμένως αδρανής) ο οποίος πρέπει να παράγει γάλα. Κατά τον τοκετό παράγεται α-λακταλβουμίνη που είναι μια ρυθμιστική πρωτεΐνη: είναι σε θέση να ρυθμίσει την καταλυτική ικανότητα της γαλακτοζυλο-τρανσφεράσης (με διάκριση του υποστρώματος). Η γαλακτοζυλο-τρανσφεράση τροποποιημένη από α-λακταλαβουμίνη είναι σε θέση να μεταφέρει ένα γαλακτοζύλιο σε ένα μόριο γλυκόζης: σχηματίζοντας έναν β-1,4 γλυκοσιδικό δεσμό και δίνει λακτόζη (συνθετάση λακτόζης).
Ως εκ τούτου, η γαλακτόζη τρανσφεράση προετοιμάζει τον μαστικό αδένα πριν από τον τοκετό και παράγει γάλα μετά τον τοκετό.
Για την παραγωγή γλυκοπρωτεϊνών, η γαλακτοζυλοτρανσφεράση συνδέεται με ένα γαλακτοζύλιο και ένα NAG. κατά τη διάρκεια του τοκετού η γαλακτική λευκωματίνη συνδέεται με τη γαλακτοζυλτρανσφεράση κάνοντας την τελευταία να αναγνωρίζει τη γλυκόζη και να μην δίνει πλέον NAG λακτόζη.